Изменение давления не влияет на смещение равновесия, если не меняется число молекул газообразных веществ.
5) При увеличении концентрации исходных веществ или уменьшении концентрации продуктов реакции равновесие смещается вправо, т.е. в сторону продуктов реакции.
6) При увеличении концентрации продуктов реакции или уменьшении концентрации исходных веществ равновесие смещается влево, т. е. в сторону исходных веществ.
Концентрации газообразных веществ пропорциональны их парциальным давлениям, поэтому в кинетическом уравнении концентрацию газа можно заменять парциальным давлением:
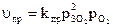
Если реакция гетерогенная, то концентрации твёрдых веществ не входят в кинетическое уравнение для константы равновесия.
Пример:
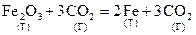 ;
; 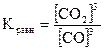
Дата добавления: 2015-08-08; просмотров: 853;
