Потенциал, замеренный в реальных условиях, называется реальным потенциалом.
На величину потенциала влияют:
1. Посторонние комплексообразующие ионы
Fe3+ / Fe2+, 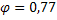 В; Fe(CN)63- / Fe(CN)64-,
В; Fe(CN)63- / Fe(CN)64-, 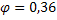 В.
В.
2. Ионная сила раствора, т.е. наличие всех примесей (индеферентных солей)
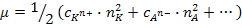
3. Ионы Н+, принимающие участие в реакции
MnO4- + 5 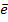 + 8H+ → Mn2+ + 4H2O;
+ 8H+ → Mn2+ + 4H2O; 
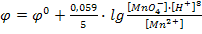
4. Ионы Н+, не принимающие участие в реакции
Fe3+ + HOH → Fe(OH)2+ + H+; Fe2+ + HOH → FeOH+ + H+
Чаще всего величина реального электродного потенциала может быть определена только экспериментально.
ОПРЕДЕЛЕНИЕ 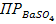 :
:
I. Берем стандартный раствор ВаSO4.
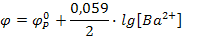
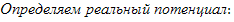
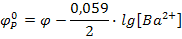
II. Берем насыщенный раствор ВаSO4.
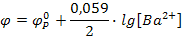
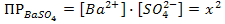
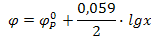
Дата добавления: 2015-08-04; просмотров: 1125;
