Электрод сравнения – хлорсеребряный
В качестве примера разберем процесс титрования хлорида железа (III) раствором хлорида олова (II):
| 0,35 |
| т.э. |
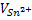
|
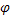
|
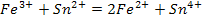

Так как 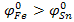 , железо будет окислять олово. На платиновом электроде установиться потенциал, характерное отношение концентраций Fe3+ к Fe2+.
, железо будет окислять олово. На платиновом электроде установиться потенциал, характерное отношение концентраций Fe3+ к Fe2+.
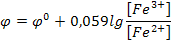
В точке эквивалентности потенциал будет определяться по формуле:
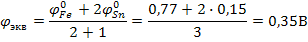
При дальнейшем добавлении ионов Sn2+ концентрация ионов железа практически меняться не будет, и платиновый электрод будет отражать зависимость: 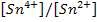
Величина скачка зависит от:
Ø первоначальной концентрации раствора (чем больше концентрация, тем больше скачок)
Ø от разности нормальных окислительно-восстановительных потенциалов протекающих процессов (чем больше разность потенциалов, тем больше скачок)
Например:
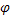
|
1) Fe3+ + Cu+ → Fe2+ + Cu2+

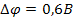
2) Fe3+ + Fi3+ → Fe2+ + Fi4+
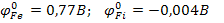
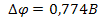
4.
Кривые титрования могут быть построены для реакций осаждения и комплексообразования.
В качестве индикаторных электродов используется металл, обратимый относительно собственных катионов (серебро). Электрод сравнения – хлорсеребряный.
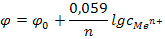
Пример:
Ag+ + Cl- = AgCl ↓
| т.э. |
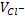
|
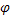
|
В первый момент времени потенциал электрода определяется начальной концентрацией ионов серебра:
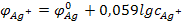
При добавлении хлорид – ионов, концентрация ионов серебра падает и, следовательно, уменьшается потенциал, т.е.
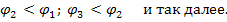
Вблизи т.э., когда почти все серебро находится в осадке, концентрация серебра находится из произведения растворимости:
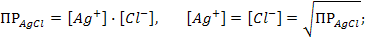
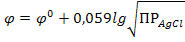
После т.э. концентрацию серебра рассчитывают также исходя из ПРAgCl по избытку хлорид – ионов:
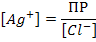
Величина скачка потенциала зависит от:
Ø Концентрации титруемого раствора (чем больше концентрация, тем больше скачок)
Ø ПР образующегося осадка (чем меньше ПР, тем больше скачок)
Ионы серебра можно определить, переведя их в малодиссоциируемые комплексы.
| т.э. |
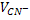
|
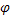
|
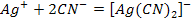
1. Ионы Аg+ расходуются на образование комплекса.
2. Все ионы связаны в комплекс.
3. За т.э. наблюдается образование малодиссоциируемого осадка Аg2(CN)2, потенциал электрода остается практически постоянным
5.
Все описанные методы потенциометрического титрования могут быть применены для анализа смеси ионов.
Примеры:
1) Определение смеси иодидов, бромидов и хлоридов методом осаждения.
Титруемый раствором AgNO3. Индикаторный электрод Аg.

В первую очередь будет оттитровываться тот ион, у кого наименьшее ПР, то есть I-.
Ионы Br – начинают оттитровываться, когда практически все ионы I-, связаны в осадок; и в последнюю очередь будут оттитровываться ионы Cl-.
На кривой титрования имеется три скачка.
| 1,52 |
| 0,77 |
| 0,15 |
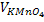
|
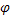
|
2) Определяем концентрацию Fe3+ и Sn2+ методом окисления - восстановления.
Рабочий раствор - перманганат калия КМn04. Индикаторный электрод – платиновый.
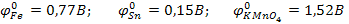
Первым оттитровывается тот ион, у которого разница с потенциалом рабочего раствора наибольшая.
То есть первым будет оттитровываться олово, и только потом железо.
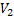
|
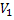
|
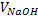
|
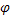
|
3) Титрование двух кислот или двух оснований различной силы:
Смесь НСl, СН3СООН титруем NaОН.
Сначала титруется более сильная кислота, дающая скачок в своей области рН, затем более слабая, в её т.э. наблюдается второй скачок.
Дифференциальное титрование двух кислот возможно только в том случае, когда отношение их констант диссоциации составляет 104 или больше.
6 .
Замерить ЭДС в потенциометрическом методе анализа можно двумя способами: компенсационным и некомпенсационным.
КОМПЕНСАЦИОННЫЙ СПОСОБ:
| EA |
| B |
| A |
| EX |
| EW |
Используется элемент Вестона. Две цепи: большая и малая.
I. Включаем в цепь ЕW с помощью движка. Добиваемся такого положения на реостате, когда ток равен нулю. При этом записываем: 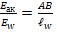 (1)
(1)
II. Включаем в цепь исследуемый элемент Ех. С помощью движка добиваемся такого положения, когда ток равен нулю. Записываем: 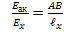 (2)
(2)
III. Разделив (1) на (2) получаем: 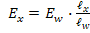
Чтобы учесть процессы внутри раствора, замер ведется при разомкнутых контактах.
Метод точный, но громоздкий.
НЕКОМПЕНСАЦИОННЫИ СПОСОБ:
| М |
| К |
| А |
| R |
| Г |
В некомпенсационном методе титрования замеряется не
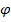 системы, а изменение тока в цепи. Раствор с двумя электродами является сопротивлением этой цепи.
системы, а изменение тока в цепи. Раствор с двумя электродами является сопротивлением этой цепи.
Меняется R при титровании, меняется ток в цепи. Для усиления тока в цепь включают аккумулятор и для того чтобы не учитывать внутреннее сопротивление цепи включают большое внешнее сопротивление. Ток регистрируется гальванометром.
Дата добавления: 2015-08-04; просмотров: 1635;
