Спектр атома водорода
Невзаимодействующие атомы излучают электромагнитные волны определенных, характерных для данного вещества частот. Спектр такого излучения состоит из отдельных линий, которые принято объединять в «серии».
На рисунке 12.2 представлен фрагмент спектра атома водорода (до λ = 7000 Ǻ).
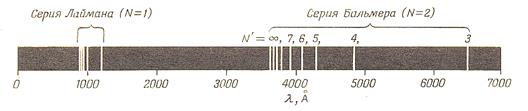
Рис. 12.2
В 1885 году Иоганн Бальмер показал, что, несмотря на кажущийся беспорядок, в распределении этих спектральных линий существуют определенные закономерности. Он нашел, что частоты линий видимой части спектра атомарного водорода могут быть связаны простой формулой
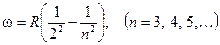
Ободренные успехом Бальмера, Лаймен, Пашен, Брэкет нашли и другие серии в излучении атома водорода. Так возникли
серия Лаймена:
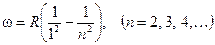
серия Пашена:

серия Брэккета:
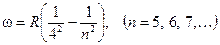
Все эти серии описываются похожими формулами, что позволило Бальмеру объединить их в одно простое математическое выражение:
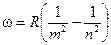 , (12.1)
, (12.1)
где: m = 1, 2, 3,...;
n = (m + 1), (m + 2),…
Это и есть объединенная формула Бальмера.
Здесь R = 2.07 · 1016 с-1 — постоянная Ридберга.
Числа 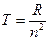 — называются спектральными термами атома водорода.
— называются спектральными термами атома водорода.
Частота любой линии атома водорода может быть представлена в виде разности соответствующих термов:
ω = T1(m) – T2(n)
Из всех этих эмпирических формул Ритц вывел «комбинационный принцип»:
«Для каждого элемента можно найти совокупность таких чисел – спектральных термов, что частота любой спектральной линии данного элемента равна разности спектральных термов этого элемента».
Вплоть до 1913 года не было никакого намека на то, каким образом можно было бы теоретически истолковать эти серии, а тем более - комбинационный принцип Ритца. Классическая электромагнитная теория объясняла спектральные линии, но их частоты не имели ничего общего с тем, что давал опыт.
Эмпирические закономерности спектра атома водорода впервые удалось объяснить после создания планетарной модели атома Бора-Резерфорда.
8. Опыт по рассеянию α-частиц. Планетарная модель атома Резерфорда
Планетарная модель атома родилась в ходе исследования рассеяния α-частиц. Схема этого эксперимента Резерфорда приведена на рис 12.3.
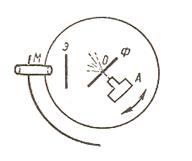
Рис. 12.3
Αльфа-частицы, излучаемые источником А, пролетев сквозь щель, попадали на экран из сернистого цинка Э. На экране возникало четкое изображение щели в виде узкой полоски.
Затем между щелью и экраном помещалась тонкая металлическая пластина, вернее, - тонкая золотая фольга Ф. При этом изображение щели на экране размывалось, что и указывало на рассеяние α-частиц веществом пластинки.
Именно в этом эксперименте был установлен поразительный факт: очень небольшая часть α-частиц (примерно 1 из 10000!) рассеивалась на значительный угол, отбрасывалась практически назад - к источнику (рис. 12.4).
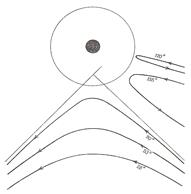
Рис. 12.4
Анализируя этот результат, Резерфорд в 1911 году пришел к следующему выводу: «Рассеяние α-частиц может быть объяснено, если предположить такой атом, который состоит из центрального положительного заряда, сосредоточенного в точке и окруженного однородным сферическим распределением противоположного электричества равной величины».
Позднее статистическая обработка результатов исследования рассеяния α-частиц позволила рассчитать линейный размер ядра атома. Он, по оценке Резерфорда, составил 10-15 м.
Планетарная модель атома с центральным положительно заряженным ядром и с электронами, вращающимися вокруг него по круговым орбитам, была лишь качественным представлением строения атома.
Резерфорд постулировал движение электронов по круговым орбитам, так как статическая модель атома с неподвижными зарядами оказывалась неустойчивой системой.
Но движущиеся по круговой орбите электроны, должны излучать энергию. Ведь согласно законам классической электродинамики, любой ускоренно движущийся заряд является источником электромагнитных волн. Такое непрерывное излучение энергии должно было очень быстро привести к истощению энергии атома и к падению электрона на ядро.
Выход в этой, казалось бы, безвыходной ситуации удалось найти в 1913 году датскому физику Нильсу Бору.
Дата добавления: 2015-08-04; просмотров: 1348;
