НАПРАВЛЕНИЕ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
Направление самопроизвольного протекания ОВР определяется так же, как и у всех других реакций – по знаку изменения свободной энергии Гиббса (ΔG0х.р). Если в результате реакции свободная энергия системы убывает, то такая реакция термодинамически разрешена (ΔG0х.р<0).
Для окислительно-восстановительных реакций существует взаимосвязь между изменением свободной энергии и электродвижущей силой (ЭДС):
ΔG0х.р = -nFΔЕ (1)
В этом уравнении n-число электронов, участвующих в ОВР, F 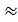 96500Кл/моль = 26,8 А∙час/моль – число Фарадея (эту величину часто называют одним фарадеем), ΔЕ – ЭДС окислительно-восстановительной системы.
96500Кл/моль = 26,8 А∙час/моль – число Фарадея (эту величину часто называют одним фарадеем), ΔЕ – ЭДС окислительно-восстановительной системы.
Для стандартных условий: ΔG0х.р = -nFΔЕ0.
Условие самопроизвольности реакции ΔG0х.р<0. В ур. (1) n и F -константы, следовательно, окислительно-восстановительная реакция термодинамически разрешена, если ΔЕ>0.
В свою очередь, ЭДС рассчитывается как разность потенциала окислителя (Еок) и восстановителя (Eвосс): ΔЕ= Еок – Eвосс > 0. Из этого соотношения следует, что ОВР будет протекать самопроизвольно в прямом направлении, если Еок > Eвосс.
Реальные ОВР начинают протекать самопроизвольно с заметной скоростью, если ЭДС системы превышает 0,4 В.
Дата добавления: 2015-07-24; просмотров: 1013;
