Общие сведения о цепных реакциях
Первые представления о цепных процессах были связаны с открытием в 1913 г. М. Боденштейном того, что существуют фотохимические реакции, имеющие квантовый выход, значительно больший 1. Им впервые было установлено, что квантовый выход реакции хлора с водородом может превышать 105. В. Нернст объяснил это явление разрывом под действием квантов световой энергии связей в молекулах водорода и хлора и образованием отдельных атомов и молекул, вступающих в реакции с другими молекулами и вновь образующихся в ходе этих реакций. Схема, предложенная Нернстом, такова:
H2 + hn ® H· + H·, или Сl2 + hn ® Cl· + Cl·,
H· + Cl2 ® Cl· + HCl, Cl· + H2 ® H· + HCl,
Cl· + H2 ® H· + HCl, H· + Cl2 ® Cl· + HCl,
H· + Cl2 ® H· + HCl, Cl· + H2 ® H· + HCl,
.................................. ..................................
.................................. ..................................
................................. ..................................
Одноатомные частицы, участвующие в этих реакциях, обладают одним неспаренным электроном, который обозначен точкой сверху.
В дальнейшем были изучены более сложные процессы с участием органических соединений, в которых также образуются и многократно появляются вновь обладающие одним или двумя неспаренными электронами группы атомов, соединенных химическими связями.
Обладающие неспаренными электронами как одноатомные частицы, так и группы атомов, соединенных химическими связями, называются свободными радикалами.
Многостадийные химические реакции, в ходе которых многократно участвуют в превращениях и вновь образуются свободные радикалы, называются химическими цепными реакциями.
Мы вынуждены подчеркнуть химический характер этих процессов, так как наряду с ними существуют ядерные цепные реакции, в которых роль, аналогичную свободным радикалам, играют нейтроны.
Минимальное число стадий реакции, в которых свободный радикал вступает в реакцию и затем образуется вновь, называется звеном цепи. В приведенном выше примере реакции взаимодействия хлора с водородом звеном цепи является:
H· + Cl2 ® Cl· + HCl, (a)
Cl· + H2 ® H· + HCl
или
Cl· + H2 ® H· + HCl, (b)
H· + Cl2 ® Cl· + HCl.
Число звеньев в реакции определяет ее длину.
Покажем на примере реакции хлора с водородом, как эти характеристики цепной реакции могут быть связаны с квантовым выходом.
Пусть квантовый выход равен g. Каждый поглощенный квант вызывает появление двух свободных радикалов Cl· или H· и приводит к появлению двух цепей. Одно звено цепи этой реакции состоит из двух стадий, на каждой из которых появляется молекула HCl. Если длина цепи равна l, то каждая цепь дает 2l молекул HCl. Таким образом, каждый поглощенный квант приводит к появлению 4l молекул и для данной реакции выполняется условие l = 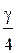 . В частности, при квантовом выходе 105 длина цепи составит 25000.
. В частности, при квантовом выходе 105 длина цепи составит 25000.
Рассмотренный выше пример цепной реакции относится к случаю, когда один вступающий в реакцию свободный радикал вызывает появление только одного нового свободного радикала. Такие реакции называются неразветвленными цепными реакциями(реакциями без размножения свободных радикалов см. рис. 15 - 1а).
В 1927 - 1929 гг. Н. Н. Семенов показал, что многие цепные реакции протекают с размножением свободных радикалов. Реакции, в которых превращение одного свободного радикала вызывает появление не менее двух новых свободных радикалов, называются разветвленными цепными реакциями (см. рис. 15 - 1а).
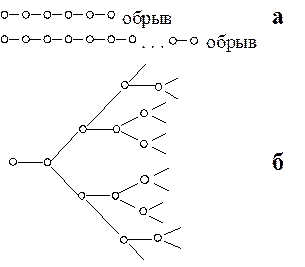 Рис. 15 - 1. Схематическое изображение неразветвленных (а) и разветвленных (б) цепных реакций.
Рис. 15 - 1. Схематическое изображение неразветвленных (а) и разветвленных (б) цепных реакций.
|
На рис. 15 - 1 схематически показаны неразветвленные и разветвленные цепные реакции.
Примером разветвленной цепной реакции может служить реакция между кислородом и водородом, для которой возможны следующие стадии:
H· + O2 ® ·OH + ·O·
·OH + H2 ® H· + H2O
·O· + H2 ® H· + ·OH.
Лавинообразный характер разветвленных цепных реакций при определенных условиях приводит к взрыву. К взрыву могут приводить и реакции, протекающие не по типу разветвленных цепных реакций. В этом случае взрыв называется тепловым и вызван тем, что проводимая без отвода теплоты реакция самоускоряется в соответствии с уравнением Аррениуса.
Теоретические представления о природе цепных процессов и методы их изучения получили широкое применение в медико-биологических исследованиях и клинической практике. Рассмотрим некоторые из них.
Дата добавления: 2015-07-22; просмотров: 1067;
