Дифференцирование кинетической кривой
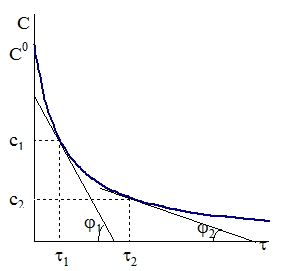 Рис. 9 - 5. Определение порядка реакции методом графического дифференцирования кинетической кривой.
Рис. 9 - 5. Определение порядка реакции методом графического дифференцирования кинетической кривой.
|
Выберем на кинетической кривой точки с концентрациями С1 и С2 и проведем касательные, как показано на рис. 9 ‑ 5. Так как угловой коэффициент каждой касательной tgj равен производной 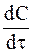 , в соответствии с уравнением (9 ‑ 7) имеем:
, в соответствии с уравнением (9 ‑ 7) имеем:
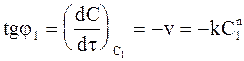 ;
; 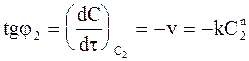 .
.
Делением частей правого равенства на соответствующие части левого равенства получим:
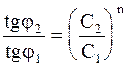 . (9 - 36)
. (9 - 36)
После логарифмирования равенства (9 - 36) находим формулу для определения порядка реакции:
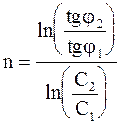 . (9 - 37)
. (9 - 37)
В основу еще одного метода определения порядка реакции положена зависимость времени полупревращения от исходной концентрации.
Логарифмируя равенство (9 - 35), имеем:
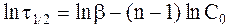 . (9 - 38)
. (9 - 38)
На рис. 9 - 6 показана зависимость логарифма времени полупревращения от логарифма исходной концентрации. Угловой коэффициент прямой tgg на рис. 9 ‑ 6 равен - (n − 1).
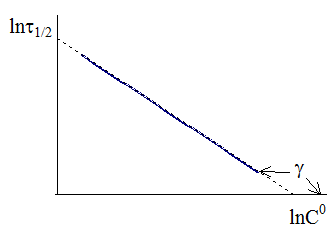 Рис. 9 - 6. Определение порядка реакции по зависимости времени полупревращения от исходящей концентрации.
Рис. 9 - 6. Определение порядка реакции по зависимости времени полупревращения от исходящей концентрации.
|
Обращаем внимание на то, что описываемые методы определения порядка реакции не пригодны для реакций 1-го порядка.
Частный порядок реакции по веществу определяют при условии, что концентрация данного вещества во много раз меньше концентраций остальных веществ. Обработка экспериментальных данных проводится с применением тех же методов, что и при определении порядка реакции в целом.
Дата добавления: 2015-07-22; просмотров: 964;
