ВИЗНАЧЕННЯ ВИТРАТ ЕНЕРГІЇ ПРИ ФІЗИЧНИХ НАВАНТАЖЕННЯХ
Неможливо безпосередньо визначити обмін енергії у м'язових волокнах.
Велика кількість непрямих лабораторних методів дозволяє визначити інтенсивність та витрати енергії у спокої і при виконанні фізичного навантаження. Багато з цих методів застосовуються з початку XX ст. Інші лише зовсім недавно стали використовуватися у фізіології м'язової діяльності. Далі ми розглянемо деякі з цих методів.
ПРЯМА КАЛОРИМЕТРІЯ
 Як уже відмічалося, тільки близько 40 % енергії, що вивільнюється при метаболізмі глюкози та жирів, йде на утворення АТФ. Решта 60 % перетворюються на тепло, тому інтенсивність та кількість вивільнюваної енергії можна визначити, вимірявши утворюване тепло. Цей метод називається прямою калориметрією.
Як уже відмічалося, тільки близько 40 % енергії, що вивільнюється при метаболізмі глюкози та жирів, йде на утворення АТФ. Решта 60 % перетворюються на тепло, тому інтенсивність та кількість вивільнюваної енергії можна визначити, вимірявши утворюване тепло. Цей метод називається прямою калориметрією.
Уперше він був описаний Зунцем та Хагеманном наприкінці XIX ст. Вони створили калориметр (рис. 4.10), що являє собою геометричне закриту камеру. Стінки камери мають мідні труби, у котрих тече вода. Коли людина перебуває у камері, тепло, що виділяє її тіло, випаровується й нагріває воду. Реєструються зміни температури води, а також повітря, котре надходить у камеру та виходить з неї під час дихання людини. Ці зміни зумовлені теплом, що виділяється тілом людини. Використовуючи сумарні показники, можна кількісно оцінити метаболізм.
Калориметри дуже дорогі, окрім того, для отримання достовірних результатів період дослідження має тривати досить довго. Єдиною реальною перевагою калориметра є те, що він безпосередньо вимірює тепло. Хоча калориметр дозволяє точно визначити загальні витрати енергії, але він не дає змоги простежити за швидкими змінами у вивільненні енергії. Саме тому енергетичний обмін під час інтенсивного навантаження не можна вивчати за допомогою калориметра. Метод прямої калориметрії нині використовується досить рідко. Значно простіше й дешевше визначити витрати енергії на основіобміну кисню й діоксиду вуглецю під час окиснювального фосфорилювання.
НЕПРЯМА КАЛОРИМЕТРІЯ
 Як уже відмічалося, метаболізм глюкози й жирів залежить від наявності О2, утворення СО2 та води. Кількість обмінюваних О2 та СО2 у легенях звичайно дорівнює тій їх кількості, котра використовується і виділяється тканинами тіла. Знаючи це, можна визначити витрати енергії, вимірявши кількість дихальних газів. Цей метод називається непрямою калориметрією, оскільки утворення тепла вимірюється непрямо, на основі дихального газообміну СО2 та О2.
Як уже відмічалося, метаболізм глюкози й жирів залежить від наявності О2, утворення СО2 та води. Кількість обмінюваних О2 та СО2 у легенях звичайно дорівнює тій їх кількості, котра використовується і виділяється тканинами тіла. Знаючи це, можна визначити витрати енергії, вимірявши кількість дихальних газів. Цей метод називається непрямою калориметрією, оскільки утворення тепла вимірюється непрямо, на основі дихального газообміну СО2 та О2.
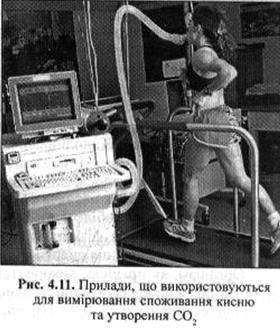
Прилад для вимірювання утворення СО2 та споживання О2 показано на рис. 4.11. Незважаючи на те що він є трохи громіздким і обмежує рухи, його можна використати в різних умовах — лабораторії, на ігровому майданчику тощо.
Дихальний коефіцієнт. Для визначення кількості енергії, котру витрачає організм, необхідно знати, що використовується в окиснювальних процесах у якості субстратів (вуглеводи, жири чи білки). Вміст вуглецю й кисню у глюкозі, вільних жирних кислотах та амінокислотах дуже відрізняється. Через це кількість кисню, використовуваного у процесі метаболізму, залежить від окиснюваного субстрату. Метод непрямої калориметрії дозволяє визначити кількість СО2 (VСО2), що виділяється, та кисню (VО2). Співвідношення цих двох величин називається дихальним коефіцієнтом (ДК).
Кількість кисню, необхідна для повного окиснення молекули вуглеводу або жиру, пропорційна вмісту вуглецю у цьому субстраті. Наприклад, глюкоза (С6Н12О6 ) містить шість атомів вуглецю. При спалюванні глюкози 6 молекул кисню використовуються для утворення 6 молекул СО2,6 молекул Н2О та 38 молекул АТФ:
6 О2 + С6Н12О6 → 6 СО2 + 6 Н2О + 38 АТФ.
Оцінюючи кількість виділеного СО2 порівняно з кількістю спожитого О2, ми встановимо, що ДК дорівнює 1,0:
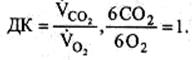
Як слідує з табл. 4.4, ДК змінюється залежно від субстрату, котрий використовується для утворення енергії. Вільні жирні кислоти містять значно більше вуглецю й водню, але менше кисню, ніж глюкоза. Візьмемо, наприклад, пальмітинову кислоту С16Н32О2. Щоб повністю окиснити цю молекулу до СО2 таН2О, необхідно 23 молекули кисню:
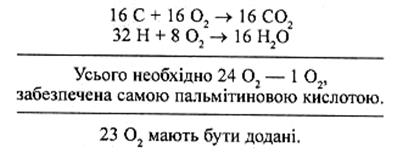
Насамкінець цей процес окиснення приводить до утворення 16 молекул СО2, 16 молекул Н2О та 129 молекул АТФ:
С16Н32О2 + 23 О2 → 16 СО2 + 16 Н2О + 129 АТФ
Для спалювання однієї молекули жиру потребується значно більше кисню, ніж для спалювання однієї молекули вуглеводів. Під час окиснення з кожної молекули використовуваного О2 утворюється приблизно 6,3 молекули АТФ (38 АТФ на 6 О2), тоді як при обміні пальмітинової кислоти — 5,6 молекули АТФ (129 АТФ на 23 О2).
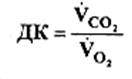
Хоча жири забезпечують більше енергії, ніж вуглеводи, для їх окиснення потребується більше кисню. Це означає, що ДК жирів значно поступається ДК вуглеводів. При використанні пальмітинової кислоти ДК дорівнює 0,70:
ДК = VСО2 = 16 = 0,70
VО2 23
Таблиця 4.4
Дата добавления: 2015-08-26; просмотров: 2386;
