Примеры полиморфных переходов
1. Для чистого железа при атмосферном давлении известно три модификации; переходы осуществляются при следующих температурах:
910оС 1400оС
a -железо«g-железо«d-железо
ОЦК ГЦК ОЦК
К.ч.=8 К.ч.=12 К.ч.=3
Это первый вид полиморфизма – с изменением координационного числа.
В связи с такими переходами, наблюдается деформация крупногабаритных эмалированных изделий, поэтому разрабатываются и внедряются легкоплавкие эмали, деформация прогиба для которых составляет 2-4,5см на 1 погонный метр (для обычных 6-14 см.)
2. Серое олово (a) термодинамически устойчиво до 13,2оС, имеет кубическую модификацию со структурой алмаза, типичный полупроводник с ковалентными связями. Белое олово (b) устойчиво при температуре выше 13,2оС, имеет объемоцентрированную тетрагональную решетку, типичный металл.
Это пример третьего типа полиморфизма, т.е. с изменением типа связей.
Белое олово может переохлаждаться ниже температуры перехода, равной 13,2оС и существовать в виде белого металла достаточно долго. Однако, его состояние при температуре ниже 13,2оС неустойчиво, поэтому сотрясения, механические повреждения, внесение затравки вызывают резкий скачкообразный фазовый переход, получивший название «оловянной чумы». Переход из a в b сопровождается резким изменением (увеличением) объема: плотность белого олова 7,3 г/см3, а серого 5,8 г/см3, поэтому белое олово переходит в серое и рассыпается в порошок.
Здесь же можно привести пример о том, как примеси ускоряют, задерживают и предотвращают фазовые переходы. Так предотвратить переход белого олова в серое при низких температурах позволяет добавка висмута 0,001% (атомы висмута в кристаллической решетке мешают перестройке ее структуры); ускоряет этот переход добавка 0,1% алюминия; в тоже время добавка 0,75% германия стабилизирует серое олово до температуры 600 С.
1000оС

 3. Графит алмаз
3. Графит алмаз
3000оС, 100 МПа
Полиморфные переходы углерода сопровождаются изменением типа связи: в алмазе связи чисто ковалентные, в слоистой структуре графита связи между слоями ван-дер-вальсовские, а внутри слоев – ковалентные.
Алмаз – кубический, прозрачный, самый твердый из всех природных материалов, диэлектрик; графит - гексагональный, черный, непрозрачный, один из самых мягких материалов, хорошо проводит электричество.
Алмаз гораздо плотнее, чем графит, когда алмаз превращается в графит объем материала увеличивается на 36%.
При комнатной температуре и атмосферном давлении стабильная модификация – это графит, а алмаз – метастабилен. Область стабильности алмаза лежит при высоких давлениях и температурах. Но скорость превращения алмаза в графит чрезмерно мала. Это пример монотропного, необратимого перехода. При температуре более 10000 алмаз легко и быстро переходит в графит. Обратный переход происходит при температуре более 3000о и давлении до 100МПа. Поэтому искусственные алмазы удалось получить лишь недавно.

 4. aZnS сфалерит b ZnS вюртцит.
4. aZnS сфалерит b ZnS вюртцит.
Это переход 2 типа. Координационное число 4 не изменяется, а изменяется тип плотнейшей упаковки - от трехслойной кубической до двухслойной гексагональной.
Полиморфный переход сфалерит вюртцит происходит при 10200С, причем структура вюртцита термодинамически устойчива при высоких температурах, однако в природе существует и вюртцит и сфалерит.
10.3. Полиморфные превращения в системе SiO2
В системе SiO2существует сложный ряд полиморфных превращений (при атмосферном давлении):
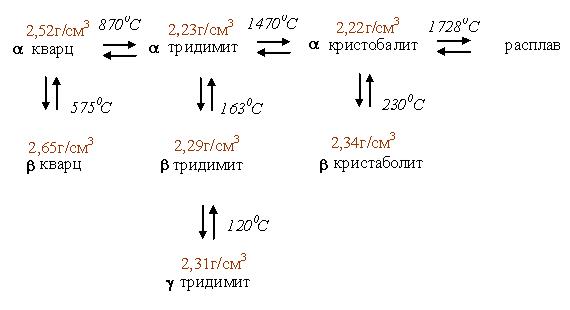
Это также 2 тип превращений, т.е. координационное число Si/O=4 не изменяется во всех модификациях, атомы кремния тетраэдрически окружены атомами кислорода. Два соседних тетраэдра соединяются вершинами. Полиморфные превращения связаны с поворотами тетраэдров.
Горизонтальные переходы проходят очень трудно и долго, в течение нескольких дней и даже месяцев. Вертикальные переходы проходят легко и быстро. Это связано с тем, что горизонтальные переходы проходят с глубоким изменением структуры, а вертикальные – с незначительным.
В присутствии минерализаторов (соединений щелочных и щелочноземельных металлов) горизонтальные переходы значительно ускоряются.
Например, существует научная теория что, если a-кварц не содержит минерализаторов, а является чистым беспримесным, то a-тридимит не образуется, а область существования кварца простирается вплоть до t0 превращения в a-кристобалит.
Объемные изменения могут достигать значительных величин (15%) и вызывать разрыв изделий, например динасового кирпича.
Кремнезем встречается в природе в основном в виде b-кварца в следующих минералах и горных породах: кварцевый песок, горный хрусталь, кварциты, песчанки.
a-кварц в природе и в искусственных продуктах не встречается.
a-тридимит в природе не встречается, т.к. при охлаждении он быстро и полностью переходит в b-тридимит, а последний в g-тридимит. То есть при обычных температурах существует в течение неограниченного времени g-тридимит.
b -кристобалит подобно g-тридимит может существовать при обычных температурах неопределенно долго и редко встречается в природе.
Расплавленный кремнезем может быть охлажден без перехода в кристаллическую фазу. При этом получается кварцевое стекло.
При сверхвысоких давлениях получены три новые модификации кремнезема.
Особенно интересен стишовит – тетрагонагональная модификация, координационное число Si/O=6,тип рутила; плотность 4,35 г/см3, тогда как плотность кварца 2,65г/см3. Вначале он был получен в лабораторных условиях при 1200-1500оС, 105 атмосфер, а через год был найден в метеоритном кратере (Аризона – США). Высказывается идея, что ядро нашей земли потому тяжелое, что в нем кремнезем имеет структуру не кварца, а стишовита.
Коэсит получен при температурах более 800о С, давлении более 350 МПа. Это прозрачная, тонкозернистая разновидность SiO2, обладающая по сравнению с кварцем повышенной плотностью 3,01 г/см3 и твердостью.
Волокнистый кремнезем (W) – получен при температуре 1200 – 1400оС путем конденсации монооксида кремнезема SiO в атмосфере разряженного кислорода. Образуются прочные волокна с плотностью 1,98 г/см3, длинной 5- 9 мм, толщиной 2 – 25 мкм.
Дата добавления: 2015-06-27; просмотров: 2503;
