Сульфатный метод переработки
Этот способ основан на переводе бериллия вместе с алюминием и железом в сернокислый раствор с оставлением основной массы диоксида кремния в нерастворимом остатке и на последующем разделении бериллия и алюминия, основанном на различии в поведении их сульфатов в растворе сульфата аммония. В связи с тем, что берилл взаимодействует с серной кислотой очень медленно, проводят подготовительные операции:
– сплавление концентрата со щелочами;
– термическое активирование берилла.
Механизм щелочной обработки, по-видимому, зависит от природы щелочи и от температуры процесса. Может применяться низкотемпературное и высокотемпературное спекание берилла со щелочными реагентами:
1– при сплавлении при температуре не выше 750–800°С, получают соединения типа Na2BeSiО4, не растворимые в воде, но взаимодействующие с серной кислотой:
Na2BeSiО4 + 2H2SО4 → Na2SО4 + BeSО4 + SiО2 + 2H2О.
После обработки серной кислотой бериллий можно перевести в раствор водным выщелачиванием селективно от кремния и остальных примесей.
2– при более высокой температуре сплавления (1000–1200 °С) образующиеся Na2BeSiО4, или СaBeSiО4, (в зависимости от применявшегося щелочного реагента) разлагаются на оксид бериллия и растворимый силикат:
Na2BeSiО4 → ВеО + Na2SiО3.
В этом случае при водном выщелачивании в раствор переходят примеси.
В настоящее время чаще применяют термическую активацию берилла, изменяющую его кристаллическую структуру. Концентрах берилла плавят при 1700°С, затем резко охлаждают, выливая плавы в закалочную ванну с водой; при этом берилл распадается, выделяя оксид бериллия. Классификация на грохоте стекловидных агломератов, полученных при закалке, позволяет отделить куски размером более 12 мм, в которых возможна рекристаллизация берилла, затрудняющая последующее взаимодействие с серной кислотой. Эти куски направляют в начало процесса.
Однако в этом случае только 50–60 % оксида способно раствориться в серной кислоте. Остальная часть — твердый раствор оксида бериллия в кремнеземе, для разрушения которого требуется вторичный нагрев до 900°С. Отсеянный спек подвергают вторичной термической обработке во вращающейся печи. После двукратной термической обработки в раствор удается перевести 90–95 % бериллия. Большая экономичность метода по сравнению с щелочной обработкой заключается в отсутствии затрат на какие-либо реагенты при почти равноценных энергетических затратах.
Для дальнейшей переработки берилла независимо от способа активирования обычно используют одинаковые схемы, так как в обоих случаях при обработке серной кислотой бериллий, а также А1 и Fe переходят в раствор в виде сульфатов. Различие заключается лишь в том, что термически активированный берилл поддается воздействию только концентрированной H2SO4, а продукт щелочной обработки берилла растворим и в разбавленной кислоте. На первый взгляд, выгоднее использовать продукт щелочной обработки, но в действительности в этом случае приходится тратить значительно больше кислоты, так как часть ее идет на нейтрализацию щелочи.
При щелочной обработке берилла на 1 кг руды тратится 13 кг карбоната натрия и 40 кг серной кислоты, в то время как на 1 кг термообработанного берилла только 26 кг серной кислоты.
Спек измельчают в шаровой мельнице, которая работает в замкнутом цикле с воздушным классификатором. Мокрое измельчение не применяют, чтобы при сульфатизации не разбавлять серную кислоту. Измельченный спек через дозатор поступает в стальной аппарат предварительного смешения. Туда же поступает серная кислота (93 %) в количестве, несколько превышающем то, которое необходимо для образования сульфатов бериллия и алюминия. Избыток серной кислоты нужен в дальнейшем для получения сульфата аммония при взаимодействии с аммиаком. Кислая пульпа впрыскивается тонкой непрерывной струей в стальной барабан, нагретый до 250–300°С. Пульпа попадает на его раскаленные стенки. При этом почти мгновенно сульфатизируются ВеО и Al2O3. Полнота сульфатизации 93–95 %. Такой метод значительно продуктивнее одновременной сульфатизации больших количеств оксидов. Отходящие газы пропускают через циклон, где оседают тонкие частицы унесенной пыли. Затем они проходят скруббер с насадкой, где SO2 и SO3 поглощаются маточником от осаждения гидроксида, содержащим NaOH и некоторое количество дисперсного Be(ОН)2.
Продукт сульфатизации выщелачивают водой по принципу противотока с целью извлечения растворимых сульфатов и отделения от SiО2. Кек (в основном SiО2) отделяют на непрерывно действующей центрифуге, применяя двукратную репульпацию. Это обеспечивает извлечение бериллия в раствор на 99 %. Получают сульфатный раствор состава, г/л: Be 13; Аl 15; Fe 2; Si 0,1; H2SO4 0,5 моль/л, который очищают от алюминия и железа. Чтобы удалить большую часть алюминия в виде дисульфата алюминия, аммония (квасцов) (наиболее распространенный метод), горячий раствор сульфатов, содержащий серную кислоту, смешивают с аммиаком, который берут в количестве, необходимом для образования квасцов (NH4)A1(SО4)2·12H2О.
Пульпа квасцов поступает в кристаллизатор, охлаждаемый до 20°С. Там ее выдерживают до тех пор, пока не удалится из раствора 75% Аl в виде квасцов. Квасцы отделяют на центрифуге непрерывного действия. Оставшийся в растворе алюминий, а также железо (после его окисления до Fe(III)) выделяют в виде гидроксидов при рН 3,8–4,2. Из очищенного раствора выделяют Ве(ОН)2. Способы выделения гидроксида бериллия описаны при рассмотрении фторидного метода.
На рисунке 2.7. приведена технологическая схема производства гидрооксида бериллия сульфатным способом. Общий выход бериллия в процессе 90 %. Состав полученного продукта представлен в таблице 3.3.
Схема, подобная представленной на рисунке 2.7, используется на единственном в СНГ предприятии по получению бериллия из рудного сырья — Ульбинском металлургическом заводе (АО «УМЗ»). Отличие заключается в отсутствии стадии выделения алюмоаммониевых квасцов — разделение алюминия и бериллия производится в процессе щелочной перечистки осажденного первичного гидроксида бериллия. Отличается также технология перечистки чернового оксида бериллия до товарного.
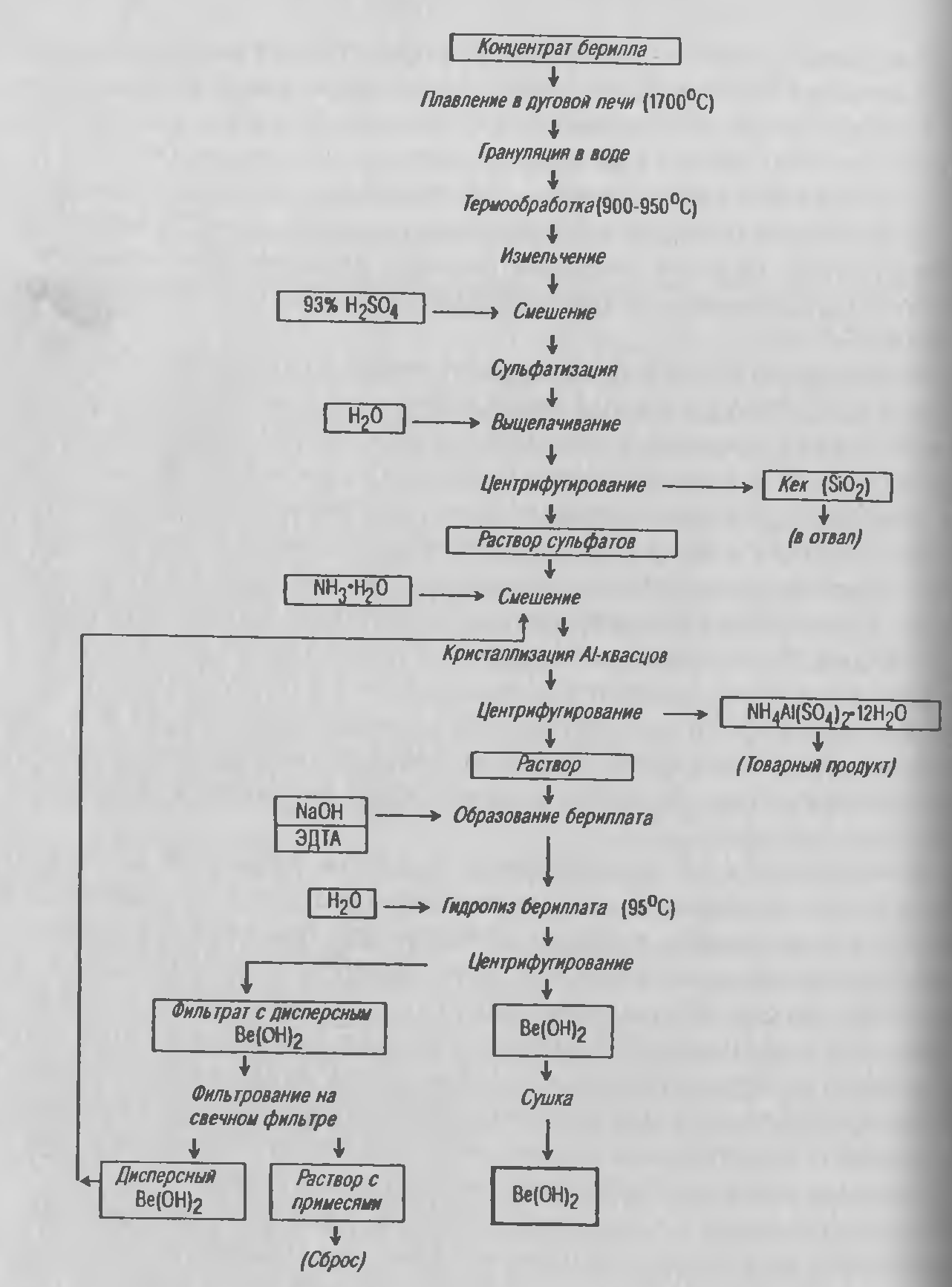
'Рисунок 3.7 — Принципиальная технологическая схема получения BeO сульфатным способом.
Дата добавления: 2015-06-22; просмотров: 2042;
