Мембранное равновесие Доннана
Измерения осмотического давления растворов ВМС полиэлектролитов могут быть связаны с ошибками, вызванными присутствием электролитов. Во избежание ошибок необходимо вводить поправки на мембранное равновесие. Теория мембранного равновесия была создана в 1911 г. английским физикохимиком Ф. Доннаном.
Мембранным равновесием Доннана (эффект Доннана) называют равновесие, устанавливающееся в системе растворов, разделенных мембраной, непроницаемой хотя бы для одного вида присутствующих в системе ионов.
Задерживаемый мембраной ион называется недиализируемым. Присутствие такого иона приводит к неравномерному распределению ионов по обе стороны мембраны при равновесном состоянии системы.
Пусть слева от мембраны находится белок в виде соли RNa, где R- - анион, имеющий коллоидные размеры и не проходящий через мембрану. Справа находится раствор NaCl, для ионов которого мембрана проницаема:
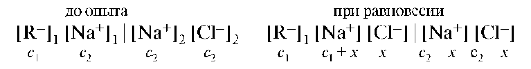
При равновесии произведение концентраций диффундирующих ионов по обе стороны мембраны должно быть одинаковым (недиализуемые ионы в расчет не принимаются). Тогда: (c1 + x)x = (c2 - x)2.
При c1 = 0х = ½с2 концентрация NaCl в равновесных растворах одинакова. При c1 >> c2 значение х очень мало, т.е. NaCl практически не переходит через мембрану, и осмотическое давление определяется только полиэлектролитом. При c1 << c2 электролит NaCl равномерно распределяется по обе стороны мембраны. Осмотическое давление определяется в этом случае только ионами низкомолекулярного электролита NaCl и составляет половину от осмотического давления полиэлектролита.
При промежуточных соотношениях концентраций в измеряемые значения осмотического давления необходимо вводить поправку, учитывающую мембранное равновесие.
Эффект Доннана обусловливает распределение электролитов в тканях организма и является причиной возникновения биопотенциалов.
15. Застудневание растворов ВМС. Свойства студней: синерезис и тиксотропия.
Гель - связнодисперсная система, содержащая сплошную пространственную сетку из частиц дисперсной фазы, в ячейках которой заключен растворитель. Гель можно рассматривать как коллоидный раствор ВМС, который под воздействием внешних факторов потерял свою текучесть. Но гель может образоваться и в процессе ограниченного набухания. Для каждого полимера существует определенная точка гелеобразования, которая соответствует тому пороговому значению концентрации раствора, при превышении которой раствор переходит в гель. Для водного раствора агар-агара при комнатной температуре точка гелеобразования соответствует концентрации 1,2%, а для желатина - 0,5%.
Понижение температуры уменьшает подвижность макромолекул и способствует гелеобразованию. Наиболее легко гелеобразование протекает при рН, соответствующем изоэлектрической точке, когда макромолекула белка по всей длине содержит противоположно заряженные функциональные группы, склонные к образованию межмолекулярных связей. Способствует гелеобразованию также прибавление к раствору электролитов, чьи ионы, связывая воду, частично дегидратируют полимер.
Гелями в организме являются мозг, кожа, хрящи, глазное яблоко.
Для большинства гелей характерна эластичность. При резком механическом воздействии на гель происходит его разжижение, но этот процесс обратим, и в состоянии покоя образовавшийся раствор снова превращается в гель. Это явление называется тиксотропией. Тиксотропия наблюдается при сотрясении мозга и последующем восстановлении его структур.
При длительном стоянии геля происходит необратимый процесс его старения, который выражается в дальнейшем упорядочении структуры, сжатии геля и выделении из него растворителя. Этот процесс называется синерезисом. Старению геля способствуют низкая температура, высокая концентрация полимера, кислотность, соответствующая изоэлектрической точке, и длительный покой в системе. С процессом синерезиса, протекающем в живых тканях, связан процесс уплотнения мяса старых животных и утончение их костей.
Дата добавления: 2015-05-26; просмотров: 10975;
