Тепловая теорема Нернста.
Прямой и простой расчет изменения энергии Гиббса, а, следовательно, и констант равновесия химических реакций не вызывает затруднений, если известны теплота химической реакции и абсолютные значения энтропии всех участников реакции. Постулат Планка дает такую возможность, т.е. возможность вычисления абсолютных значений энтропии индивидуальных веществ при любой температуре.
Тепловая теорема Нернста исторически предшествовала названному постулату и относится к тому периоду в развитии термодинамики, когда решение задачи об определении изменения энергии Гиббса реакции было связано с определенными трудностями.
Для расчета DG реакции - главной цели учения о химическом равновесии – требовались опытные определения:
- теплового эффекта реакции при какой-нибудь одной температуре
- теплоемкостей в широком интервале температур
- констант равновесия при разных температурах для того, чтобы определить значение константы интегрирования I в уравнении (III, 36).
Получаемое в конечном результате уравнение 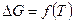 могло быть применимо в тех пределах температур, в которых определены теплоемкости и константы равновесия. Описанный нами путь являлся безукоризненным с опытной точки зрения; точность конечных расчетов полностью зависела от точности опытных данных. Очевидно, что весь этот путь являлся сугубо эмпирическим и притом очень трудоемким.
могло быть применимо в тех пределах температур, в которых определены теплоемкости и константы равновесия. Описанный нами путь являлся безукоризненным с опытной точки зрения; точность конечных расчетов полностью зависела от точности опытных данных. Очевидно, что весь этот путь являлся сугубо эмпирическим и притом очень трудоемким.
Нернст отчетливо поставил цель облегчить его теоретическими моментами. Рассуждения сводилась к следующему. Для вычисления DG химической реакции надо:
- опытным путем определить тепловой эффект реакции при какой-нибудь одной температуре
- опытным путем определить теплоемкости в широком интервале температур
- создать теорию теплоемкости для того, чтобы избежать эмпирических формул зависимости теплоемкостей от температуры
- вывести уравнение для вычисления DG химической реакции непосредственно из уравнения Гиббса-Гельмгольца, совершенно не прибегая к опытным определениям констант равновесия.
Создать теорию теплоемкости, которая бы количественно отображала действительные соотношения, не удалось.
Тем не менее, мысль Нернста вывести уравнения DG химической реакции непосредственно из уравнения Гиббса-Гельмгольца
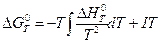 (V,14)
(V,14)
представляла особый интерес.
Очевидно, что для вычисления DG по этой формуле надо знать кроме зависимости 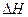 от Т, по меньшей мере значение DG при какой-либо одной температуре, чтобы определить константу интегрирования I. Наличие этой неопределенности в качестве решения уравнения (V,14) дает семейство кривых (смотри рис.10 , на котором это семейство кривых обозначено пунктирными линиями).
от Т, по меньшей мере значение DG при какой-либо одной температуре, чтобы определить константу интегрирования I. Наличие этой неопределенности в качестве решения уравнения (V,14) дает семейство кривых (смотри рис.10 , на котором это семейство кривых обозначено пунктирными линиями).
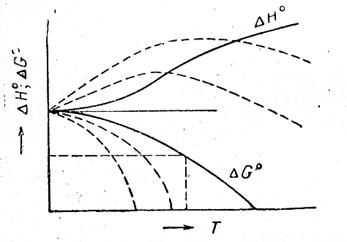
Рис.10. Зависимость теплового эффекта и изменения энергии Гиббса химической реакции от температуры.
Причем, только одна из кривых является истинной (на рис. она обозначена сплошной линией), т.к. энергия Гиббса – однозначная функция параметров состояния системы.
Руководствуясь рядом опытных указаний, Нернст высказал следующую гипотезу, получившую название тепловой теоремы Нернста: вблизи абсолютного нуля для конденсированных систем не только
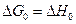 , но и
, но и
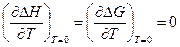 (V,15)
(V,15)
Графически это означает, что кривые DG и 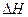 при абсолютном нуле соприкасаются, т.е. имеют общую касательную, причем эта касательная параллельна оси абсцисс (температур). Следовательно, из всего семейства кривых
при абсолютном нуле соприкасаются, т.е. имеют общую касательную, причем эта касательная параллельна оси абсцисс (температур). Следовательно, из всего семейства кривых 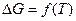 реальной является та кривая, касательная которой при Т = 0 горизонтальна.
реальной является та кривая, касательная которой при Т = 0 горизонтальна.
Если мы, как и раньше, представим 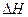 в виде
в виде
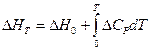
где 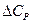 - разность теплоемкостей продуктов реакции и исходных веществ, находящихся в конденсированном состоянии, то после подстановки в уравнение (V,14) получим:
- разность теплоемкостей продуктов реакции и исходных веществ, находящихся в конденсированном состоянии, то после подстановки в уравнение (V,14) получим:
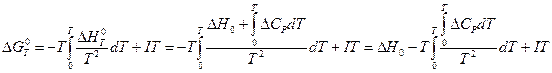 (V,16)
(V,16)
Берем теперь производную DG по Т, причем средний член справа в (V,16) дифференцируем как произведение:
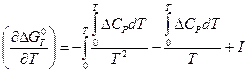 (V,17)
(V,17)
(при дифференцировании 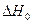 обращается в нуль, т.к. является константой и не зависит от температуры).
обращается в нуль, т.к. является константой и не зависит от температуры).
При переходе к пределу 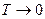 учитывается тот факт, что
учитывается тот факт, что 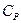 , а значит и
, а значит и 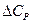 пропорциональны
пропорциональны 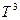 по закону Т-кубов Дебая (смотри (I, 20)). Тогда при приближении к
по закону Т-кубов Дебая (смотри (I, 20)). Тогда при приближении к 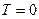 оба первых члена в правой стороне уравнения (V,17) обращаются в нуль. С учетом (V,15) получаем:
оба первых члена в правой стороне уравнения (V,17) обращаются в нуль. С учетом (V,15) получаем:
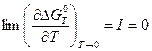
Следовательно, при температурах, близких к абсолютному нулю, константа интегрирования I в уравнении Гиббса-Гельмгольца также обращается в нуль.
Таким образом, для реакций в конденсированных системах в области абсолютного нуля уравнение (V,16) переходит в уравнение:
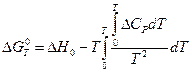
Опираясь на тепловую теорему Нернста, был сделан ряд важных и интересных заключений относительно энтропии твердых тел.
Т.к. в соответствии с (III, 26а)
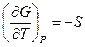 , то при Т = 0
, то при Т = 0 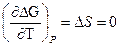
иными словами, процессы, протекающие в системе при абсолютно нуле, не изменяют ее энтропии.
Планк расширил этот вывод, допустив, что энтропия всякого однородного кристаллического вещества равна нулю, т.е.
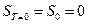
Теорему Нернста в сочетании с гипотезой Планка, касающейся значения энтропии в нулевой точке, принято называть третьим законом (началом) термодинамики (смотри § 4 второй главы).
Дата добавления: 2015-05-21; просмотров: 1321;
