ВОЗБУДИТЕЛЬ ТУБЕРКУЛЕЗА, СТРОЕНИЕ, ИЗМЕНЧИВОСТЬ МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА 1 страница
Возбудители туберкулеза — кислотоустойчивые микобактерии, открытые Р. Кохом в 1882 г. Известно несколько видов микобактерии туберкулеза: Mycobacterium tuberculosis (человеческий вид), Mycobacterium africanum (промежуточный вид) и Mycobacterium bovis (бычий вид), которые относятся к роду Mycobacterium, семейству Mycobacteriacae, порядку Actinomycetalis. Возбудителями туберкулеза у человека наиболее часто (в 92% случаев) являются микобактерии туберкулеза человеческого вида, микобактерии бычьего и промежуточного видов вызывают развитие туберкулеза у человека соответственно в 5 и 3% случаев. В современной микробиологической классификации микобактерии птичьего вида (М. avium) относят к нетуберкулезным микобактериям комплекса avium — intracellular, которые могут быть возбудителями мико-бактериоза у человека и животных.
Микобактерии туберкулеза — тонкие, прямые или незначительно изогнутые палочки длиной 1—10 (чаще 1—4) мкм, шириной 0,2—0,6 мкм, гомогенные или зернистые со слегка закругленными концами (рис 1.1), Они неподвижны, не образуют эндоспор, конидий и капсул. Морфология и размеры бактериальных клеток значительно колеблются, что зависит от возраста клеток и особенно от условий существования и состава питательной среды. С помощью электронной микроскопии выделены основные структурные элементы микобактерии туберкулеза: клеточная стенка, цитоплазматическая мембрана и ее производное — мезосома, цитоплазма, ядерное вещество — нуклеотид.
Клеточная стенка ограничивает клетку снаружи, обеспечивая механическую и осмотическую защиту. Электронно-микроскопиче-ски в клеточной стенке выделяют три слоя толщиной по 10 нм, поверхностный — микрокапсула — состоит из полисахаридов и играет важную роль в жизнедеятельности микобактерии, в том числе обеспечивает их устойчивость к неблагоприятным воздействиям. В клеточной стенке находятся видоспецифические антигены. Вакцины, приготовленные из клеточных стенок туберкулезных микобактерии, имеют разные вирулентность и иммуногенность. Наиболее выраженный иммунитет вызывают вакцины из клеточных стенок высоковирулентных микобатерий. Клеточные стенки вызывают в организме здоровых животных развитие повышенной чувствительности замедленного типа (ПЧЗТ), антителообразование. Однако их сильные сенсибилизирующие свойства и наличие в них токсического корд-фактора (фактора вирулентности) значительно осложняют гипериммунизацию этой фракцией микобактерии тубер-
Рис 11 Микобактерия туберкулеза Негативное контрастирование х 35 ООО
кулеза [Авербах М. М. и др., 1976; Романова Р. Ю., 1981]. Задача заключается в выделении из фракций клеточных стенок компонентов, обладающих высокой протективной активностью.
Согласно современным представлениям, в состав цитоплазмати-ческой мембраны, расположенной под клеточной стенкой, входят липопротеидные комплексы. С ней связаны различные ферментные системы, в частности окислительно-восстановительные. В цитоплаз-матической мембране осуществляются процессы, ответственные за
специфичность реакций микобактериальной клетки на окружающую среду.
Цитоплазматическая мембрана микобактерии туберкулеза путем инвагинации в цитоплазму формирует внутрицитоплазмати-ческую мембранную систему, или мезосому. Мезосомы полифункциональны. С ними связана локализация многих ферментных систем, они участвуют в синтезе материала клеточной стенки, выполняют роль посредника между ядром и цитоплазмой. Отмечено слабое развитие или отсутствие мезосом у авирулентных штаммов микобактерии туберкулеза и их L-форм [Кац Л. Н., Волк А. В., 1974]. Цитоплазма микобактерии туберкулеза состоит из гранул и вакуолей различной величины. Основная часть мелкогранулярных включений представлена рибосомами, на которых синтезируется специфический белок.
Ядерная субстанция микобактерии туберкулеза определяет специфические свойства клетки, важнейшими из которых являются синтез белка и передача наследственных признаков потомству. Установлено, что основным способом размножения этих бактерий является деление материнских клеток на две дочерние.
Установлено, что носителем генетической информации бактерий являются не только хромосомы, но и в нехромосомные элементы — плазмиды. Основное различие между хромосомами и плазмидами заключается в их размерах. Хромосома во много раз крупнее плаз-миды и соответственно несет большое количество генетической информации. Возможно взаимодействие плазмид с хромосомой. Плаз-миды благодаря малому размеру хорошо приспособлены к переносу из клетки в клетку. Исследования плазмид имеют не только теоретическое, но и практическое значение. Существует мнение, что гены устойчивости микобактерии туберкулеза к химиопрепаратам локализованы как на хромосоме, так и на плазмиде [Konny М., ParentiF., 1980].
Описаны многочисленные морфологические варианты микобактерии: гигантские формы с колбовидно утолщенными разветвлениями, нитевидные, мицелиеподобные и булавовидные, дифтероидные и актиномикотические формы. Микобактерии туберкулеза могут быть длиннее или короче, толще или тоньше обычных, гомогенны или зернисты. Иногда они представляют собой цепочки или отдельные скопления кокковидных зерен.
Явление изменчивости микобактерии туберкулеза было обнаружено вскоре после их открытия. Уже в 1888 г. И. И. Мечников сообщил, что в культурах, кроме типичных палочек Коха, встречаются полиморфные формы этих микроорганизмов в виде коротких, соединенных попарно звеньев и гигантских образований с колбовидными разветвлениями. Первое сообщение о возможности существования у микобактерии туберкулеза фильтрующихся форм относится к 1910 г. (A. Fontes). При химиотерапии экспериментального деструктивного туберкулеза, а также после ее прекращения в гомогенатах из стенки каверны, пропускаемых через бактериальные фильтры с размером пор 0,2 мкм, были обнаружены 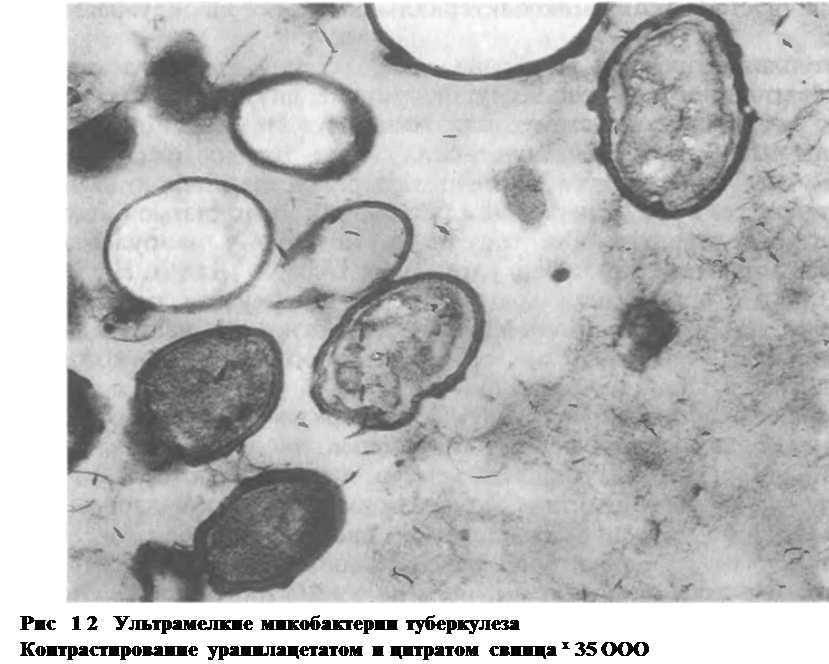
очень мелкие, с упрощенной структурой формы возбудителя туберкулеза, названные ультрамелкими (рис. 1.2). Затем было показано, что эти формы путем многократных биологических пассажей способны реверсировать в классическую палочковидную форму [ХоменкоА. Г. и др., 1982, 1989]. Одним из видов изменчивости многих бактерий является образование L-форм. Доказана способность к образованию L-форм и у микобактерии туберкулеза [Дорожкова И. Р., 1974; Шмелев Н. А., ЗемсковаЗ. С, 1974]. При этом было обнаружено, что трансформация микобактерии в L-формы усиливается под влиянием противотуберкулезных препаратов. В мокроте «абациллярных» больных с деструктивными формами туберкулеза могут находиться L-формы микобактерии, способные длительно пребывать в организме и в дальнейшем при соответствующих условиях реверсировать в палочковидный вариант [ХоменкоА. Г. и др., 1980]. Следовательно, абациллирование каверн таких больных еще не означает их стерилизации в отношении микобактерии туберкулеза.
Наряду с морфологической изменчивостью микобактериям туберкулеза свойственна широкая изменчивость и других признаков, в частности кислотоустойчивое™. Последняя проявляется способностью сохранять окраску даже при интенсивном обесцвечивании кислым спиртом и является характерной особенностью всех видов микобактерии, обусловленной высоким содержанием в них миколовой кислоты и липидов. Частичная или полная утрата кислотоустойчивости ведет к образованию смешанной, состоящей из кислотоустойчивых и некислотоустойчивых особей, или полностью некислотоустойчивой популяции.
Микобактерии туберкулеза весьма устойчивы к воздействию факторов окружающей среды. В естественных условиях при отсутствии солнечного света их жизнеспособность может сохраняться в течение нескольких месяцев, при рассеянном свете возбудители погибают через 1—IV2 мес. В уличной пыли микобактерии туберкулеза сохраняются до 10 дней, на страницах книг — до 3 мес, в воде — до 5 мес В то же время облученная солнечным светом культура микроорганизмов погибает в течение IV2 ч, а под воздействием ультрафиолетовых лучей — через 2—3 мин. При кипячении влажной мокроты микобактерии погибают через 5 мин, высушенной мокроты — через 25 мин. Соединения, выделяющие свободный активный хлор (3—5% растворы хлорамина, 10—20% растворы хлорной извести и др.), вызывают гибель микобактерии туберкулеза в течение 3—5 ч.
Микобактерии туберкулеза считаются аэробами, хотя имеются сведения, что некоторые их виды можно рассматривать как факультативные анаэробы. Размножаются эти микобактерии очень медленно (одно деление клетки происходит за 14—18 ч). Микроскопически видимый рост микроколоний, культивируемых на жидких средах при температуре 37°С, выявляется на 5—7-е сутки, видимый рост колоний на плотных средах, культивируемых при той же температуре, — на 14—20-е сутки.
Для нормального развития микобактерии туберкулеза требуются специальные питательные среды, содержащие углерод, азот, кислород, водород, фосфор, магний, калий, натрий, железо, хлор и серу. Эти микроорганизмы нуждаются и в некоторых факторах роста, к числу которых относятся соединения, родственные витаминам группы В, биотин, никотин, рибофлавин и др. Все эти факторы входят в состав применяемых для культивирования микобактерии туберкулеза специальных питательных сред, из них выделяют среды, содержащие глицерин, белковые (яичные, сывороточные, картофельные) и безбелковые (синтетические) среды, в состав которых входят минеральные соли. По консистенции различают плотные, полужидкие и жидкие среды. Наиболее широко применяются плотные яичные среды Левенштейна—Йенсена, Огавы, Петраньяни и Гельбера, разнообразные агаровые среды Миддбрука, синтетические и полусинтетические среды Сотона, Дюбо, Проскауэра—Гека, Шулы, Школь-никовой и др.
На жидких питательных средах микробактерии туберкулеза растут в виде сухой морщинистой пленки (Р-форма) кремового цвета, поднимающейся на стенки сосуда, среда при этом остается прозрачной. При внутриклеточном развитии микобактерии, а также при культивировании их на жидких средах хорошо выделяется характерный корд-фактор (трегалоза-6,6-димиколат). Он обнаруживается на поверхности клеток многих микобактерии и, по мнению некоторых исследователей, имеет отношение к их вирулентности, способствуя сближению микробных клеток и росту их в виде серпан-тинообразных кос.
На плотных средах микобактерии туберкулеза растут в виде светло-кремового морщинистого или суховатого чешуйчатого налета, образуют колонии с неровными краями, приподнятые в центре, по мере роста они приобретают бородавчатый вид, напоминающий цветную капусту.
Под влиянием антибактериальных веществ микобактерии туберкулеза могут приобретать лекарственную устойчивость. Культуры таких микобактерии не всегда типичны, они могут быть влажными, мягкими (S-вариант), иногда содержать отдельные гладкие или пигментированные колонии.
1.2. ПАТОГЕНЕЗ
Микобактерии туберкулеза могут попадать в организм различными путями: аэрогенно, энтерально (через желудочно-кишечный тракт), через поврежденную кожу и слизистые оболочки, через плаценту при развитии плода. Однако основным путем заражения является аэрогенный.
Определенную защитную роль при аэрогенном заражении играет система мукоциллиарного клиренса, позволяющая частично вывести попавшие в бронхи частицы пыли, капли слизи, слюны и мокроты, содержащие микроорганизмы. При энтеральном заражении определенное значение может иметь всасывающая функция кишечника.
Локальные изменения в месте внедрения микобактерии обусловлены прежде всего реакцией полинуклеарных клеток, которая сменяется более совершенной формой защитной реакции с участием макрофагов, осуществляющих фагоцитоз и разрушение микобактерии. Процесс взаимодействия легочных макрофагов с различными микроорганизмами, в том числе микобактериями туберкулеза, сложен и до конца не изучен. Результат взаимодействия макрофагов и микобактерии определяется состоянием иммунитета, уровнем ПЧЗТ, развивающейся в процессе туберкулезной инфекции, а также рядом других факторов, в том числе обусловливающих переваривающую способность макрофагов.
Фагоцитоз состоит из трех фаз: фазы соприкосновения, когда макрофаги с помощью рецепторов на клеточной мембране фиксируют микобактерии; фазы проникновения микобактерии внутрь макрофага путем инвагинации стенки макрофага и «окутывания» микобактерии; фазы переваривания, когда лизосомы макрофагов сливаются с фа госомами, содержащими микобактерии. Выделяющиеся в фаголизосомы ферменты разрушают микобактерии. В процессе фагоцитоза важная роль принадлежит также механизмам перекис-ного окисления [Charaparas D., 1982; Collins F., 1982].
Микобактерии туберкулеза, как и некоторые другие микроорганизмы, попадая в макрофаги, могут сохраняться и даже продолжать размножение. В тех случаях, когда процесс переваривания микобактерий блокируется, происходят разрушение макрофагов и выход микобактерии из поглотивших их клеток.
Макрофаги, фагоцитировавшие микобактерии и осуществляющие их переваривание, выделяют во внеклеточное пространство фрагменты разрушенных микобактерии, протеолитические ферменты, медиаторы (в том числе интерлейкин-1), которые активируют Т-лимфоциты, в частности Т-хелперы. Активированные Т-хелперы выделяют медиаторы — лимфокины (в том числе интерлейкин-2), под влиянием которых происходит миграция новых макрофагов к месту локализации микобактерии. Одновременно подавляется синтез фактора угнетения миграции, возрастает ферментативная активность макрофагов под влиянием фактора активации макрофагов. Активированные лимфоциты выделяют также кожно-реактивный фактор, который обусловливает воспалительную реакцию, повышение сосудистой проницаемости. С этим фактором связывают подавление ПЧЗТ и положительной туберкулиновой реакции [Медуницын Н. В. и др., 1980]. Кроме Т-хелперов, на состояние иммунитета значительно влияют Т-супрессоры и суп рессорные моноциты, которые угнетают иммунный ответ.
Помимо Т-лимфоцитов и макрофагов, важная роль в патогенезе туберкулезного процесса принадлежит веществам, освобождающимся при разрушении микобактерии. Эти вещества (фракции) подробно изучены [Seibert F. В., 1982; Goren М., 1982]. Доказано, что корд-фактор (фактор вирулентности микобактерии туберкулеза, обусловливающий их рост на плотной питательной среде в виде «кос»), провоцирует острый воспалительный процесс, а сульфатиды повышают токсичность корд-фактора и, главное, подавляют образование фаголизосом в макрофагах, что предохраняет внутриклеточно расположенные микобактерии от разрушения.
При интенсивном размножении микобактерии в организме человека вследствие малоэффективного фагоцитоза выделяется большое число токсичных веществ, индуцируется резко выраженная ПЧЗТ, которая способствует появлению экссудативного компонента воспаления с развитием казеозного некроза и его размножения. В этот период увеличивается число Т-супрессоров, снижается число Т-хелперов, что приводит к угнетению ПЧЗТ. Это обусловливает прогрессирование туберкулезного процесса.
При сравнительно небольшой бактериальной популяции в условиях ПЧЗТ и эффективного фагоцитоза отмечается образование туберкулезных гранулем. Такая гранулема развивается в результате реакций ПЧЗТ [Авербах М. М. и др., 1974]. Скопление мононук-леаров вокруг нейтрофилов, содержащих антиген, и их последующая трансформация происходят под регулирующим влиянием лимфоки-нов, вырабатываемых Т-лимфоцитами (в частности, Т-хелперами) и являющихся медиаторами гранулематозной реакции. Поскольку величина бактериальной популяции, а также характер течения иммунологических ракций на разных этапах туберкулезной инфекции меняются, морфологические реакции у заболевших туберкулезом характеризуются большим разнообразием.
В зависимости от места внедрения микобактерии туберкулеза воспалительный очаг, или первичный аффект, может образоваться в легких, ротовой полости, миндалинах, кишечнике и др. В ответ на образование первичного аффекта развивается специфический процесс в регионарных лимфатических узлах и формируется первичный туберкулезный комплекс. Установлено, что первичный туберкулез, развивающийся в результате первого контакта макроорганизма с возбудителем, может проявляться не только в виде первичного туберкулезного комплекса, как это считалось ранее. В результате первичного заражения возможно развитие туберкулеза внутригрудных лимфатических узлов, плеврита, туберкулемы, очагового процесса.
Первичный туберкулез в результате «свежего» заражения развивается лишь у 7—10% инфицированных лиц, остальные переносят первичную туберкулезную инфекцию без клинических проявлений. Наступившее заражение проявляется лишь в изменении туберкулиновых реакций.
Еще В. И. Пузик (1946), А. И. Каграманов (1954) и др. установили, что формированию первичного комплекса нередко предшествует период «латентного микробизма», при котором микобактерии туберкулеза, попадая в организм, какое-то время находятся в нем, не вызывая воспалительной реакции. При этом микобактерии чаще обнаруживаются в лимфатических узлах, особенно внутригрудных. В этих случаях локальные изменения в легких или других органах в виде очагов первичного туберкулеза возникают в поздний период первичной инфекции и не в месте проникновения микобактерии в организме, а в участках, наиболее благоприятных для развития туберкулезного воспаления.
Отсутствие клинико-морфологических проявлений первичной туберкулезной инфекции может быть объяснено высоким уровнем естественной резистентности к туберкулезу, а также может быть следствием приобретенного в результате вакцинации БЦЖ иммунитета.
При наличии локальных проявлений первичный туберкулез может протекать с развитием распространенного процесса по осложненному типу или, что в настоящее время наблюдается значительно чаще, по неосложненному типу с ограниченной воспалительной реакцией.
Как правило, первичный туберкулез заживает с небольшими остаточными изменениями, что, по-видимому, связано с высокой естественной резистентностью и проведением массовой вакцинации и ревакцинации БЦЖ.
Сохраняющиеся в остаточных очагах микобактерии или их измененные формы должны рассматриваться как туберкулезный антиген, наличие которого необходимо для поддержания сенсибилизированными лимфоцитами специфического иммунитета. Определенная, правда, еще малоизученная роль в поддержании противотуберкулезного иммунитета принадлежит В-клеточному иммунитету и генетическим механизмам.
Получены доказательства роли наследственности в течение ту» беркулезного процесса. Генетические факторы влияют на ответ иммунной системы при размножении микобактерии туберкулеза в организме человека и, в частности, определяют взаимодействие между макрофагами, Т- и В-лимфоцитами, продукцию лимфокинов, монокинов и других цитокинов Т- и В-лимфоцитами и макрофагами, комплексный иммунный ответ, от которого зависит чувствительность или устойчивость к развитию туберкулеза. Выявлено сцепление HLA-генотипов с заболеванием туберкулезом в семьях, в которых больны туберкулезом родители и дети.
Накопление некоторых специфичных типов HLA в группах больных с неблагоприятным течением болезни свидетельствует об ассоциации определенных генов HLA-комплекса (преимущественно ло-кусов В и DR с предрасположенностью к туберкулезу) [Хоменко А. Г., 1985].
Период первичного инфицирования может завершиться излечением с минимальными (малыми) или довольно выраженными остаточными изменениями. У таких людей развивается приобретенный иммунитет. Сохранение в остаточных очагах персистирующих микобактерии не только поддерживает приобретенный иммунитет, но и одновременно создает риск эндогенной реактивации туберкулезного процесса вследствие реверсии измененных форм возбудителя туберкулеза в бактериальную форму и размножения микобактери-альной популяции.
Реверсия персистирующих форм микобактерии в размножающиеся происходит в условиях эндогенной реактивации туберкулезных очагов и других остаточных изменений. Механизм эндогенной реактивации, а также развитие туберкулезного процесса изучены недостаточно.
В основе реактивации лежат прогрессирующее размножение бактериальной популяции и увеличение количества микобактерии [Хоменко А. Г., 1986]. Однако до настоящего времени остается неизвестным, что именно и какие условия способствуют реверсии возбудителя туберкулеза, находившегося в персистирующем состоянии. Установлено, что реактивация туберкулеза и развитие различных его клинических форм чаще наблюдаются у лиц с остаточными изменениями при наличии факторов, снижающих иммунитет.
Возможен и другой путь развития вторичного туберкулеза — экзогенный, связанный с новым (повторным) заражением микобак-териями туберкулеза (суперинфекция). Но и при экзогенном пути развития вторичного туберкулеза недостаточно проникновения микобактерии в уже инфицированный организм даже при массивной повторной суперинфекции. Необходима совокупность ряда условий и факторов риска, снижающих иммунитет. Вторичный туберкулез характеризуется большим разнообразием клинических форм. Основные разновидности патоморфологических изменений в легких и других органах характеризуются: а) очагами с преимущественно продуктивной тканевой реакцией, благоприятным, хроническим течением и тенденцией к заживлению; б) инфильтративно-пневмоническими изменениями с преимущественно экссудативной тканевой реакцией и тенденцией к развитию казеозного некроза или рассасыванию возникшей воспалительной реакции; в) туберкулезной каверной — результатом разложения образовавшихся казеозных масс и их отторжения через дренажные бронхи с образованием полости распада.
Различные сочетания основных патоморфологических изменений туберкулеза создают предпосылки для чрезвычайно большого разнообразия туберкулезных изменений, особенно при хроническом течении болезни со сменой периодов обострения и затихания процесса. К этому нужно добавить, что из сформировавшихся зон поражения микобактерии могут распространяться с током лимфы или крови в непораженные участки и различные органы. Исход болезни зависит от ее течения — прогрессирующего или регрессирующего, эффективности лечения и обратимости изменений, сформировавшихся в процессе болезни. Доказано, что в условиях голодания и даже при недостаточном питании, особенно когда в рационе недостаточное количество белков и витаминов, нередко возникает реактивация туберкулеза. К факторам, способствующим реактивации, относятся и различные заболевания: сахарный диабет, лимфогранулематоз, силикоз, язвенная болезнь желудка и двенадцатиперстной кишки, состояние после резекции желудка и двенадцатиперстной кишки, хронические воспалительные заболевания легких, психические заболевания, протекающие с депрессивным синдромом, алкоголизм, стрессовые ситуации, СПИД, длительный прием глюкокортикоидов, цитостатиков и иммунодепрес-сантов. Течение и исходы туберкулеза следует рассматривать только в условиях проводящейся специфической химиотерапии, которая применяется всем больным активным туберкулезом. В процессе химиотерапии отмечается уменьшение популяции микобактерии вследствие разрушающего влияния химиопрепаратов на возбудителей туберкулеза. Вследствие этого резко снижается число микобактерии, создаются более благоприятные условия для репара-тивных процессов и саногенеза. Вместе с тем при применении самых эффективных комбинаций современных химиопрепаратов отмечается разное течение туберкулезного процесса: регрессия с последующим заживлением, стабилизация процесса без клинического излечения с сохранением каверны, туберкулемы или других изменений, временное затихание воспалительного процесса с последующим возникновением обострения, развитием хронического процесса или прогрессированием заболевания.
Таким образом, уменьшение популяции микобактерии под влиянием специфических химиопрепаратов далеко не всегда приводит к излечению. Прекращение туберкулезного процесса и последующее излечение зависят не только от уменьшения популяции микобактерии, но и от способности репаративных процессов организма обеспечить регрессию туберкулезного процесса и его прекращение.
1.3. ПАТОЛОГИЧЕСКАЯ АНАТОМИЯ
1.3.1. Туберкулезное воспаление
Патоморфологические изменения в органах и тканях при туберкулезе многообразны и зависят от формы, стадии, локализации и распространенности патологического процесса.
Общими для большинства форм туберкулеза являются специфические изменения в сочетании с неспецифическими или параспе-цифическими реакциями. К специфическим изменениям относится туберкулезное воспаление, течение которого сопровождается формированием туберкулезного бугорка, или гранулемы, и более крупного очага. Неспецифическими изменениями являются различные реакции, обусловливающие так называемые маски туберкулеза.
Морфология туберкулезного воспаления зависит от реактивности организма и вирулентности возбудителя. В туберкулезном очаге могут преобладать явления экссудации, некроза или пролиферации, и очаг в соответствии с этим может быть преимущественно экссу-дативным, некротическим или продуктивным. В развитии туберкулезного воспаления большая роль принадлежит иммунологическим процессам. В участке воспаления сначала развивается реакция, не имеющая признаков, типичных для туберкулеза. В ней в разной степени выражены явления альтерации и экссудации. На первое место выступают нарушения в микроциркуляторном русле. Они затрагивают тонкую структуру стенки альвеолы, и механизмы их развития можно проследить на ультраструктурном уровне [Ерохин В. В., 1987]. На ранних стадиях воспаления изменения в субмикроскопической организации составных элементов стенки альвеолы связаны с повышением капиллярной проницаемости, развитием внутриклеточного интерстициального и внутриальвеолярного отека с вымыванием отечной жидкостью альвеолярного сурфактанта.
В дальнейшем дистрофические изменения в альвеолярной ткани нарастают, однако наряду с ними возникают и компенсаторно-восстановительные процессы, направленные на развитие внутриклеточной организации, повышение функциональной активности сохраняющихся клеток межальвеолярной перегородки. В следующей фазе воспаления — пролиферативной — появляются специфические для туберкулеза элементы (эпителиоидные и гигантские клетки Пиро-гова—Лангханса), формируются участки своеобразного гомогенного казеозного (творожистого) некроза в центре туберкулезного очага (рис. 1.3). На основании данных электронной микроскопии и авторадиографии о динамике клеточной трансформации установлена генетическая связь клеток гранулемы по линии моноцит — гигантская клетка [Серов В. В., Шехтер А. Б., 1981; Ерохин В. В., 1978, 1987; Danneberg А. М., 1982; SpectorW. G., 1982]. Макрофаги активно синтезируют и накапливают лизосомные ферменты, выполняют фагоцитарную функцию. Поглощенный материал, среди которого находятся и микобактерии туберкулеза, находится и переваривается в фагосомах и фаголизосомах. Эпителиоидные клетки 
образуются из мононуклеаров и макрофагов, скапливающихся в очаге туберкулезного воспаления в первые фазы воспалительной реакции. Они имеют крупное ядро овальной формы, обычно с 1—2 ядрышками Цитоплазма этих клеток содержит митохондрии, гранулы, аппарат Гольджи, хорошо развитую систему канальцев и цистерны зернистой и незернистой цитоплазматической сети, единичные фагосомы небольших размеров. Число митохондрий, элементов ретикулума, лизосомных включений широко варьирует и определяется функциональным состоянием клетки.
Гигантские клетки Пирогова—Лангханса могут образовываться из эпителиоидных клеток или макрофагов при их пролиферации, а также в результате слияния эпителиоидных клеток. Цитоплазма гигантских клеток содержит большое число ядер, обычно располагающихся в виде кольца или подковы по периферии клеток, множество митохондрий, лизосом, элементов зернистой цитоплазматической сети, хорошо развитый комплекс Гольджи. Гигантские клетки способны к фагоцитозу, в их цитоплазме обнаруживаются различные остаточные включения Они характеризуются высокой активностью гидролитических и дыхательных ферментов.
Помимо эпителиоидных и гигантских клеток, туберкулезная грануляционная ткань обычно содержит значительное число лимфоид-ных и плазматических клеток, а также нейтрофильный лейкоцитов. В периферических отделах грануляционного слоя выявляются фибробласты. Вокруг очага воспаления нередко имеется перифокальная зона неспецифической воспалительной реакции. При прогрессиро-вании процесса наблюдаются увеличение казеозного некроза, усиление инфильтрации грануляционной ткани мононуклеарами и лим-фоидными клетками, а также нейтрофилами, расширение зоны пе-рифокального воспаления. Специфический процесс распространяется контактным и лимфатическим путем.
При заживлении туберкулезного очага массы казеозного некроза уплотняются, в последних отмечается отложение мелких зерен солей кальция. В грануляционной ткани увеличивается количество фиб-робластов и фибрилл коллагена, объединяющихся в коллагеновые волокна, которые вокруг туберкулезного очага формируют соединительнотканную капсулу. В последующем специфическая грануляционная ткань все больше замещается фиброзной тканью. Число клеточных элементов между коллагеновыми волокнами уменьшается, иногда коллагеновые волокна подвергаются гиалинозу. В подобных очагах и посттуберкулезных очагах обнаружены измененные формы микобактерии туберкулеза, в частности L-формы, что позволяет лучше понять роль старых туберкулезных очагов в патогенезе вторичных форм туберкулеза [Пузик В. И., Земскова 3. С, Дорожкова И. Р., 1981, 1984]. В основе реактивации туберкулеза и формирования различных форм вторичного туберкулеза легких лежат реверсия и размножение бактериальной популяции на фоне развития недостаточности специфической и неспецифической защиты микроорганизма.
Дата добавления: 2015-04-25; просмотров: 2668;
