Адиабатный процесс
Условие, которым определяется адиабатный процесс: q = 0.
Процесс, происходящий без теплообмена с окружающей средой называется адиабатным.
Условие отсутствия подвода и отвода теплоты к системе называется условием адиабатности процесса.
На практике к адиабатным процессам приближаются такие процессы, в которых теплообменом между рассматриваемой системой и окружающей средой можно пренебречь.
Пренебречь теплообменом системы с окружающей средой можно в двух основных случаях: во-первых, если создать вокруг системы эффективную теплоизоляцию; во-вторых, если термодинамический процесс протекает достаточно быстро, в результате чего система за время процесса не успевает не получить из окружающей среды, ни передать ей сколько-нибудь значительное количество теплоты по сравнению с работой, совершаемой в данном процессе.
Исходная система уравнений (14.6) для адиабатного процесса с дополнительным условием имеет вид:
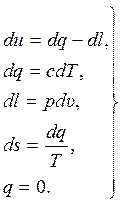 (15.27)
(15.27)
Первое и третье уравнения и последнее условие, с учётом свойства идеального газа (10.16), позволяют записать:
du + dl = cυ dT + p dυ = 0. (15.28)
Подставляя в (15.28) давление р, выраженное из уравнения состояния идеального газа, получаем:
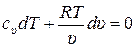 . (15.29)
. (15.29)
Преобразуем (15.29) к виду:
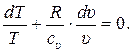 (15.30)
(15.30)
После интегрирования (15.30) получаем:
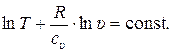 (15.31)
(15.31)
Воспользовавшись уравнением Майера (10.18) преобразуем отношение 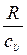 к виду:
к виду:
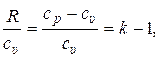 (15.32)
(15.32)
где 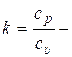 называется показателем адиабаты (безразмерная величина).
называется показателем адиабаты (безразмерная величина).
С учетом (15.32) преобразуем (15.31) к виду:
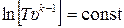 . (15.33)
. (15.33)
Очевидно, что из (15.33) следует:
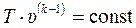 . (15.34)
. (15.34)
Преобразуем (15.34) следующим образом, учитывая уравнение идеального газа:
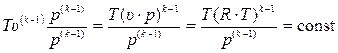 ,
,
или
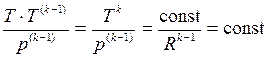 . (15.35)
. (15.35)
Выражение (15.35) возводим в степень 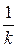 . В результате получаем:
. В результате получаем:
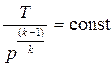 . (15.36)
. (15.36)
Выразим Т из уравнения состояния идеального газа и подставим в (15.34):
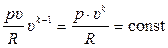
или
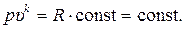 (15.37)
(15.37)
Выражения (15.34), (15.36) и (15.37) показывают, как параметры состояния идеального газа (газовой смеси) связаны между собой во время адиабатного процесса. (Вспомним, что для изотермического процесса аналогичная связь имеет вид: р υ = const). В частности, выражение (15.37) справедливо как для начального, так и конечного состояния системы в точках 1 и 2:
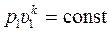 и
и 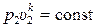 ,
,
отсюда следует, что
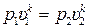 . (15.38)
. (15.38)
Аналогичным образом из (15.34) и (15.36) получаем:
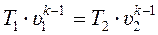 или
или 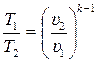 , (15.34)
, (15.34)
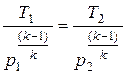 или
или 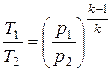 . (15.40)
. (15.40)
Уравнение (15.37) называется уравнением адиабаты, которое говорит о том, что в ходе адиабатного процесса произведение давления на удельный объём в степени k остаётся постоянным.
Из уравнения адиабаты (15.37) следует, что в р υ-координатах адиабатный процесс отображается степенной функцией вида 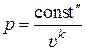 :
:
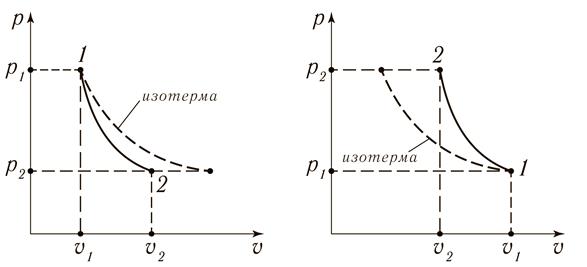
а) б)
Рис. 15.7. Адиабатный процесс 1 – 2 в рυ – координатах:
а) расширение газа; б) сжатие газа
На рис. 15.7 пунктирной линией изображена изотерма (равнобокая гипербола). Очевидно, что график адиабаты круче графика изотермы.
В результате интегрирования (15.28) получаем:
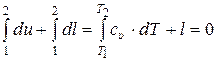 ,
,
или, с учётом (15.32):
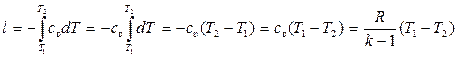 . (15.41)
. (15.41)
Формулу (15.41), используя уравнение идеального газа, можно преобразовать к виду:
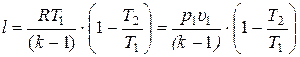 , (15.42)
, (15.42)
или
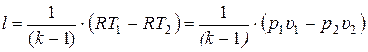 . (15.43)
. (15.43)
Выводы:
1) Из (15.41) следует, что в адиабатном процессе работа совершается только за счёт уменьшения внутренней энергии.
2) Из последнего условия q = 0 следует, что dq = 0, а значит 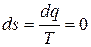 . Это означает, что s = const, т.е. в адиабатном процессе энтропия не изменяется.
. Это означает, что s = const, т.е. в адиабатном процессе энтропия не изменяется.
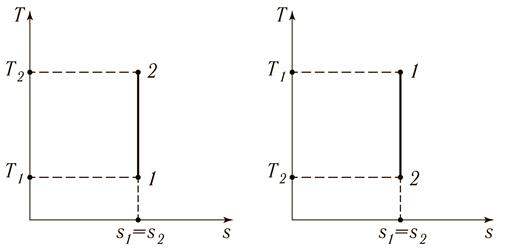
Рис. 15.8. Адиабатный процесс в Ts-координатах
Дата добавления: 2015-03-19; просмотров: 1197;
