Определите степень гидролиза (для первой ступени) и рН в 0,001М растворе и . Напишите уравнения реакций в молекулярном и ионном виде. 4 страница
III. Приложение
Таблица 1. Термодинамические константы некоторых веществ
| Вещество | 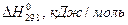
| 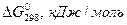
| 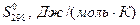
|
| Al (к) | 28,31 | ||
| Al2O3 (к) | – 1675,0 | – 1576,4 | 50,94 |
| BaCO3 (к) | – 1202,0 | – 1138,8 | 112,1 |
| BeCO3 (к) | – 981,57 | – 944,75 | 199,4 |
| C (алмаз) | 1,897 | 2,866 | 2,38 |
| С (графит) | 5,74 | ||
| CO (г) | – 110,5 | – 137,27 | 197,4 |
| CO2 (г) | – 393,51 | – 394,38 | 213,6 |
| COCl2 (г) | – 223,0 | –210,5 | 289,2 |
| CS2 (г) | – 115,3 | 65,1 | 237,8 |
| CS2 (ж) | – 87,8 | 63,6 | 151,0 |
| C2H2 (г) | 226,75 | 209,2 | 200,8 |
| C2H4 (г) | 52,28 | 68,12 | 219,4 |
| CH4 (г) | – 74,85 | – 50,79 | 186,19 |
| C2H6 (г) | – 84,67 | – 32,89 | 229,5 |
| C6H6 (ж) | 49,04 | 124,50 | 173,2 |
| CH3 OH (ж) | – 238,7 | – 166,31 | 126,7 |
| C2H5 OH (ж) | – 227,6 | – 174,77 | 160,7 |
| Ca (к) | 41,62 | ||
| CaО (к) | – 635,1 | – 604,2 | 39,7 |
| Ca(OH)2 (к) | – 986,2 | – 896,76 | 83,4 |
| CaCО3 (к) | – 1206,0 | – 1128,8 | 92,9 |
| Cl2 (г) | 223,0 | ||
| HCl (г) | – 92,30 | – 95,27 | 186,7 |
| HCl (ж) | – 167,5 | – 131,2 | 55,2 |
| Cu (к) | 33,3 | ||
| Cu2O (к) | – 167,36 | – 146,36 | 93,93 |
| CuO (к) | – 165,3 | – 127,19 | 42,64 |
| Cu2S (к) | – 82,01 | – 86,19 | 119,24 |
| Fe (к) | 27,15 | ||
| FeO (к) | – 263,68 | – 244,35 | 58,79 |
| FeCl2 (к) | – 341,0 | – 302,08 | 119,66 |
| Fe2O3 (к) | – 821,32 | 740,99 | 89,96 |
| Fe3O4 (к) | – 1117,1 | – 1015,5 | 146,2 |
| Ge (к) | 31,09 | ||
| GeO (к) | – 305,4 | – 276,1 | 50,2 |
| GeO2 (к) | – 539,74 | – 531,4 | 52,30 |
| H2 (г) | 130,6 | ||
| H2O (г) | – 241,84 | – 228,8 | 188,74 |
| H2O (ж) | 285,84 | – 237,5 | 69,96 |
| N2 (г) | 191,5 | ||
| N2 О (г) | 81,55 | 103,6 | 220,0 |
| NО (г) | 90,37 | 86,69 | 210,62 |
| NО2 (г) | 33,89 | 51,84 | 240,45 |
| NН3 (г) | – 46,19 | – 16,64 | 192,5 |
| NН4Cl (к) | – 315,39 | – 343,64 | 94,56 |
| NН4OH (ж) | – 366,69 | – 263,8 | 179,9 |
| NaOH (к) | – 426,6 | – 377,0 | 64,18 |
| NaCl (к) | – 410,9 | – 384,0 | 72,36 |
| O2 (г) | 205,03 | ||
| Pb (к) | 64,9 | ||
| PbO (к) | – 217,86 | – 188,49 | 67,4 |
| PbO2 (к) | – 276,6 | – 218,99 | 76,44 |
| SO2 (г) | – 296,9 | – 300,37 | 248,1 |
| H2S (г) | – 20,15 | – 33,02 | 205,64 |
| H2S (ж) | – 39,33 | – 27,36 | 122,2 |
| Sn (к) | 51,55 | ||
| SnO (к) | – 286,0 | – 257,32 | 56,74 |
| SnO2 (к) | – 580,8 | – 519,65 | 52,34 |
| Ti (к) | 30,6 | ||
| TiO2 (к) | – 938,6 | – 852,2 | 49,92 |
Таблица 2. Константы диссоциации некоторых слабых электролитов
в водных растворах, 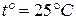
| Электролит | Кд | 
| |
| HNO2 | 4.0·10 – 4 | 3.40 | |
| NH4OH | 1.8·10 – 5 | 4.75 | |
| H2SiO3 | K1 | 2.2·10 – 10 | 9.66 |
| K2 | 1.6·10 – 12 | 11.80 | |
| H2SO4 | K2 | 1.2·10 – 2 | 1.92 |
| H2SO3 | K1 | 1.6·10 – 2 | 1.80 |
| K2 | 6.3·10 – 8 | 7.21 | |
| H2S | K1 | 6.0·10 – 8 | 7.22 |
| K2 | 1.0·10 – 14 | 14.0 | |
| H2CO3 | K1 | 4.5·10 – 7 | 6.35 |
| K2 | 4.7·10 – 11 | 10.33 | |
| CH3COOH | 1.8·10 – 5 | 4.75 | |
| H3PO4 | K1 | 7.5·10 – 3 | 2.12 |
| K2 | 6.3·10 – 8 | 7.20 | |
| K3 | 1.3·10 – 12 | 11.89 | |
| HF | 6.6·10 – 4 | 3.18 | |
| HCN | 7.9·10 – 10 | 9.10 |
Таблица 3. Степень диссоциации кислот, щелочей и солей
в водных растворах, 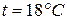 .
.
| Электролит и его ионы | α % | |
| 1Н | 0,1Н | |
| Кислоты | ||
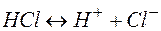
| ||
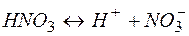
| ||
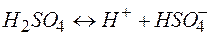
| ||
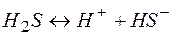
| - | 0,07 |
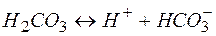
| - | 0,17 |
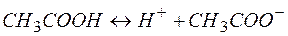
| 0,4 | 1,3 |

| ||

| - | |
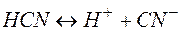
| - | 0,01 |
| Основания | ||
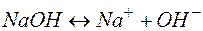
| ||

| ||
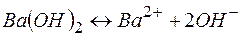
| - | |

| 0,4 | 1,3 |
| Соли | ||

| ||

| ||
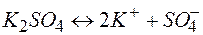
| ||

|
Таблица 4.Стандартные восстановительные потенциалы,  при
при 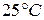 .
.
| Процесс |  , В , В
| |
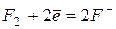
| +2,87 | |

| +1,51 | |

| +1,50 | |

| +1,36 | |
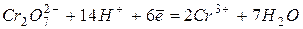
| +1,33 | |
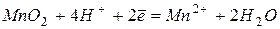
| +1,23 | |
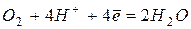
| +1,23 | |

| +1,07 | |
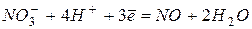
| +0,96 | |
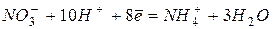
| +0,87 | |
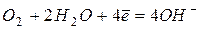
| +0,815 | |
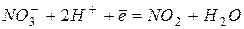
| +0,80 | |
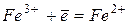
| +0,77 | |

| +0,63 | |

| +0,60 | |

| +0,56 | |

| +0,54 | |
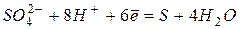
| +0,36 | |
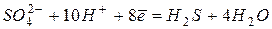
| +0,31 | |
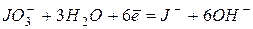
| +0,26 | |

| +0,17 | |

| 0,000 | |
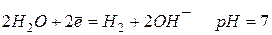 (pH=9) (pH=9)
| -0,413 (-0,53) | |
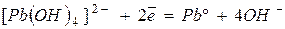
| -0,54 | |

| -0,83 | |

| -0,86 | |
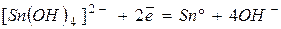
| -0,91 | |
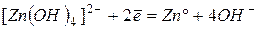
| -1,22 | |

| -2,35 | |

| -2,55 |
Таблица 4. Ряд напряжений металлов.
Нормальные (стандартные) электродные потенциалы, Е°(В) при 25°С.
| Электрод | Электродный процесс | Е° | ||

| ← окислительная активность иона возрастает ← | 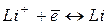
| → восстановительная активность атома возрастает → | -3,02 |
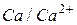
| 
| -2,84 | ||
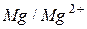
| 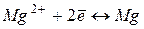
| -2,38 | ||

| 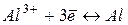
| -1,66 | ||

| 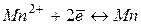
| -1,05 | ||

| 
| -0,76 | ||
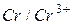
| 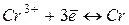
| -0,74 | ||
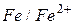
| 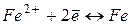
| -0,44 | ||
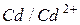
| 
| -0,40 | ||

| 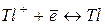
| -0,33 | ||

| 
| -0,27 | ||
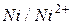
| 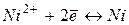
| -0,23 | ||
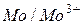
| 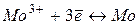
| -0,20 | ||
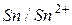
| 
| -0,14 | ||
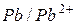
| 
| -0,13 | ||
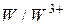
| 
| -0,05 | ||
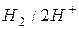
| 
| ±0,00 | ||
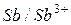
| 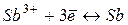
| +0,20 | ||

| 
| +0,23 | ||

| 
| +0,34 | ||
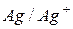
| 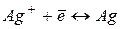
| +0,80 | ||

| 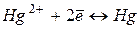
| +0,85 | ||
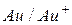
| 
| +1,50 |
Таблица 5. Константы устойчивости некоторых комплексов
| Аммиакаты и др. | Гидроксокомплексы | ||
| Комплекс | lgβn | Комплекс | lgβn |
| Ag(NH3)2 + | 7,24 | Al(OH)4– | 33,00 |
| Cd(NH3)4 2+ | 6,56 | Be(OH)3– | 15,00 |
| Cd(NH3)6 2+ | 5,13 | Cr(OH)4– | 30,00 |
| Co(NH3)6 2+ | 5,13 | Cu(OH)4– | 18,50 |
| Co(NH3)6 3+ | 32,51 | Fe(OH)4– | 38,00 |
| Cu(NH3)4 2+ | 12,67 | Sn(OH)4– | 25,13 |
| Fe(NH3)2 2+ | 2,20 | Zn(OH)4– | 14,66 |
| Ni(NH3)4 2+ | 7,95 | Цианиды | |
| Ni(NH3)6 2+ | 8,73 | Ag(CN)2– | 21,00 |
| Zn(NH3)6 2+ | 9,46 | Co(CN)64– | 19,00 |
| Cu(NH3)2+ | 10,87 | Co(CN)63– | 64,00 |
| HI4 2– | 30,20 | Cu(CN)62– | 30,30 |
| Fe(SCN)6 3– | 25,00 | Fe(CN)64– | 35,00 |
| Ag(S2O3)3 5– | 13,50 | Fe(CN)63– | 42,00 |
Таблица 6. Растворимость солей, кислот и оснований в воде
 Катионы
Анионы Катионы
Анионы
| H+ |

| K+ | Na+ | Ag+ | Hg+ | Hg2+ | Ba2+ | Ca2+ | Mg2+ | Zn2+ | Mn2+ | Sn2+ | Pb2+ | Cu2+ | Fe2+ | Al3+ | Cr3+ | Bi3+ |
| OH- | Р | Р | Р | - | - | - | Р | М | М | Н | Н | Н | М | Н | Н | Н | Н | Н | |
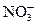
| Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | - | Р | Р | Р | Р | Р | Р |
| F- | Р | Р | Р | Р | Р | Н | М | М | Н | Н | М | М | Р | Н | Н | М | Р | Р | Н |
| Cl- | Р | Р | Р | Р | Н | Н | Р | Р | Р | Р | Р | Р | - | М | Р | Р | Р | Р | - |
| Br- | Р | Р | Р | Р | Н | Н | Р | Р | Р | Р | Р | Р | Р | М | Р | Р | Р | Р | - |
| I- | Р | Р | Р | Р | Н | Н | Н | Р | Р | Р | Р | Р | М | Н | - | Р | Р | Р | - |
| S2- | Р | Р | Р | Р | Н | Н | Н | Р | М | Р | Н | Н | Н | Н | Н | Н | - | - | Н |

| Р | Р | Р | Р | Н | Н | Н | М | М | Н | М | Н | - | Н | Н | М | - | - | Н |
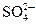
| Р | Р | Р | Р | М | М | Р | Н | М | Р | Р | Р | Р | М | Р | Р | Р | Р | Р |

| Р | Р | Р | Р | Н | Н | Н | Н | М | М | Н | Н | - | Н | Н | Н | - | - | Н |

| Н | - | Р | Р | Н | - | - | Н | Н | Н | Н | Н | Н | Н | - | Н | - | - | - |

| Р | Р | Р | Р | Н | Н | Н | Н | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | Н |
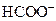
| Р | Р | Р | Р | Р | М | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р |

| Р | Р | Р | Р | Р | М | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | М | Р | Р |
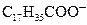
| Н | Р | Р | Р | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
Р-растворимые М -малорастворимые Н -нерастворимые
Дата добавления: 2014-12-05; просмотров: 1504;
