Определите степень гидролиза (для первой ступени) и рН в 0,001М растворе и . Напишите уравнения реакций в молекулярном и ионном виде. 2 страница
в) 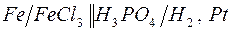 .
.
177. Цепи, записанные в ионной форме, представьте в молекулярной форме:
а) 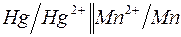 ; ;
| в) 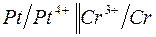 ; ;
|
б) 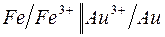 ; ;
| г) 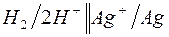 . .
|
178. Составьте химические цепи следующих компонентов:
а) 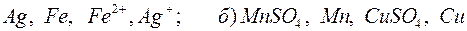 .
.
179. Гальванический элемент содержит взаимодействующие между собой компоненты 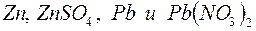 . Укажите состав электрода-окислителя и электрода-восстановителя.
. Укажите состав электрода-окислителя и электрода-восстановителя.
180. Имеются гальванические цепи:
а) 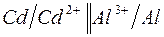 ; ;
| в) 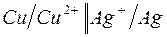 ; ;
|
б) 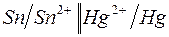 ; ;
| г) 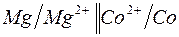 . .
|
Для каждой из этих цепей укажите:
1) окислитель (акцептор электронов) и восстановитель (донор электронов);
2) электрод-окислитель и электрод-восстановитель;
3) положительный и отрицательный полюсы гальванического элемента;
4) направление потока электронов по внешней цепи.
181. Составьте схемы (в ионной форме) двух гальванических цепей, в одной из которых никель являлся бы отрицательным электродом, а в другом – положительным.
182. Приведите примеры записей в молекулярной форме двух гальванических элементов, в одном из которых медь играла бы роль положительного полюса, а в другом – отрицательного.
183. Цепи для определения электродных потенциалов металлов имеют вид:
а) 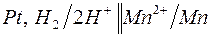 ; ;
| в) 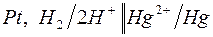 ; ;
|
б) 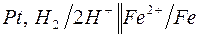 ; ;
| г) 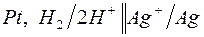 . .
|
Для каждой из перечисленных цепей:
1) укажите, какую роль (окислителя или восстановителя) и в какой форме (Н2 или Н+) играет водород;
2) обозначьте знаки полюсов и направление перемещения электронов по внешнему металлическому проводнику;
3) запишите электронно-ионные уравнения электродных реакций. Как сдвигается равновесие 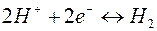 в каждом отдельном случае.
в каждом отдельном случае.
184. Запишите в ионной форме гальванические цепи для определения электродных потенциалов металлов по водородному электроду: а) цинка; б) кобальта; в) меди и г) алюминия. Для каждой из этих цепей укажите положительный и отрицательный полюсы, а также направление потока электронов по металлическому проводнику, образующему внешнюю цепь гальванического элемента.
185. Гальванический элемент составлен из железных и медных нормальных электродов. Запишите схему элемента (цепь) в ионной форме. Укажите электрод-окислитель и электрод-восстановитель. Обозначьте знаки полюсов и направление потока электронов во внешней цепи.
186. Как должна быть составлена гальваническая цепь для того, чтобы осуществить электрохимическим путём следующие реакции:
а) 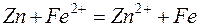 ;
б) ;
б) 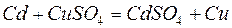 ; ;
| г) 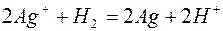 ;
д) ;
д) 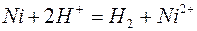 . .
|
в) 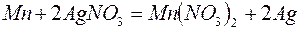 ; ;
|
Для каждого случая укажите: а) электрод – восстановитель и электрод – окислитель; б) знаки полюсов и в) направление перемещения электронов по внешней цепи.
187. Напишите уравнения реакций, соответствующих следующим гальваническим цепям, и укажите окислители и восстановители:
а) 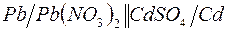 ;
б) ;
б) 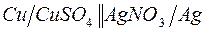 ;
в) ;
в) 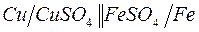 ; ;
| г) 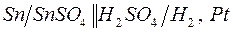 ;
д) ;
д) 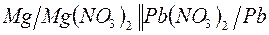 . .
|
188. Укажите направление электрического тока (т.е. направление перемещения положительных зарядов) во внешней и внутренней цепях следующих гальванических элементов:
а) 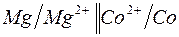 ; ;
| г) 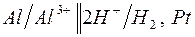 ; ;
|
б) 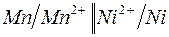 ; ;
| д) 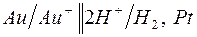 . .
|
в) 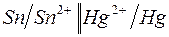 ; ;
|
189. При работе гальванического элемента 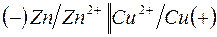 цинковый электрод вследствие окисления металла по уравнению
цинковый электрод вследствие окисления металла по уравнению 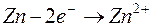 потерял в массе 10 мг
потерял в массе 10 мг 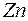 . Вычислите, какое количество электричества в кулонах протекло при этом по внешней цепи гальванического элемента.
. Вычислите, какое количество электричества в кулонах протекло при этом по внешней цепи гальванического элемента.
190. На положительном электроде гальванического элемента
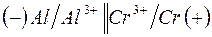 за 40 сек его работы отложилось 20,8 мг хрома. Определите, на сколько миллиграммов уменьшилась при этом масса алюминиевого электрода. Вычислите силу тока в амперах.
за 40 сек его работы отложилось 20,8 мг хрома. Определите, на сколько миллиграммов уменьшилась при этом масса алюминиевого электрода. Вычислите силу тока в амперах.
191. Гальванический элемент 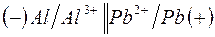 даёт ток силой 4 а. Сколько алюминия окислится и сколько восстановится за 15 сек работы элемента (в мг)?
даёт ток силой 4 а. Сколько алюминия окислится и сколько восстановится за 15 сек работы элемента (в мг)?
192. Отметьте электродные потенциалы, укажите знаки полюсов и вычислите ЭДС химических цепей, составленных из стандартных электродов:
а) 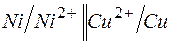 ; ;
| г) 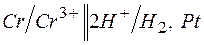 ; ;
|
б) 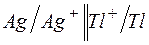 ; ;
| д) 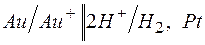 . .
|
в) 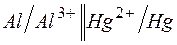 ; ;
|
193. Вычислите ЭДС следующих гальванических цепей:
а) 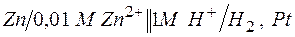 ;
;
б) 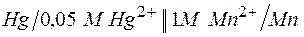 ;
;
в) 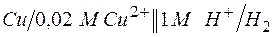 ;
;
г) 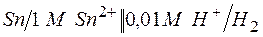 .
.
194. Вычислите ЭДС следующих гальванических цепей:
а) 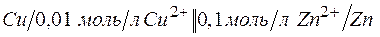 ;
;
б) 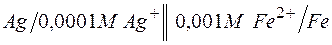 ;
;
в) 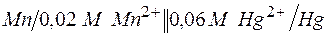 .
.
195. Вычислите ЭДС следующих гальванических цепей:
а) 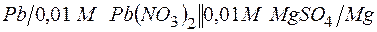 ;
;
б) 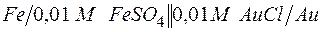 ;
;
в) 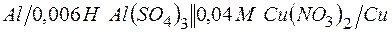 ;
;
г) 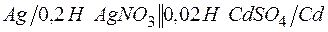 .
.
196. Вычислите ЭДС следующих гальванических цепей:
а) 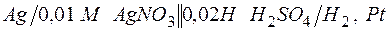 ;
;
б) 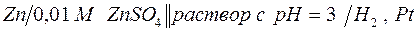 ;
;
в) 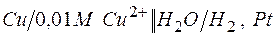 ;
;
г) 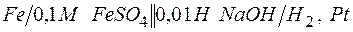 .
.
197. Гальваническая цепь составлена из нормального водородного электрода и свинцового электрода, погружённого в насыщенный раствор сульфата свинца. 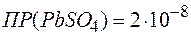 . Найдите величину электродного потенциала
. Найдите величину электродного потенциала 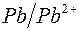 . Запишите цепь, укажите знаки полюсов, а также отметьте направление потока электронов. Вычислите ЭДС цепи.
. Запишите цепь, укажите знаки полюсов, а также отметьте направление потока электронов. Вычислите ЭДС цепи.
198. Укажите знаки полюсов, направление потока электронов и ЭДС следующей цепи ( 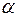 - степень диссоциации):
- степень диссоциации):
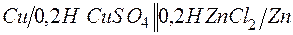
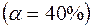
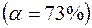
199. ЭДС цепи: 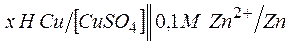 равна 1,04 В. Определите концентрацию катионов меди (в моль/л) и нормальность раствора
равна 1,04 В. Определите концентрацию катионов меди (в моль/л) и нормальность раствора 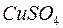 , обозначенную через х.
, обозначенную через х.
200. ЭДС цепи 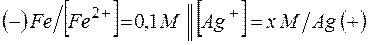 равна 1,152 В. Вычислите х.
равна 1,152 В. Вычислите х.
201. Имеется гальваническая цепь 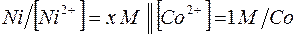 . Чему должен равняться х для того, чтобы электродный потенциал никеля стал равным нормальному электродному потенциалу кобальта?
. Чему должен равняться х для того, чтобы электродный потенциал никеля стал равным нормальному электродному потенциалу кобальта?
202. Имеется гальваническая цепь 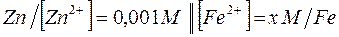 . Какой концентрации надо было взять катионы железа (в моль/л) для того, чтобы ЭДС цепи стала равной нулю?
. Какой концентрации надо было взять катионы железа (в моль/л) для того, чтобы ЭДС цепи стала равной нулю?
203. Определите величину электродных потенциалов:
а) 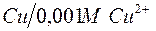 ; ; 
| в) 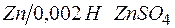 ; ;
|
б) 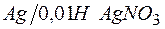 ; ;
| г) 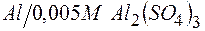 . .
|
204. Электролиз раствора K2SO4 проводили при силе тока 5А в течение 3 ч. Составьте электронные уравнения процессов, происходящих на электродах. Какая масса воды при этом разложилась и чему равен объем газов (н.у.), выделившихся на катоде и аноде?
205. При электролизе соли некоторого металла в течение 1,5 ч при силе тока 1,8А на катоде выделилось 1,75 г этого металла. Вычислите эквивалентную массу металла.
206. При электролизе раствора CuSO4 на аноде выделилось 168 см3 газа (н.у.). Составьте электронные уравнения процессов, происходящих на электродах, и вычислите, какая масса меди выделилась на катоде.
207. Электролиз раствора Na2SO4 проводили в течение 5 ч при силе тока 7А. Составьте электронные уравнения процессов, происходящих на электродах. Какая масса воды при этом разложилась и чему равен объем газов (н.у.), выделившихся на катоде и аноде?
208. Электролиз раствора нитрата серебра проводили при силе тока 2А в течение 4 ч. Составьте электронные уравнения процессов, происходящих на электродах. Какая масса серебра выделилась на катоде и каков объем газа (н.у.), выделившегося на аноде?
209. Электролиз раствора сульфата некоторого металла проводили при силе тока 6А в течение 45 мин, в результате чего на катоде выделилось 5,49 г металла. Вычислите эквивалентную массу металла.
210. На сколько уменьшится масса серебряного анода, если электролиз раствора AgNO3 проводить при силе тока 2 А в течение 38 мин 20 с? Составьте электронные уравнения процессов, происходящих на графитовых электродах.
211. Электролиз раствора сульфата цинка проводили в течение 5 ч, в результате чего выделилось 6 л кислорода (н.у.). Составьте уравнения электродных процессов и вычислите силу тока.
212. Электролиз раствора CuSO4 проводили с медным анодом в течение 4 ч при силе тока 50 А. При этом выделилось 224 г меди. Вычислите выход по току (отношение массы выделившегося вещества к теоретически возможной). Составьте электронные уравнения процессов, происходящих на электродах в случае медного и угольного анодов.
213. Электролиз раствора NaI проводили при силе тока 6 А в течение 2,5 ч. Составьте электронные уравнения процессов, происходящих на угольных электродах, и вычислите массу вещества, выделившегося на катоде и аноде?
214. Составьте электронные уравнения процессов, происходящих на угольных электродах при электролизе раствора AgNO3. Если электролиз проводить с серебряным анодом, то его масса уменьшается на 5,4 г. Определите расход электричества при этом.
215. Электролиз раствора CuSO4 проводится в течение 15 минут при силе тока 2,5 А. Выделилось 0,72 г меди. Составьте электронные уравнения процессов, происходящих на электродах в случае медного и угольного анодов. Вычислите выход по току (отношение массы выделившегося вещества к теоретически возможной).
216. Составьте электронные уравнения процессов, происходящих на графитовых электродах при электролизе расплавов и водных растворов NaCl и KOH. Сколько литров (н.у.) газа выделится на аноде при электролизе гидроксида калия, если электролиз проводить в течение 30 мин при силе тока 0,5 А?
217. Составьте электронные уравнения процессов, происходящих на графитовых электродах при электролизе раствора KBr. Какая масса вещества выделяется на катоде и аноде, если электролиз проводить в течение 1 ч 35 мин при силе тока 15 А?
218. Составьте электронные уравнения процессов, происходящих на угольных электродах при электролизе раствора CuCl2. Вычислите массу меди, выделившейся на катоде, если на аноде выделилось 560 мл газа (н.у.).
219. При электролизе соли трехвалентного металла при силе тока 1,5 А в течение 30 мин на катоде выделилось 1,071 г металла. Вычислите атомную массу металла.
220. При электролизе растворов MgSO4 и ZnCl2, соединенных последовательно с источником тока, на одном из катодов выделилось 0,25 г водорода. Какая масса вещества выделится на другом катоде; на анодах?
221. Составьте электронные уравнения процессов, происходящих на угольных электродах при электролизе раствора Na2SO4. Вычислите массу вещества, выделяющегося на катоде, если на аноде выделяется 1,12 л газа (н.у.). Какая масса H2SO4 образуется при этом возле анода?
222. При электролизе раствора соли кадмия израсходовано 3434 Кл электричества. Выделилось 2 г кадмия. Чему равна молярная масса эквивалента кадмия?
223. Составьте электронные уравнения процессов, происходящих на электродах при электролизе раствора КОН. Чему равна сила тока, если в течение 1 ч 15 мин 20 с на аноде выделилось 6,4 г газа? Сколько литров газа (н.у.) выделилось при этом на катоде?
224. Как происходит атмосферная коррозия луженого и оцинкованного железа при нарушении покрытия? Составьте электронные уравнения анодного и катодного процесса.
225. Медь не вытесняет водород из разбавленных кислот. Почему? Однако, если к медной пластинке, опущенной в кислоту, прикоснуться цинковой, то на меди начинается бурное выделение водорода. Дайте этому объяснение, составив электронные уравнения анодного и катодного процессов. Напишите уравнение протекающей химической реакции.
226. Как происходит атмосферная коррозия луженого железа и луженой меди при нарушении покрытия? Составьте электронные уравнения анодного и катодного процессов.
227. Если пластинку из чистого цинка опустить в разбавленную кислоту, то начавшееся выделение водорода вскоре почти прекращается. Однако при прикосновении к цинку медной палочкой на последней начинается бурное выделение водорода. Дайте этому объяснение, составив электронные уравнения анодного и катодного процессов. Напишите уравнения протекающей химической реакции.
228. В чем сущность протекторной защиты металлов от коррозии? Приведите пример протекторной зашиты железа в электролите, содержащем растворенный кислород. Составьте электронные уравнения анодного и катодного процессов.
229. Железное изделие покрыли никелем. Какое это покрытие – анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе и в хлороводородной (соляной) кислоте. Какие продукты коррозии образуются в первом и во втором случаях?
230. Составьте электронные уравнения анодного и катодного процессов с кислородной и водородной деполяризацией при коррозии пары магний – никель. Какие продукты коррозии образуются в первом и во втором случаях?
231. В раствор хлороводородной (соляной) кислоты поместили цинковую пластинку и цинковую пластинку, частично покрытую медью. В каком случае процесс коррозии цинка происходит интенсивнее? Ответ мотивируйте, составив электронные уравнения соответствующих процессов.
232. Почему химически чистое железо более стойко против коррозии, чем техническое железо? Составьте электронные уравнения анодного и катодного процессов, происходящих при коррозии технического железа во влажном воздухе и в кислой среде.
233. Какое покрытие металла называется анодным и какое – катодным? Назовите несколько металлов, которые могут служить для анодного и катодного покрытий железа. Составьте электронные уравнения анодного и катодного процессов, происходящих при коррозии железа, покрытого медью, во влажном воздухе и в кислой среде.
234. Железное изделие покрыли свинцом. Какое это покрытие – анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе и в хлороводородной (соляной) кислоте. Какие продукты коррозии образуются в первом и во втором случаях?
235. Две железные пластинки, частично покрытые одна оловом, другая медью, находятся во влажном воздухе. На какой из этих пластинок быстрее образуется ржавчина? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этих пластинок. Каков состав продуктов коррозии железа?
236. Какой металл целесообразней выбрать для протекторной защиты от коррозии свинцовой оболочки кабеля: цинк, магний или хром? Почему? Составьте электронные уравнения анодного и катодного процессов атмосферной коррозии. Каков состав продуктов коррозии?
237. Если опустить в разбавленную серную кислоту пластинку из чистого железа, то выделение на ней водорода идет медленно и со временем почти прекращается. Однако, если цинковой палочкой прикоснуться к железной пластинке, то на последней начинается бурное выделение водорода. Почему? Какой металл при этом растворяется? Составьте электронные уравнения анодного и катодного процессов.
238. Цинковую и железную пластинки опустили в раствор сульфата меди. Составьте электронные и ионно-молекулярные уравнения реакций, происходящих на каждой из этих пластинок. Какие процессы будут проходить на пластинках, если наружные концы их соединить проводником?
239. Как влияет рН среды на скорость коррозии железа и цинка? Почему? Составьте электронные уравнения анодного и катодного процессов атмосферной коррозии этих металлов.
240. В раствор электролита, содержащий растворенный кислород, опустили цинковую пластинку и цинковую пластинку, частично покрытую медью. В каком случае процесс коррозии цинка проходит интенсивнее? Составьте электронные уравнения анодного и катодного процессов.
241. Составьте электронные уравнения анодного и катодного процессов с кислородной и водородной деполяризацией при коррозии пары алюминий – железо. Какие продукты коррозии образуются в первом и во втором случаях?
242. Как протекает атмосферная коррозия железа, покрытого слоем никеля, если покрытие нарушено? Составьте электронные уравнения анодного и катодного процессов. Каков состав продуктов коррозии?
243. Установите термодинамическую вероятность протекания электрохимической коррозии при механическом повреждении сплошности катодного покрытия на стальном изделии во влажной атмосфере воздуха. Запишите схему коррозионной гальванопары, уравнения анодного и катодного процессов. Укажите вид и состав конечного продукта коррозии.
244. Гальванопара образуется на поверхности алюминиевого изделия с медными заклепками во влажной атмосфере воздуха. Установите термодинамическую вероятность протекания электрохимической коррозии. Запишите схему коррозионной гальванопары, уравнения анодного и катодного процессов. Укажите вид и состав конечного продукта коррозии.
245. Установите термодинамическую вероятность протекания электрохимической коррозии на поверхности стального изделия с цинковым протектором в нейтральной водной среде (морская вода) в присутствии растворенного кислорода. Запишите схему коррозионной гальванопары, уравнения анодного и катодного процессов. Укажите вид и состав конечного продукта коррозии. Можно ли использовать в качестве протектора в этом случае олово?
246. Установите термодинамическую вероятность протекания электрохимической коррозии при механическом повреждении сплошности анодного покрытия на стальном изделии во влажной атмосфере воздуха. Запишите схему коррозионной гальванопары, уравнения анодного и катодного процессов. Укажите вид и состав конечного продукта коррозии. Надежна ли защита при помощи анодного покрытия?
247. Установите термодинамическую вероятность протекания электрохимической коррозии при коррозии латуни (сплав цинка с медью) во влажной атмосфере воздуха. Запишите схему коррозионной гальванопары, уравнения анодного и катодного процессов. Укажите вид и состав конечного продукта коррозии. В какой среде латунные изделия обладают большей коррозионной устойчивостью: в кислой среде или во влажной атмосфере воздуха?
248. Установите термодинамическую вероятность протекания электрохимической коррозии на поверхности стального изделия с магниевым протектором в нейтральной водной среде, содержащей растворенные соли (NaCl, Na2SO4) в присутствии растворенного кислорода. Запишите схему коррозионной гальванопары, уравнения анодного и катодного процессов. Укажите вид и состав конечного продукта коррозии.
249. Установите термодинамическую вероятность протекания электрохимической коррозии при повреждении катодного покрытия на стальном изделии в растворе серной кислоты. Запишите схему коррозионной гальванопары, уравнения анодного и катодного процессов. Укажите вид и состав конечного продукта коррозии. Надежна ли защита при помощи катодных покрытий?
250. Установите термодинамическую вероятность протекания электрохимической коррозии при механическом повреждении анодного покрытия на стальном изделии во влажной атмосфере воздуха. Запишите схему коррозионной гальванопары, уравнения анодного и катодного процессов. Укажите вид и состав конечного продукта коррозии. Надежен ли такой способ защиты от коррозии?
251. Магниево-алюминиевый сплав эксплуатируется во влажной атмосфере воздуха. В какой среде (кислой или нейтральной) этот сплав будет обладать большей коррозионной устойчивостью? Ответ обоснуйте, запишите соответствующие уравнения катодного и анодного процессов, сделайте расчеты.
252. Медное изделие, паянное серебром, эксплуатируется а) в растворе соляной кислоты; б) во влажной атмосфере воздуха. Является ли коррозионный процесс в данных случаях термодинамически возможным? Ответ обоснуйте, запишите соответствующие уравнения катодного и анодного процессов, сделайте расчеты.
253. Пользуясь таблицей восстановительных потенциалов и рядом напряжений металлов, укажите, какие металлы являются термодинамически неустойчивыми в следующих эксплуатационных средах: кислая среда в присутствии растворенного кислорода; щелочная среда (рН=10) без кислорода; соляная кислота. Ответ поясните.
254. Пользуясь таблицей восстановительных потенциалов и рядом напряжений металлов, укажите, какие металлы являются термодинамически неустойчивыми в следующих эксплуатационных средах: пленка влаги; раствор щелочи; разбавленная серная кислота в присутствии перманганат-ионов. Ответ объясните.
255. Пользуясь таблицей восстановительных потенциалов и рядом напряжений металлов, а также, исходя из расчетов по уравнению Нернста, укажите, какие металлы являются термодинамически неустойчивыми в следующих эксплуатационных средах: щелочная среда (рН=10); 0,1Н раствор серной кислоты; щелочная пленка влаги.
256. Пользуясь таблицей восстановительных потенциалов и рядом напряжений металлов, а также, исходя из расчетов по уравнению Нернста, укажите, какие металлы являются термодинамически устойчивыми в следующих эксплуатационных средах: кислая пленка влага (рН=3); разбавленный раствор серной кислоты (0,1 М); раствор щелочи (pН=14).
257. Определите заряд комплексного иона, степень окисления и координационное число комплексообразователя в соединениях [Cu(NH3)4]SO4, K2[PtCl6], K[Ag(CN)2]. Назовите их. Напишите уравнения диссоциации этих соединений в водных растворах.
258. Составьте координационные формулы следующих комплексных соединений платины: PtCl4∙6NH3; PtCl4∙4NH3; PtCl4∙2NH3. Координационное число платины (IV) равно шести. Напишите уравнение диссоциации этих соединений в водных растворах. Какое из соединений является комплексным неэлектролитом?
259. Составьте координационные формулы следующих комплексных соединений кобальта: CoCl3∙6NH3; CoCl3∙5NH3; СoСl3∙4NH3. Координационное число кобальта (III) равно шести. Напишите уравнения диссоциации этих соединений в водных растворах.
260. Составьте координационные формулы следующих комплексных соединений серебра: AgCl∙2NH3; AgCN∙KCN; AgNO2∙NaNO2. Координационное число серебра равно двум. Напишите уравнения диссоциации этих соединений в водных растворах.
261. Определите заряд комплексного иона, степень окисления и координационное число комплексообразователя в соединениях K4[Fe(CN)6], K4[TiCl8], K2[HgI4]. Назовите их. Как диссоциируют эти соединения в водных растворах?
262. Из сочетания частиц Co3+, NH3, NO2– и K+ можно составить семь координационных формул комплексных соединений кобальта, одна из которых [Co(NH3)6](NO2)3. Составьте формулы других шести соединений и напишите уравнения их диссоциации в водных растворах.
263. Определите, чему равен заряд следующих комплексных ионов: [Cr(H2O)4Cl2], [HgBr4], [Fe(CN)6], если комплексообразователями являются Cr3+, Hg2+, Fe3+. Напишите формулы соединений, содержащих эти комплексные ионы. Назовите их.
264. Определите заряд следующих комплексных ионов: [Cr(NH3)5NO3], [Pt(NH3)Cl3], [Ni(CN)4], если комплексообразователями являются Cr3+, Pt2+, Ni2+. Напишите формулы комплексных соединений, содержащих эти ионы. Назовите их.
265. Из сочетания частиц Cr3+, H2O, Cl– и K– можно составить семь координационных формул комплексных соединений хрома, одна из которых [Cr(H2O)6]Cl3. Составьте формулы других шести соединений и напишите уравнения их диссоциации в водных растворах.
266. Составьте координационные формулы следующих комплексных соединений кобальта: 3NaNO2∙Co(NO2)3; CoCl3∙3NH3∙2H2O; 2KNO2∙NH3∙Co(NO2)6. Координационное число кобальта (III) равно шести. Напишите уравнения диссоциации этих соединений в водных растворах.
Дата добавления: 2014-12-05; просмотров: 3569;
