V. Центральная регуляция висцеральных функций.
Сложные механизмы регуляции деятельности висцеральных органов и представляют многоэтажную иерархическую структуру.
1. Базовый структурный уровень – внутриорганные рефлексы, замыкающиеся в интрамуральных ганглиях и имеющие метасимпатическую природу. Эти ганглии являются низшими рефлекторными центрами.
2. Экстрамуральные паравертебральные ганглиии брыжеечных и чревного сплетений. Оба этих низших этажа обладают отчетливо выраженной автономностью и могут осуществлять регуляцию деятельности висцеральных органов и тканей относительно независимо от центральной нервной системы.
3. Центры спинного мозга и ствола. В шейной и в начале грудной части располагаются тела преганглионарных симпатических нейронов, иннервирующие гладкие мышцы глазного яблока. Пять верхних грудных сегментов служат местом локализации симпатических нейронов, иннервирующих сердце и бронхи. На уровне всех грудных, а также верхних поясничных сегментов спинного мозга, т. е. на всем протяжении симпатического ядра, расположены нейроны, иннервирующие сосуды и потовые железы. Располагающиеся в стволе скопления парасимпатических нейронов образуют центры, в которых осуществляется замыкание рефлексов сосания, жевания, глотания, чиханья, слюноотделения, слезотечения, торможения сердечной деятельности, секреции желудочных желез и т. д. Крестцовые отделы спинного мозга занимают парасимпатические нейроны, которые образуют ряд центров рефлексов мочеиспускания, дефекации, эрекции и т. д.
4. Гипоталамус, ретикулярная формация, лимбическая система, мозжечок, новая кора.
В гипоталамусе принято различать три скопления ядер: переднее, среднее и заднее. При стимуляции гипоталамуса возникает комплекс сложных реакций, в которых нервный компонент дополняется гормональным. Так, раздражение ядер задней группы характеризуется эффектами, аналогичными раздражению симпатической части автономной нервной системы – расширяются зрачки и глазная щель, возрастает частота сердечных сокращений, повышается кровяное давление, тормозится двигательная активность пищеварительного тракта, в крови возрастает концентрация адреналина и норадреналина. Разрушение этой области приводит к гипергликемии, ожирению, нарушению терморегуляции.
Раздражение ядер передней группы сопровождается реакциями, подобными раздражению парасимпатической части автономной нервной системы, – сужением зрачков и глазных щелей, урежением частоты сердечных сокращений, снижением артериального давления, усилением двигательной активности желудочно-кишечного тракта. Ядра этой группы участвуют в механизме терморегуляции.
Функция ядер средних групп состоит преимущественно в регуляции метаболизма. Разрушение, например, вентромедиальных ядер сопровождается повышением потребления пищи (гиперфагия) и ожирением, двустороннее разрушение латеральных ядер, напротив, приводит к полному отказу от пищи.
Лимбическая система («висцеральный мозг») регулирует висцерально-гормональные функции, направленные на обеспечение различных форм деятельности, таких, как пищевое, сексуальное, оборонительное поведение, регулирует эмоциональную сферу, осуществляя, таким образом, сома-товисцеральную интеграцию.
Мозжечок, наряду с регуляцией двигательной соматической сферы мозжечок контролирует течение висцеральных процессов. После удаления мозжечка возникает угнетение периодической моторной деятельности пищеварительного тракта, секреторной функции кишечных желез и т. д.
Ретикулярная формация. Основной ролью ее нисходящей части по отношению к деятельности автономной нервной системы является повышение активности нервных центров, связанных с висцеральными функциями. Проводником этих влияний на периферию является симпатическая часть автономной нервной системы.
Кора большого мозга. У человека раздражение точек в теменных и других долях сопровождается изменением сердечной деятельности, артериального давления, дыхательного ритма, слюноотделения, желудочной и кишечной моторики. Высшими центрами автономной иннервации считаются передние отделы больших полушарий. Известно, что в определенных условиях у человека гипнотическим внушением (влияние через кору мозга) можно вызвать изменение сердечного ритма, вазоконстрикцию и вазодилатацию, изменение метаболизма.
Лекция 9. Гуморальная регуляция функций. Гипоталамо-гипофизарная система.
1. Факторы гормональной регуляции.
5.1. ПРИНЦИПЫ ГОРМОНАЛЬНОЙ РЕГУЛЯЦИИ
Все процессы жизнедеятельности организма строго согласованы между собой по скорости, времени и месту протекания. В организме человека эту согласованность осуществляют внутриклеточные и межклеточные механизмы регуляции, важнейшую роль в которых играют гормоны и нейромедиаторы. Специфические регуляторы, которые секретируются эндокринными железами в кровь или лимфу, а затем попадают на клетки-мишени, называют гормонами. Вещества, которые выделяются из пресинаптических нервных окончаний в синаптическую щель и вызывают биологический эффект, связываясь с рецепторами постсинаптической мембраны, называют нейромедиаторами.
Функциональная активность эндокринной железы может регулироваться «субстратом», на который направлено действие гормона. Так, глюкоза стимулирует секрецию инсулина из /?-клеток панкреатических островков (островки Лангерганса), а инсулин понижает концентрацию глюкозы в крови, активируя ее транспорт в мышцы и печень. Это происходит следующим образом. Глюкоза входит в /?-клетки поджелудочной железы через переносчик глюкозы и сразу же фосфорилируется глюкокиназой, после чего вовлекается в гликолиз. Образующийся при этом АТФ ингибирует калиевые каналы, вследствие чего снижается мембранный потенциал /?-клеток и активируются потенциалзависимые кальциевые каналы. Входящий в /?-клетку кальций стимулирует слияние везикул, содержащих инсулин, с плазматической мембраной и секрецию инсулина. Инсулин активирует перенос глюкозы в печень, сердце и скелетные мышцы, вследствие чего уровень глюкозы в крови снижается, замедляется ее вход в /3-клетки и уменьшается секреция инсулина (рис. 5.1).
Такой же механизм лежит в основе секреции паратгормона (паратиреоидный гормон, паратирин) и кальцитонина. Оба гормона влияют на концентрацию кальция и фосфатов в крови. Паратиреоидный гормон вызывает выход минеральных веществ из кости и стимулирует реабсорбцию кальция в почках и кишечнике, в результате чего возрастает концентрация кальция в плазме крови. Кальцитонин, напротив, стимулирует поступление кальция и фосфатов в костную ткань, в результате чего концентрация минеральных веществ в крови снижается. При высокой концентрации кальция в крови подавляется секреция паратиреоидного гормона и стимулируется секреция кальцитонина. В случае снижения концентрации кальция в крови секреция паратиреоидного гормона усиливается, а кальцитонина — ослабляется.
Такая регуляция постоянства внутренней среды организма, происходящая по принципу отрицательной обратной связи, очень эффективна для поддержания гомеостаза, однако не может выполнять все задачи адаптации организма. Например, кора надпочечников продуцирует стероидные гормоны в ответ на голод, болезнь, эмоциональное возбуждение и т. п. Чтобы эндокринная система могла «отвечать» на свет, звуки, запахи, эмоции и т. д., должна существовать связь между эндокринными железами и нервной системой.
Основные связи между нервной и эндокринной системами регуляции осуществляются посредством взаимодействия гипоталамуса и гипофиза (рис. 5.2). Нервные импульсы, приходящие в гипоталамус, активируют секрецию так называемых рилизинг-факторов (либеринов и статинов): тиреолиберина, соматолиберина, пролактолиберина, гонадолиберина и кортиколиберина, а также со-матостатина и пролактостатина. Мишенью для либеринов и статинов,
2. Контур гуморальной регуляции.
3. Взаимосвязь нервной и гуморальной регуляции.
4. Структурно-функциональная организация эндокринной системы. Эндокринные железы.
5. Основные механизмы действия гормонов. Мембраны и внутриклеточные рецепторы, G-белки, вторичные посредники.
6. Регуляция секреции гормонов.
7. Гипоталамо-гипофизарная система.
8. Нейросекреты гипоталамуса. Роль либеринов и статинов.
РЕГУЛЯЦИЯ КРОВООБРАЩЕНИЯ
I. Основные особенности регуляции кровообращения. Миогенная и нейрогуморальная регуляция тонуса сосудов. Роль эндотелия в регуляции тонуса
Система кровообращения служит для обеспечения адекватного обмена веществ в органах и тканях организма. Их потребности в кровотоке могут колебаться в широких пределах, поэтому деятельность системы должна обеспечивать как минимальные, так и значительно увеличенные потребности тканей в кислороде и веществах. Скорость оборота крови в организме характеризуется величиной минутного объема, то есть количеством крови, проходящей через сердце за 1 мин. Обычно в состоянии покоя эта величина составляет 4,5–5 л/мин. Поскольку общий объем крови в системе составляет примерно 7% массы тела, то фактически в организме человека среднего веса вся кровь проходит через сердце за 1 мин.
Величина минутного объема определяется соотношением градиента давления в системе кровообращения и сосудистого сопротивления:
MO = (АД-ВД)/СС (1)
где МО – минутный объем, АД и ВД – соответственно среднее артериальное и венозное давление, а СС – сопротивление сосудов.
Увеличение минутного объема возможно как за счет роста градиента давления, так и при снижении сосудистого сопротивления. Принципиальная разница между этими двумя путями состоит в изменении нагрузки на сердце: при повышении АД она возрастает, затрудняя выброс крови из сердца, а при уменьшении сосудистого сопротивления снижается, облегчая выброс. В связи с этим, очевидно, что второй способ увеличения минутного объема явно предпочтительнее, и он действительно реализуется на практике. Артериальное давление, как правило, поддерживается на относительно стабильном уровне благодаря разнообразным механизмам. Часть из них определяет сопротивление сосудов, другие регулируют АД в системе, третьи – общий объем крови. Все они в определенной степени вовлечены в регуляцию деятельности системы кровообращения при естественных нагрузках и стрессах.
В результате этого кровоток в органах, функциональные потребности которых значительно варьирует (скелетные мышцы, желудочно-кишечный тракт, кожа), может сильно изменяться. Напротив, в таких жизненно важных органах как мозг и почки – поддерживается почти на постоянном уровне.
При физиологическом покое организма величина сосудистого сопротивления относительно высока и определяется в основном сопротивлением крупных и мелких артерий (артериол). Составляющие основную часть их стенок гладкие мышцы находятся в постоянном сокращении (тонусе), величина которого зависит в конечном итоге от степени активации сократительных белков ионами Са2+ в каждой клетке. При этом тонус артерий может быть неодинаковым в различных тканях, что определяется их потребностью в кровотоке.
Основные механизмы, определяющие сосудов можно разделить на местные и центральные. Местные механизмы реализуются следующими путями.
1. Миогенная ауторегуляция. Некоторые сосуды (почек, головного мозга и т.д.) способны поддерживать постоянный объем кровотока при значительных колебаниях давления. Физическими факторами миогенной авторегуляции являются величина давления в сосуде и скорость кровотока. Величина давления определяет степень растяжения гладкомышечных клеток стенки. Повышение давления и усиленное растяжение клеток сопровождаются увеличением силы сокращения. Поэтому возникающее в ответ на повышение давления кратковременное расширение сосуда сменяется его сужением, это предохраняет сосуд от перерастяжения и ограничивает объем крови, проходящий через сосуд. Данная саморегуляторная реакция реализуется в основном в крупных артериях и имеет важное значение для сохранения нужного кровотока при длительном повышении АД, например при гипертонической болезни. При этом мышечный слой стенок утолщается, гипертрофируется, что позволяет поддерживать нормальный тонус в каждой мышечной клетке.
Важнейшая роль в регуляции артериального тонуса принадлежит эндотелию – тонкому слою клеток, отделяющих кровь от мышечного слоя. Совсем недавно установлено, что эндотелий восприимчив к действию чисто физических факторов, а именно скорости потока крови. Увеличение скорости потока сопровождается расширением сосуда, следствием чего (при постоянном давлении) является снижение скорости потока. Напротив, снижение скорости потока сопровождается сужением артерии и последующим увеличением скорости потока. Таким образом, эндотелий выступает как некая саморегулирующая структура, оптимизирующая скорость потока для данного участка ткани. В основе данной реакции лежит механочувствительность эндотелия. Поток крови в сосуде носит название ламинарного (пластинчатого) в связи с тем, что все слои цилиндрического потока крови, как и воды в гладкой трубе, движутся параллельно оси сосуда. При этом содержащиеся в потоке более крупные частицы смещаются к оси потока. В связи с повышенной вязкостью крови (по сравнению с водой) периферические слои цилиндрического потока, прилегающие к стенкам, движутся медленнее, чем центральные. В результате осевой поток, содержащий клетки (преимущественно эритроциты), движется значительно быстрее, чем пристеночные слои, в которых находится плазма. Увеличение степени деформации мембран эндотелиоцитов при повышении скорости потока крови сопровождается образованием оксида азота и других физиологически активных веществ, продуцируемых эндотелием. Тонус мышц снижается, сосуд расширяется, что приводит к снижению скорости потока.
Миогенная регуляция играет ведущую роль в поддержании сосудистого тонуса. Даже при полном отсутствии внешних влияний этот тонус сохраняется, поэтому его называют базальным. В его основе спонтанная активность гладкомышечных клеток сосудов.
2. Метаболическая ауторегуляция. На мускулатуру сосудов оказывают влияние кислород и продукты метаболизма тканей. Снижение напряжения О2, повышение концентрации СО2, ионов Н+, молочной кислоты и других веществ в крови ведет к расширению сосудов. Метаболическая саморегуляция приспосабливает местный кровоток к функциональным потребностям органа.
3. Влияние тканевых гормонов. Находящиеся в крови физиологически активные вещества – брадикинин, гистамин, серотонин – связываясь с наружной мембраной эндотелиоцита, вызывают образование веществ, оказывающих на мышечные клетки расслабляющее или сокращающее действие. Брадикинин образуется при активации пищеварительных желез и расширяет их сосуды. Гистамин выделяется главным образом при повреждении кожи и слизистых оболочек (при сдавливании сосудов может вызвать гистаминовый шок, расширяя их). Сравнительно недавно было установлено, что основным (а возможно, и единственным) эндотелийзависимым фактором расслабления является NO2 – оксид азота. Это позволило объяснить, почему нитраты, в том числе нитроглицерин, являются весьма эффективными лекарствами, устраняющими спазм сосудов. Сосудосуживающее действие оказывает серотонин (участвует в запуске мигрени).
II. Нейрогуморальная регуляция сосудистого тонуса.
Координационные акты, которые приспосабливают сердечно-сосудистую систему к оптимальному обеспечению кровоснабжением органов и тканей осуществляется и за счет центральных воздействий: со стороны нервной системы и при влиянии гуморальных факторов.
Нервная регуляция просвета сосудов осуществляется вегетативной нервной системой. Регуляция артериального тонуса осуществляется преимущественно при помощи окончаний симпатических нервов, которые обильно оплетают все сосуды, кроме капилляров. Большая часть симпатических волокон при возбуждении выделяет медиатор норадреналин (НА). НА действует на мембраны гладкомышечных клеток, увеличивая проникновение ионов Са2+ в клетки и тем самым степень активации сократительных белков. Симпатические волокна имеют постоянную тоническую активность (разряд с частотой 1-3 с-1), о чем свидетельствует опыт Клода Бернара (перерезка симпатического нерва у кролика привела к тому, что сосуды, которые нерв иннервировал, значительно расширились). Эти волокна поддерживают тонус сосудов и действуют как вазоконстрикторы.
Парасимпатические нервы иннервируют сосуды наружных половых органов. Волокна активируются при половом возбуждении, выделяют медиатор ацетилхолин, что приводит к расширению сосудов, т.е. парасимпатические нервы действуют как вазодилататоры.
Влияние гормонов надпочечников. Катехоламины адреналин и норадреналин постоянно выделяются мозговым слоем надпочечников и циркулируют в крови. При этим 80% катехоламинов, секретируемых надпочечниками приходится на долю адреналина и лишь 20% –НА. Доля НА увеличивается при стрессе.
Адреналин может оказывать как сосудосуживающий, так и сосудорасширяющий эффект, НА – лишь сосудосуживающий. Разнонаправленность определяется наличием различных типов адренорецепторов – α и β. Эти рецепторы представляют участки мембраны сосудистых мышц с особым химическим строением. Возбуждение α-рецепторов сопровождается сокращением мускулатуры сосудов, а возбуждение β-рецепторов – расслаблением. НА действует преимущественно на α-рецепторы, адреналин – на оба типа. В большинстве сосудов есть оба типа рецепторов, при этом, если преобладают α-рецепторы, то адреналин вызывает их сужение, если – β-рецепторы – расширение. Порог возбуждения β-рецепторов – ниже, чем α-рецепторов. Поэтому, в низких концентрациях адреналин вызывает расширение сосудов, в высоких концентрациях (в стрессовой ситуации) – сужение.
III. Гемодинамические центры рефлекторной регуляции тонуса сосудов.
В регуляции кровообращения принимают участие следующие центры.
1. Спинальные центры. Симпатические нейроны, аксоны которых образуют сосудосуживающие волокна, лежат в боковых рогах спинного мозга. В норме находятся под контролем вышележащих центров.
2. Стволовой (бульбарный) центр. Сосудодвигательный центр продолговатого мозга является основным центром поддержания тонуса сосудов и рефлекторной регуляции АД. Центр расположен на дне четвертого желудочка мозга. Его разделяют на прессорную и депрессорную зоны, которые частично перекрываются.
а). Депрессорная зона (лежит медиокаудально) снижает артериальное давление, уменьшая активность симпатических сосудосуживающих волокон и уменьшая сердечный выброс (ослабляет симпатическую стимуляцию сердца). Вблизи лежит кардиоингибирующая зона, которая действует через волокна блуждающего нерва (Х), идущие к сердцу. Ее активность ведет к уменьшению сердечного выброса.
б). Прессорная зона (лежит антеролатерально) повышает артериальное давление и сердечный выброс.
3. Центры гипоталамуса. Активация каудальных отделов гипоталамуса повышает активность симпатической системы (с соответствующими эффектами), что сопутствует реакции «борись или убегай» и ощущению тревоги. Активация ростральных отделов вызывает реакции обратной направленности, восстанавливает резервы организма. Таким образом, гипоталамус интегрирует вегетативные и моторные компоненты поведенческих реакций.
4. Кора головного мозга. Раздражение неокортекса (внешняя поверхность полушарий) вызывает преимущественно прессорные эффекты. Эти эффекты обеспечивают опережающие реакции при выполнении двигательных задач. Стимуляция палеокортеса (внутренняя поверхность полушарий) вызывает как прессорные (орбитальная область), так и депрессорные (поясная извилина) реакции.
Разнообразие этих реакций иллюстрировали опыты А. Экса. При провоцировании у испытуемых эмоции гнева АД росло, а пульс замедлялся. При вызове страха – АД падало, а частота пульса росла.
IV. Прессорные и депрессорные рефлексы. Роль аортальной и синокаротидной зоны.
Необходимую информацию о состоянии сосудистой системы мозговые центры получают от датчиков, находящихся в стенках крупнейших артерий. Чувствительные к давлению датчики – барорецепторы находятся в стенках аорты (аортальная зона) и сонных артериях, снабжающих кровью головной мозг (синокаротидная зона). Они реагируют не только на величину среднего АД, но и на скорость его прироста и амплитуду пульсового давления. Дифференцированная информация от датчиков поступает по нервным стволам в стволовой сосудодвигательный центр. Как отмечено выше, центр управляет артериальным и венозным тонусом, а также силой и частотой сокращений сердца. При отклонении от стандартных величин, например при снижении среднего АД, клетки центра посылают команду к симпатическим нейронам, и тонус артерий повышается (прессорный рефлекс). При избыточном АД симпатические нейроны тормозятся и АД падает (депрессорный рефлекс). Таким образом, система представляет собой ауторегуляторный механизм действующий по принципу замкнутой цепи обратной связи (рис. 1). (18-29) Сигналы от барорецепторов при кратковременных сдвигах АД вызывают рефлекторные изменения сердечного выброса и периферического сопротивления, и в результате восстанавливается исходный уровень давления.
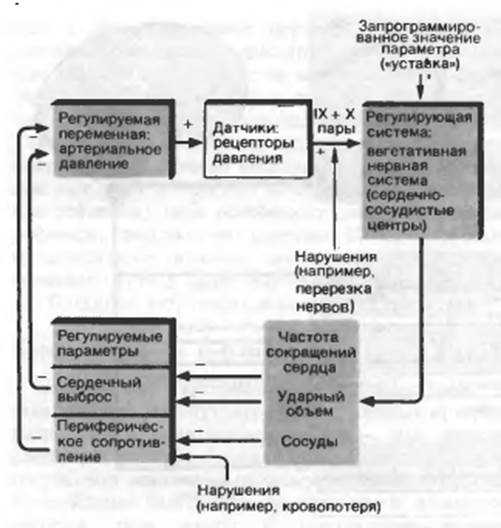
Барорецепторная система принадлежит к числу быстродействующих механизмов регуляции, ее воздействие проявляется в течение нескольких секунд. Мощность регуляторных влияний на сердце настолько велика, что сильное раздражение барорецепторной зоны, например, при резком ударе по области сонных артерий способно вызвать кратковременную остановку сердца и потерю сознания из-за резкого падения АД в сосудах головного мозга.
Особенность барорецепторов состоит в их адаптации к определенному уровню и диапазону колебаний АД. Феномен адаптации состоит в том, что рецепторы реагируют на изменения в привычном диапазоне давления слабее, чем на такие же по величине изменения в необычном диапазоне АД. Поэтому, если по какой-либо причине уровень АД сохраняется устойчиво повышенным, барорецепторы адаптируются к нему и уровень их активации снижается – данный уровень АД уже считается как бы нормальным. Такого рода адаптация происходит при гипертонической болезни, и вызываемое под влиянием применения медикаментов резкое снижение АД уже будет восприниматься барорецепторами как опасное снижение АД с последующей активацией противодействия этому процессу.
При искусственном выключении барорецепторной системы диапазон колебаний АД в течение суток значительно увеличивается, хотя в среднем остается в нормальном диапазоне благодаря наличию других регуляторных механизмов. В частности, столь же быстро реализуется действие механизма, следящего за достаточным снабжением клеток головного мозга кислородом. Для этого в сосудах головного мозга имеются специальные датчики, чувствительные к снижению напряжению О2 и повышению Н+ и СО2 в артериальной крови, – хеморецепторы (расположены в аортальной и каротидной областях, чувствительны также к никотину). Поскольку наиболее частой причиной снижения напряжения кислорода служит уменьшение кровотока из-за снижения АД, сигнал от датчиков поступает к высшим симпатическим центрам, которые способны повысить тонус артерий тела, а также стимулировать работу сердца (прессорные рефлексы). Благодаря этому АД восстанавливается до уровня, необходимого для снабжения кровью мозговых клеток.
Более медленно (в течение минут) действует третий механизм, чувствительный к изменениям АД – почечный. Его существование определяется условиями работы почек, требующих для нормальной фильтрации крови поддержания стабильного давления в почечных артериях. При снижении пульсового давления из-за различных причин почки вырабатывают свой гормон – ренин, который превращается в крови последовательно в ангиотензин I и II, последний оказывает сильное сосудосуживающее действие, и АД повышается. Ренин-ангиотензиновая система регуляции реагирует не столь быстро и точно, как нервная система, и поэтому даже кратковременное снижение АД может “запустить” образование значительного количества ангиотензина II и вызвать тем самым устойчивое повышение артериального тонуса.
Существует специальная форма гипертонической болезни, вызванная склерозом или сужением почечной артерии. В связи с этим значительное место в лечении заболеваний сердечно-сосудистой системы принадлежит препаратам, снижающим активность фермента, превращающего ангиотензин I в II.
Кроме этих механизмов, непосредственно стабилизирующих давление, оно также может быть нормализовано через регуляторные механизмы, определяющие объем циркулирующей крови. Его величина в организме относительно постоянна и составляет около 7% массы тела. Регуляция объема крови также может осуществляться с различной скоростью. Быстродействующий механизм регуляции, реализуемый в пределах нескольких минут, осуществляется нервными клетками сосудодвигательного центра на основе информации, поступающей от рецепторов растяжения, находящихся в стенках предсердий. Выбор места установки датчиков, как и в случае барорецепторов, продиктован целесообразностью, они находятся в легкорастяжимых участках системы кровообращения, через которые проходит вся масса крови. Если степень растяжения стенок предсердий из-за недостаточного наполнения предсердий уменьшается, центр воспринимает этот сигнал как признак уменьшения объема крови. Для его восстановления могут быть использованы как повышение симпатического тонуса, так и выработка гипофизом гормона вазопрессина, обладающего антидиуретическим, то есть задерживающим выделение воды в почках, действием.
Другим эффективным и также быстро действующим механизмом регуляции объема циркулирующей крови является регуляция объема воды в тканях, осуществляющаяся через капиллярную сеть. Она основана на противодействии гидростатического давления, заставляющего воду поступать из крови в ткани, и онкотического давления белков плазмы, притягивающего воду обратно. Уменьшение объема циркулирующей крови, сочетающееся со снижением давления на входе в капилляры, будет ограничивать направленный в ткани поток воды, удерживать ее в сосудистом русле. При значительном снижении давления может происходить мобилизация воды из ткани с увеличением объема крови и повышением АД. Хотя данный механизм реализуется довольно быстро, стабилизация объема требует все же нескольких минут, потому что поступление воды в кровь снижает онкотическое давление в ней и для его выравнивания требуется уравновешивание во всей массе крови.
Еще медленнее осуществляется регуляция объема при включении предсердного гуморального механизма. Рецепторы растяжения стенки предсердий связаны с клетками, вырабатывающими пептид (простейший белок), который способен существенно ускорить выделение ионов натрия (и связанной с ним воды) в почках. При возрастании объема крови степень растяжения стенок увеличивается и вырабатываемый натрий-уретический пептид повышает выработку мочи, что способствует восстановлению объема крови. В связи с включением синтезирующего белок механизма, данный процесс длится несколько часов.
Все эти механизмы поддерживают систолическое АД на уровне 120 мм рт. ст., а диастолическое – 80 мм рт. ст. (норма для молодых здоровых людей). С возрастом АД повышается, причем систолическое давление – больше, что связано со снижением эластичности сосудов.
V. Рефлекторная регуляция гемодинамики при изменении положения тела и мышечной работе, а также при действии естественных факторов,
Разнообразие и дублирование регуляторных механизмов делают АД весьма устойчивым при различных поведенческих реакциях организма. К их числу можно отнести изменения положения тела, ритма дыхания, суточные колебания гормонов в крови или температуры окружающей среды. Адекватная регуляция кровообращения обеспечивает также устойчивую работу системы при физических нагрузках.
Положение тела в пространстве определяет распределение крови в различных бассейнах в связи с емкостной функцией вен. При переходе из горизонтального положения в вертикальное в венах нижней части туловища депонируется около 15% всего объема крови. Это замедляет приток крови к сердцу и уменьшает сердечный выброс. При неизменном сосудистом сопротивлении это означает снижение АД (формула (1)). Для восполнения минутного объема используется кровь, находящаяся во внутренних органах. Таким образом, происходит перераспределение крови, а снижение АД предотвращается благодаря стимуляции деятельности сердца и повышению венозного тонуса. В последнем случае уменьшение диаметра вен сопровождается ускорением течения крови и увеличением притока к сердцу. Важнейшей же особенностью сердца как насоса является равенство притока и выброса.
Таким образом, вертикальное положение тела сочетается с более значительным напряжением регуляторных механизмов, чем горизонтальное. При хорошей регуляции величина отклонения АД при переходе из горизонтального положения в вертикальное (ортостатическая проба) не должна превышать 5 мм рт.ст., при недостаточной компенсации АД снижается больше, при слабой компенсации может развиться обморок.
Подобные же механизмы поддержания минутного объема включаются и при потере части крови (кровотечении). При одномоментной потере 0,5 л крови ее объем может быть полностью восстановлен уже через 30 мин за счет мобилизации воды из тканей вследствие снижения АД и уменьшения выделения через почки.
Выполнение физической работы сопряжено с расходом энергии в работающих мышцах. Источниками энергии в мышечных клетках являются запасы АТФ, креатинфосфата и гликогена. Если мышца из состояния покоя сразу переходит к максимальной активности, то работа вначале выполняется за счет имеющихся в мышце легко мобилизуемых запасов энергии – АТФ и креатинфосфата. Но они способны обеспечить лишь весьма кратковременную работу (до 0,5 мин), поэтому уже через несколько секунд активируется распад гликогена и происходящий гликолитический (анаэробный) синтез АТФ обеспечивает энергию для выполнения работы средней длительности – до 1,5 мин. Далее в связи с исчерпанием запасов гликогена в клетках выполнение работы возможно лишь при условии аэробного синтеза АТФ в митохондриях, а для этого необходимо увеличение кровоснабжения мышц. Сигналом, запускающим расширение артериол, снабжающих мышцу, является выход из клеток продуктов распада АТФ – АДФ, АМФ и особенно аденозина. В покоящейся мышце аденозин вновь ресинтезируется до АТФ, но при превышении распада АТФ над ресинтезом аденозин попадает во внеклеточное пространство и, накапливаясь там, диффундирует к стенкам артериол. Он обладает сильным сосудорасширяющим действием, что и обеспечивает достаточный приток оксигенированной крови к работающим клеткам. Необходимость накопления достаточного количества аденозина и диффузии его во внеклеточном пространстве объясняет довольно длительную задержку, требуемую для активации окислительного ресинтеза АТФ. В течение этого периода (до 1,5–2 мин) работа мышц осуществляется за счет внутренних запасов энергии, после него работа полностью обеспечивается за счет притока субстратов (глюкозы) и запасы АТФ в клетке восстанавливаются даже при продолжающейся работе. В период, предшествующий выходу окислительного фосфорилирования на устойчивый уровень, использование энергетических запасов превышает их синтез и их содержание снижается. Работа при этом как бы выполняется в долг. Действительно, в физиологии спорта существует понятие кислородного долга, поскольку потребление кислорода нарастает медленнее, чем работа. В устойчивом состоянии уровень потребления кислорода полностью соответствует работе, а после прекращения работы потребление кислорода снижается постепенно. Тем самым происходит возвращение кислородного долга. Эти закономерности обосновывают применение предварительной разминки мышц, которым вскоре предстоит интенсивная работа, благодаря чему мышцы начинают работу при почти полностью мобилизованном кровотоке.
Необходимо заметить, что кровоток в мышцах существенно и устойчиво возрастает лишь при динамической (циклической) работе, когда сокращения чередуются с расслаблением. При статической работе, сопряженной с развитием максимальной силы сокращений, вены пережимаются и кровоток в капиллярах останавливается. Вот почему длительные максимальные усилия невозможны. Если потребление энергии начинает превышать ее синтез, наступает утомление мышцы.
Такое различие между динамической и статической работой лежит в основе дифференцированного подхода к тренировке спортсменов. Фактически все виды статических спортивных нагрузок (подъем и удержание штанги, выполнение креста и угла на кольцах, силовые единоборства) выполняются за счет накопленных в мышцах энергетических запасов. Эти же запасы играют главную роль и при выполнении кратковременной интенсивной динамической работы, например спринтерского бега. В отличие от этого стайерский бег, марафон, длительное плавание, лыжный спорт, велосипед требуют высокого совершенства системы кровоснабжения работающих мышц. Таким образом, даже при тяжелой динамической работе запасы энергии в клетке снижаются умеренно. Полное восстановление уровня энергетических запасов происходит после работы, когда компенсируется кислородный долг. В фазе восстановления уровень энергозапасов может даже превышать исходный, что лежит в основе тренировочного процесса, имеющего целью повысить максимальные функциональные возможности мышц.
Чем более значительные мышечные группы вовлечены в работу, тем сильнее возрастает кровоток в этих участках сосудистого русла. Известно, что кровоток может возрастать по сравнению с периодом покоя в десятки раз. Это должно бы вызывать снижение общего АД, но на самом деле АД не снижается из-за включения регуляторных факторов.
1. При каждом сокращении мышц кровь выжимается из находящихся в них вен. В состоянии покоя в венах находится более двух третей всего объема крови в системе – вены являются емкостными сосудами. Увеличение притока к сердцу мобилизует его работу, и сердечный выброс возрастает в такой же степени, как и приток крови.
2. Вследствие усиленного растяжения камер сердца, в частности предсердий, возрастает частота сокращений сердца и фактически в устойчивом состоянии увеличенный минутный объем, необходимый для выполнения работы, достигается за счет повышенной частоты сокращений сердца при неизменном ударном объеме и АД. Вследствие увеличенного выброса из правого желудочка и ограниченной емкости сосудистого русла в малом круге скорость потока по сосудам легких также возрастает.
3. В поддержание стабильного АД вносит свой вклад и повышение артериального тонуса во внутренних органах, деятельность которых не является необходимой для выполнения физической работы. Кровоток во внутренних органах снижается до уровня, необходимого для обеспечения минимальной потребности органа в кислороде.
4. Снижению АД при физической работе противодействуют также механизмы, регулирующие объем циркулирующей крови. Повышение тканевого давления в мышцах уменьшает поток воды из капилляров в ткани, а потеря воды через кожу при испарении и потении, сопровождающаяся повышением онкотического давления крови, способствует перемещению воды из тканей в капилляры и увеличению массы циркулирующей крови. После внезапного прекращения интенсивной динамической работы выключается важнейший фактор, обеспечивавший усиленный приток крови к сердцу – мышечные сокращения, что естественно сопровождается резким снижением сердечного выброса. В условиях сниженного тонуса артериальных сосудов, который не может быть восстановлен ранее чем за несколько десятков секунд, это чревато опасностью снижения АД и возникновением обморока. Вот почему продолжение работы, даже на значительно сниженном уровне, в течение нескольких минут после прекращения интенсивной нагрузки является необходимым для сохранения нормального АД.
Уровень гормонов в крови также оказывает определенное воздействие на величину АД, ее максимум наблюдается обычно в 15 часов, а минимум – в 3 часа ночи. Нарушение обычного режима дня или перемещение в сильно отличающиеся часовые пояса сопровождается соответствующей перестройкой в системах регуляции, во время которой деятельность системы не столь совершенна. Различные стрессорные реакции благодаря изменению спектра и уровня гормонов также влияют на сосудистый тонус и работу сердца.
Температура окружающей среды способна существенно повлиять на регуляцию системы посредством изменения артериального тонуса в поверхностно расположенных тканях. Так, например, значительное повышение температуры кожи сопровождается резким расширением сосудов, снижение сопротивления привлекает в данную область увеличенное количество крови. В результате АД в других областях, и в первую очередь во внутренних органах, будет снижаться, и для стабилизации АД должны быть задействованы механизмы регуляции как АД, так и объема крови.
VI. Особенности кровообращения в некоторых отдельных органах.
Кровообращение в сердце обеспечивается коронарными сосудами. И симпатические и парасимпатические нервы обеспечивают расширение коронарных сосудов.
Мозговое кровообращение более интенсивно, чем других органов – мозг потребляет 15% сердечного выброса, хотя сам составляет 2% веса тела. Этот кровоток исключительно важен, т.к. его прекращения на 5 мин приводит к гибели мозга. Основные сосуды мозга находятся на его поверхности в мягкой мозговой оболочке. Они имеют многочисленные изгибы. Все это сглаживает последствия изменения АД по отношению к работе мозга.
Легочное кровообращение (малый круг) осуществляется по относительно коротким сосудам с малым сопротивлением и нетолстыми стенками. АД в легочных артериях в 5-6 раз меньше, чем в аорте. В связи с большой растяжимостью легочные сосуды играют роль кровяных депо.
Кровяным депо также является селезенка. Капилляры, пронизывающие селезенку, открываются в ее пульпу (мякоть). Здесь содержится кровь особенно насыщенная эритроцитами.
Почечное кровообращение отличается особенно высокой интенсивностью. Его особенностью является наличие двух систем капилляров, расположенных последовательно. Между ними высокий градиент давления, что обеспечивает образование мочи.
1. Капелько В.И. Гидродинамические основы кровообращения // Соросовский Образовательный Журнал. 1996. № 2. С. 44–50.
2. Физиология человека / Ред. Р. Шмидт, Г. Тевс. М.: Мир, 1996. Т. 3: Кровь, кровообращение, дыхание.
3. Основы физиологии человека / Ред. Б.И. Ткаченко. СПб.: Междунар. фонд истории науки, 1994. Т. 1.
СИСТЕМА ПИЩЕВАРЕНИЯ. ПИЩЕВАРЕНИЕ В ПОЛОСТИ РТА.
Дата добавления: 2017-09-19; просмотров: 2601;
