Электросинтез гипохлорита натрия
Гипохлорит натрия (NaOCl) является достаточно сильным окислителем и находит применение при очистке от примесей сточных вод, а также как эффективное антисептическое средство. Гипохлорит натрия получают электролизом водного раствора хлорида натрия без диафрагмы. Суммарная реакция образования гипохлорита натрия в электролизере может быть записана следующим образом:
NaCl + H2O → NaOCl + H2 (8.и)
Побочными электрохимическими реакциями являются:
|
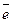 на катоде OCl- + H2O + 2
на катоде OCl- + H2O + 2 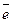 → Cl- + 2OH-
→ Cl- + 2OH-
Условия электролиза. В производстве гипохлорита натрия используют различные материалы для изготовления анодов – графит, магнетит, титан с осажденной на поверхность платиной, ОРТА. Наибольший интерес в настоящее время представляют ОРТА.
Выход гипохлорита по току зависит от потенциала ОРТА. Максимальный выход по току (98,0%) достигается при потенциале анода 1,6 В (отн. нас. каломельного электрода).
Плотность тока зависит от материала анода. При использовании графитовых анодов электролиз можно провести при плотностях тока до 1,4 кА/м2. На платино-титановых анодах выход гипохлорита натрия по току практически не изменяется до достижения плотности тока 4 кА/м2 (0,4 А/см2). Оптимальной плотностью тока при электролизе с ОРТА является 1,5 – 2 кА/м2 (0,15 – 0,2 А/см2). При повышении анодных плотностей тока выход по току гипохлорита натрия несколько снижается, а хлората натрия - возрастает.
Для практического использования пригодны разбавленные растворы гипохлорита, применять концентрированные исходные растворы хлорида натрия экономически нецелесообразно. Обычно элеткролизу подвергают растворы, содержащие 50 – 100 г/л NaCl, а в некоторых случаях – морскую воду.
Оптимальное значение рН раствора хлорида близко к 7. Подкисление исходного раствора приводит к повышению концентрации свободной хлорноватистой кислоты и к возрастанию скорости побочной химической реакции образования хлората:
OCl- + 2HOCl → ClO3- + 2HCl (8.л)
При повышении рН раствора зона образования гипохлорита натрия сдвигается в сторону анода, что благоприятствует попаданию ионов OСl- на анод и их окислению до хлората. Кроме того, с увеличением рН облегчается побочная электрохимическая реакция выделения кислорода.
Для электросинтеза гипохлорита натрия получили распространение электролизеры сравнительно небольшой мощности.
Дата добавления: 2017-01-29; просмотров: 2416;
