Шкала оцінки важкості синдрому вкороченого інтервалу QT
(за Gollob M., 2011)
| Методи дослідження | Дані | Оцінка, бали |
| ЕКГ | QTc < 370 мс | |
| QTc < 350 мс | ||
| QTc < 330 мс | ||
| Точка J –T верхівка інтервал < 120 мс | ||
| Анамнез захворювання | Поліморфна шлуночкові тахікардія чи фібриляція шлуночків | |
| Раптова зупинка серця | ||
| Раптова втрата свідомості | ||
| Фібриляція передсердь | ||
| Сімейний анамнез | Члени сім’ї з встановленим діагнозом синдрому вкороченого інтервалу QT | |
| Раптова смерть близьких родичів | ||
| Синдром раптової дитячої смерті | ||
| Генотип | Позитивний результат |
Загальна оцінка:
≤2.0 бали – низька ймовірність наявності синдрому вкороченого інтервалу QT.
3.0-2.0 бали – середня ймовірність синдрому вкороченого інтервалу QT.
≥4.0 бали – висока ймовірність синдрому вкороченого інтервалу QT.
Питання допуску. Питання профілактики подібного синдрому, особливо в середовищі спортсменів в доступній літературі практично не розглядаються. Можливість виконання фізичних навантажень при даному захворюванні не встановлено. Лікування зводиться також до встановлення імплантаційного кардіовертера-дефібрилятора.
Синдром Бругада є ще одним типом каналопатій, що може призводити до РСС в спорті. Виникає він при мутаціях в генах SCN5A (20-25% випадків), KCND2, GPD1L, CACNA1C, CACNB2, KCNE3, KCND3, KCND3, SCN1B, SCN5A, SCN10A та HEY2, які відповідають за структуру іонних каналів натрію, кальцію та калію. Зустрічається у представників азіатської нації з частотою 12-58:10000 у європейців та американців – 5:10000, передається переважно за аутосомно-домінантним типом. В 20% випадків є причиною РСС у пацієнтів без структурних змін у серці, при чому у чоловіків цей синдром зустрічається у 8 разів частіше. Синдром Бругада за ЕКГ-змінами поділяється на три типи (рис. 5.1):
1. Значна елевація сегменту ST більш як 2 mm (0.2 mV) переходить в косо-низхідну фазу, що закінчується негативною T-хвилею.
2. Має сідлоподібну будову, де відмічається елевація точки J на 2 мм та більше і елевація сегменту ST на 1 мм з подальшим позитивною чи двофазною Т-хвилею.
3. Може мати форми першого чи другого типів при умові, що елевація точки J відбувається до 2 мм, а ST сегменту до 1 мм.
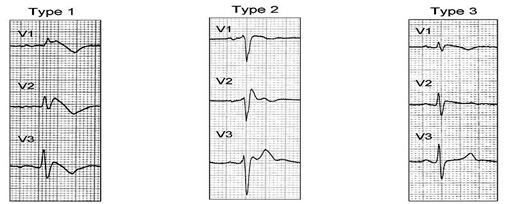
Рис. 5.1. Варіанти синдрому Бругада
Дані зміни спостерігаються у 1-3 грудних відведеннях та поєднуються з неповною блокадою правої ніжки пучка Гіса. Особливо характерними для даного синдрому є виникнення приступів у нічний час або у спокої, позитивна реакція на введення блокаторів натрієвих каналів (флекаініду, прокаінаміду).
Стратифікація ризику для пацієнтів з синдромом Бругада:
1. Пацієнти з високим ризиком: перенесена клінічна смерть в анамнезі, спонтанний 1 тип ЕКГ змін, при появі індукованої шлуночкової тахікардії.
2. Пацієнти з низьким ризиком: безсимптомні пацієнти, у яких ЕКГ зміни виникають тільки після індукції фармакологічними препаратами.
Вибором при лікуванні для даної категорії пацієнтів є встановлення імплантаційного кардіовертера-дефібрилятора (ІКВ). За рекомендаціями консенсусу по синдрому Бругада (2005), імплантація ІКД для пацієнтів з високим ризиком має І клас доказовості щодо профілактики первинних та вторинних ускладнень і ІІ b клас для пацієнтів з низьким ризиком.
Катехоламінергічна поліморфна шлуночкова тахікардія може бути причиною РС при фізичних навантаженнях та емоційному стресі в 15% випадків у молодих осіб. Хоча цей синдром зустрічається з частотою 1:10000 в загальній популяції, але летальність дуже висока (30-50% у осіб до 30 років). Розрізняють два типи захворювання: пов’язаний з мутацією в гені RYR2 1q43 хромосоми (аутосомно-домінантний тип спадкування), відповідального за синтез ріанодін-рецепторів кальцієвих каналів, і гену CASQ2 1p13.3-p11 хромосоми (аутосомно-рецесивний тип спадкування), відповідального за синтез кальциквестрину саркоплазматичного ретикулуму, що загалом викликають порушення функції іонних каналів клітин серцевого м’язу та електричну нестабільність міокарду. Типовою картиною при загостренні є зміни на ЕКГ: двонаправлена шлуночкова тахікардія зі зміною вісі QRS-комплексу на 180 градусів, яка може переходити у фібриляцію шлуночків. Звичайно це захворювання клінічно перебігає безсимптомно. Для встановлення діагнозу використовують Холтерівське добове моніторування серцевого ритму, стрес-тести для діагностики появи аритмії у відповідь на фізичні чи психічні навантаження. Діагностично значущим при даному захворюванні є поява шлуночкової аритмії при ЧСС більше 110 уд/хв та погіршення проявів аритмії відповідно до збільшення ЧСС.
Лікування даного синдрому не розроблено. Зустрічаються поодинокі дані щодо ефективності застосування бета-блокаторів, блокаторів кальцієвих каналів (верапамілу), флеканідіну (інгібітора синтезу ріанодін-рецепторів) та встановлення імплантаційного кардіовертера-дефібрилятора. При неефективності бета-блокаторів є автори, що рекомендують застосовувати симпатичну денервацію.
Синдроми передчасного збудження шлуночків. Іншими причинами, що можуть призводити до раптової серцевої смерті в спорті та пов’язані з порушенням провідності нервового імпульсу в серці є синдроми преекзитації – передчасного збудження шлуночків надшлуночковими імпульсами, що пов'язані з існуванням додаткових трактів проведення та м'язових шляхів. За даними Фремінгемського дослідження у хворих із синдромами преекзитації РС виникає в 1% випадків суправентрикулярної тахікардії і в 6% випадків фібриляції передсердь. Найбільш розповсюдженими є синдром Вольфа-Паркинсона-Уайта (WPW) з частотою 0,1-3 на 1000, синдром Клерка-Леві-Кристеско (CLC). ЕКГ-критерії класичного синдрому WPW (при проведенні збудження через пучки Kent) є наступними:
1. Наявність дельта-хвилі (відхилення тривалістю 0,03-0,06 с, рідше з амплітудою > 5 мм (рис. 5.2);
2. Скорочення інтервалу PQ, PR < 0,12 с.;
3. Розширення комплексу QRS > 0,12 с.;
4. Зміна термінальної частини шлуночкового комплексу.
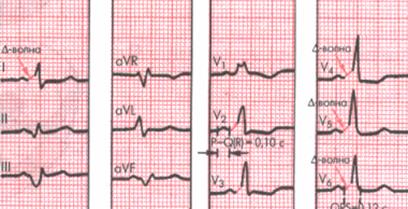
Рис. 5.2. ЕКГ хворого з синдромом WPW
(стрілкою вказано додаткову хвилю на висхідній частині комплексу QRS)
Питання допуску. Рекомендації щодо допуску до занять фізичними вправами осіб з синдромами передчасного збудження шлуночків представлені в підрозділі 5.2.
Аритмогенна дисплазія правого шлуночка (АДПШ) або аритмогенна правошлуночкова кардіоміопатія –генетичне захворювання з аутосомно домінантним типом спадкування, що характеризується збільшенням правого шлуночка за рахунок заміщення його стінки жировою та сполучною тканиною, шлуночковими тахіаритміями й високою вірогідністю РКС. Частота виникнення РКС при АДПШ складає 0,5 на 100000 спортсменів на рік, в загальній структурі РКС в спорті це складає 3%, зустрічається переважно у чоловіків, в 50% має сімейні ознаки. Найчастіше це захворювання зустрічається в Італії, де на долю АДПШ приходиться 25% РКС в спорті. На сьогодні виділено 12 форм АДПШ. На генетичному рівні воно найчастіше проявляється мутаціями гену DES в хромосомі 10q22.3 (20-35% випадків), що кодує протеїн десмін – якірний протеїн, який відповідає за адгезію десмосом; рідше виявляється мутації гену RYR2 1q42-q43, що кодує синтез кардіального ріанодін-рецептору. Але в 50% випадків АДПШ жодних відомих мутацій знайдено не було. В більшості випадків РКС в спорті померлі при житті не пред’являли скарг. РКС в них було першим симптомом захворювання.
При проведенні ЕКГ виявляються специфічні дані (рис. 5.3): інверсія зубця Т у правих грудних відведеннях (V1-V3), неповна блокада правої ніжки пучка Гіса, епсілон-хвиля на низхідній частині комплексу QRS виявляється в 50%, шлуночкова екстрасистолія та тахікардія. ЕхоКГ вказує на збільшений гіпокінетичний правий шлуночок з витонченою вільною стінкою. Збільшення правого шлуночка може призводити до недостатності та регургітацію на трикуспідальному клапані.
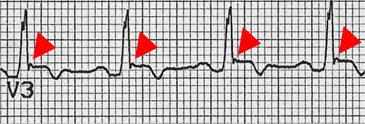
Рис. 5.3. Епсілон-хвилі (відмічені стрілкою) та реверсія зубця Т при АДПШ
Питання допуску. Встановлення діагнозу АДПШ призводить до дискваліфікації спортсмена в зв’язку з великою ймовірністю раптової кардіальної смерті під час тренувань.
Міокардити як причина РКС в спорті зустрічаються з частотою 5%. Запальні процеси в серцевому м’язі можуть призводити до електричної нестабільності та виникнення фатальних аритмій. Найбільш часто це пов’язується з виявленням вірусу Коксакі В (50% випадків). У спортсменів з міокардитом, які померли раптово при виконанні фізичних навантажень, відмічались скарги на болі в груді, задишку, слабкість, непритомність та загальні ознаки інфекційного процесу. Клінічно відмічались ознаки серцевої недостатності, при рентгенографічному досліджуванні – кардіомегалія та застійні явища в легенях, при ЕКГ у 10-50% випадків відмічається елевація сегменту ST, при ЕхоКГ – гіпокінезія та зменшення фракції викиду.
Сommotion cordis. Велика кількість смертей під час спортивних тренувань чи змагань відбувається внаслідок травматичних пошкоджень, зокрема грудної стінки. Внаслідок вдавлення передньої стінки грудної клітини можливе виникнення рефлекторної зупинки серця (шлуночкової фібриляції) т.з. commotion cordis. Як причина РКС в спорті серед молодих спортсменів commotion cordis посідає друге місце і загалом складає 20% випадків. Найбільш часто подібний стан виникає в ігрових видах спорту, де швидко переміщується твердий об’єкт (хокей, бейсбол, лакрос), а також при стрільбі з пневматичної зброї (внаслідок віддачі прикладу гвинтівки). В експерименті було встановлено, що виникнення шлуночкової фібриляції можливе лише за умови нанесення удару в момент низхідної частини Т хвилі серцевого імпульсу. Висновки щодо причин та механізмів даного порушення дало змогу застосовувати ряд профілактичних заходів: обов’язкове одягання захисної амуніції в області грудної клітини, встановлення нормативів ваги та щільності бейсбольного м’яча, відповідно віковим групам, оволодіння навичками серцево-легеневої реанімації тренерським колективом та оснащення місць проведення тренувань та змагань автоматичними дефібриляторами, що значно знизило смертність від commotio cordis.
Ішемічна хвороба серця. Значне місце в структурі причин РКС в спорті, особливо у осіб з віком понад 35 років, займає ішемічна хвороба серця (ІХС), яку встановлюють більше, ніж у 80% випадків. При чому з віком вірогідність настання фатального випадку від цього захворювання зростає. Задля профілактики РКС в спорті осіб з ІКС поділяють на дві групи:
1. Група особливої уваги – особи з клінічними проявами ІХС, які потребують індивідуального спостереження, регулярних обстежень, рекомендацій щодо оздоровлення способу життя та медикаментозного лікування.
Ця група, в свою чергу, поділяється на 2 підгрупи а залежності від ризику раптової кардіальної смерті – з середнім та високим ризиком (табл. 5.6).
Таблиця 5.6
Дата добавления: 2016-12-08; просмотров: 1069;
