Раствор объемом 500 мл содержит NaOH массой 5 г. Определить молярную концентрацию этого раствора.
| Дано: | Решение: |
| V (р-ра) = 500 мл = 0,5 л m (NaOH) = 5 г | 1. Вычислим число моль (n) в 5 г NaOH:
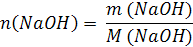 M (NaOH) = 40 г/моль
M (NaOH) = 40 г/моль
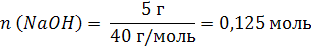 2. Определим молярную концентрацию раствора:
2. Определим молярную концентрацию раствора:
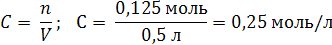
|
| Найти: C(NaOH) | |
| Ответ: Молярная концентрация раствора гидроксида натрия равна 0,25 моль/л. |
2. Вычислить массу хлорида натрия NaCl, содержащегося в растворе объемом 200 мл, если его молярная концентрация 2 моль/л.
| Дано: | Решение: |
| V (р-ра) = 200 мл = 0,2 л C (NaCl) = 2 моль/л | 1. Вычислим число моль NaCl, которое содержится в растворе объемом 0,2 л:
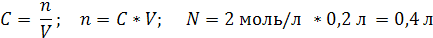 2. Вычислим массу NaCl:
2. Вычислим массу NaCl:
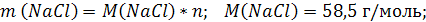
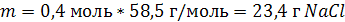
|
| Найти: m( NaCl) | |
| Ответ: m (NaCl) = 23,4 г. |
3. Вычислить молярную концентрацию раствора серной кислоты, если массовая доля H2SO4 в этом растворе 12%. Плотность раствора 1,08 г/мл при 200C.
| Дано: | Решение: |
| ρ (р-ра) = 1,08 г/мл ω (H2SO4) = 12% = 0,12 | 1. Чтобы перейти от массовой доли (%) растворенного вещества к молярной концентрации, надо рассчитать, какую массу имеют 1000 мл раствора:
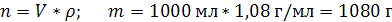 2. Вычислим массу серной кислоты в этом растворе:
2. Вычислим массу серной кислоты в этом растворе:
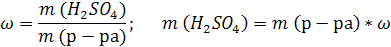 t wx:val="Cambria Math"/><w:i/><w:sz w:val="28"/><w:lang w:val="RU"/></w:rPr><m:t>1080 Рі*0,12=129,6 Рі</m:t></m:r></m:oMath></m:oMathPara></w:p><w:sectPr wsp:rsidR="00000000"><w:pgSz w:w="12240" w:h="15840"/><w:pgMar w:top="1134" w:right="850" w:bottom="1134" w:left="1701" w:header="720" w:footer="720" w:gutter="0"/><w:cols w:space="720"/></w:sectPr></w:body></w:wordDocument>">
t wx:val="Cambria Math"/><w:i/><w:sz w:val="28"/><w:lang w:val="RU"/></w:rPr><m:t>1080 Рі*0,12=129,6 Рі</m:t></m:r></m:oMath></m:oMathPara></w:p><w:sectPr wsp:rsidR="00000000"><w:pgSz w:w="12240" w:h="15840"/><w:pgMar w:top="1134" w:right="850" w:bottom="1134" w:left="1701" w:header="720" w:footer="720" w:gutter="0"/><w:cols w:space="720"/></w:sectPr></w:body></w:wordDocument>"> 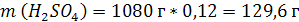 3. Сколько молей содержится в 129,6 г H2SO4?
3. Сколько молей содержится в 129,6 г H2SO4?
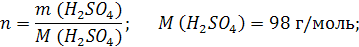
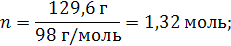
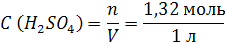
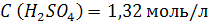
|
| Найти: C (H2SO4) | |
| Ответ: Молярная концентрация раствора серной кислоты с массовой долей H2SO4 12% равна 1,32 моль/л. |
4. Молярность раствора едкого кали KOH равна 3,8 моль/л, его плотность 1,17 г/мл. Вычислить массовую долю (%) KOH в этом растворе.
| Дано: | Решение: |
| C (KOH) = 3,8 моль/л ρ (р-ра) = 1,17 г/мл | 1. Определим количество вещества KOH в 1 л раствора:
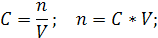
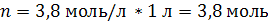 2. Определим массу KOH в 1 л раствора:
2. Определим массу KOH в 1 л раствора:
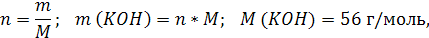
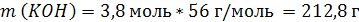 3. Определим массу 1 л (1000 мл) раствора:
3. Определим массу 1 л (1000 мл) раствора:
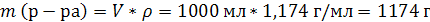 4. Определим массовую долю (%) едкого кали в растворе:
4. Определим массовую долю (%) едкого кали в растворе:
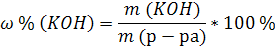
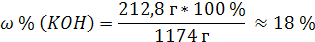
|
| Найти: ω % (KOH) | |
| Ответ: Массовая доля (%) KOH в растворе, молярность которого 3,8 моль/л, равна 18%. |
Дата добавления: 2016-10-17; просмотров: 43143;
