В 190 г воды растворили 10 г сахарозы. Вычислите массовую долю сахарозы в полученном растворе.
| Дано: | Решение: |
| m(сахарозы) = 10,0 m(H2O) = 190,0 | mр-ра = 190,0 + 10,0 = 200,0
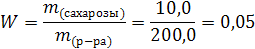
|
| Найти: W (сахарозы) | |
| Ответ: W % (сахарозы) = 0,05 |
2. Какие массы нитрата калия и воды необходимо взять для приготовления 2 кг раствора с массовой долей KNO3, равной 0, 05?
| Дано: | Решение: |
| m(р-ра) = 2 кг = 2000 г W(KNO3) = 0,05 | 1. Определим массу нитрата калия:
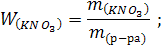
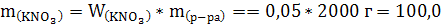 2. Определим массу воды:
2. Определим массу воды:
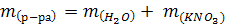
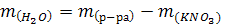
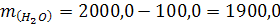
|
| Найти: m(KNO3) m(H2O) | |
| Ответ: m(KNO3) = 100,0 m(H2O) = 1900,0 |
3. К 250,0 10 %-го раствора глюкозы прилили 150 мл воды. Какова массовая доля (%) глюкозы в полученном после прибавления растворе?
| Дано: | Решение: |
| m1(р-ра) = 250,0 W1%(глюкозы) = 10% V(H2O) = 150 мл | 1. Определим массу глюкозы в исходном растворе:
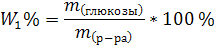
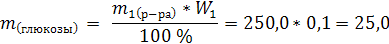 2. Масса глюкозы при разбавлении раствора не изменяется. Определим массу раствора, полученного после разбавления:
2. Масса глюкозы при разбавлении раствора не изменяется. Определим массу раствора, полученного после разбавления:
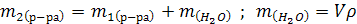
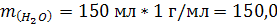
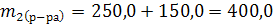 3. Определим W2%(глюкозы):
3. Определим W2%(глюкозы):
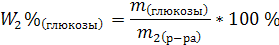
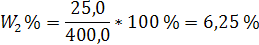
|
| Найти: W2%(глюкозы) | |
| Ответ: W2%(глюкозы) = 6,25 % |
4. При выпаривании 1200,0 20 %-ного раствора соли получили раствор массой 800,0. Какова процентная концентрация полученного раствора?
| Дано: | Решение: |
| m1(р-ра) = 1200,0 W1%(соли) = 20 % m2(р-ра) = 800,0 | 1. Определим массу соли в исходном растворе:
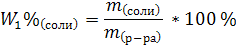
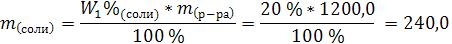 2. Определим процентную концентрацию полученного раствора (масса соли в растворе не изменилась):
2. Определим процентную концентрацию полученного раствора (масса соли в растворе не изменилась):
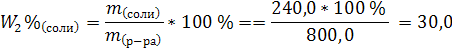
|
| Найти: W2%(соли) | |
| Ответ: W2%(соли) = 30 % | |
5. К 300 мл 20 % раствора серной кислоты (ρ = 1,14 г/мл) прилили 250 мл воды. Определите процентную и молярную концентрацию полученного раствора.
| Дано: | Решение: |
| V1(р-ра) = 300 мл W1%(H2SO4) = 20 % ρ = 1,14 г/мл V2(H2O) = 250 мл ρ (H2O) = 1 г/мл | 1. Масса первого раствора:
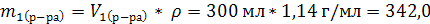 2. Масса H2SO4 в первом растворе равна:
2. Масса H2SO4 в первом растворе равна:
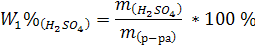
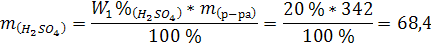 3.
3. 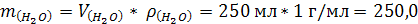 4. Масса вновь получено раствора:
4. Масса вновь получено раствора:
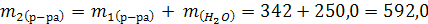 5. Массовая доля H2SO4 во вновь полученном растворе равна:
5. Массовая доля H2SO4 во вновь полученном растворе равна:
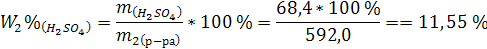
|
| Найти: W2%(H2SO4) C(H2SO4) | |
| Ответ: W2%(H2SO4) = 11,5 % C(H2SO4) = |
Дата добавления: 2016-10-17; просмотров: 8437;
