Опыт 3. Получение оксида меди (II) разложением гидроксида меди(II) и его взаимодействие с кислотой (показательный)
Получить в пробирке голубой осадок гидроксида меди(II) взаимодействием нескольких капель раствора СuSO4 с раствором щелочи NaOH. Осторожно нагреть полученный осадок. Как изменяется цвет? Составить уравнения реакций.
Опыт 4. Получение оксида углерода (IV) разложением малахита [(CuOH)2CO3] и его взаимодействие с водой (показательный)
На дно пробирки поместить небольшое количество измельченного малахита – карбоната гидроксомеди (II). Пробирку закрыть пробкой с газоотводной трубкой и закрепить в штативе в наклонном положении. Газоотводную трубку погрузить в пробирку с дистиллированной водой с 1 каплей индикатора метилоранжа. Пробирку с малахитом нагреть в пламени спиртовки до полного завершения реакции:
- охарактеризовать внешний вид малахита до реакции …………
- по мере его нагревания происходят изменения…………..
- составить уравнение термического разложения карбоната гидроксомеди (II):
to
(CuOH)2CO3 → ….… + ….… + …
- отметить, как изменяется цвет индикатора – метилоранжа в пробирке с дистиллированной водой
- составить уравнение реакции взаимодействия оксида углерода (IV) с водой:
CO2 + H2O 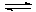 …
…
- составить уравнения диссоциации угольной кислоты:
1 стадия: H2CO3 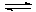 …
…
2 стадия: HCO3- 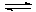 …
…
- составить выражения и привести значения (табл.) констант диссоциации угольной кислоты по первой и второй стадии;
- охарактеризовать кислотно-основные свойства оксида углерода (IV) и угольной кислоты;
- назвать все полученные соединения и ионы, содержащие углерод;
- привести все известные названия оксида углерода (IV).
Вывод
Дата добавления: 2016-09-20; просмотров: 2888;
