Опыт 6. Электролиз водного раствора сульфата меди (II) с активным медным анодом
Поменять местами электроды (опыт 2), вследствие чего анод окажется омеднённым. Снова пропустить электрический ток.
- Отметить, какие изменения происходят на электродах;
- составить уравнения электролитической диссоциации CuSO4 и H2O:
CuSO4 
H2O 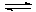
- составить уравнение гидролиза CuSO4 в растворе;
- в растворе CuSO4………………….. среда
- возможные окислители:
- выбрать окислитель, характеризующийся наибольшим значением окислительно-восстановительного потенциала:
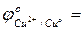 + 0,34 В
+ 0,34 В 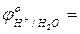 - 0,41 … 0,0 В;
- 0,41 … 0,0 В;
- составить уравнение катодной реакции:
(процесс …………….…);
- возможные восстановители:
- выбрать восстановитель, характеризующийся наименьшим значением окислительно-восстановительного потенциала:
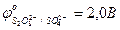
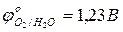 …0,82 В
…0,82 В 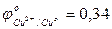 В;
В;
- составить уравнение анодной реакции:
(процесс ……………...);
- составить суммарное уравнение электролиза раствора сульфата меди (II) с активным медным анодом, объединив уравнения катодной и анодной реакций с учетом коэффициентов электронного баланса:
 (ионное уравнение);
(ионное уравнение);
 (молекулярное уравнение);
(молекулярное уравнение);
- ответить, каковы области практического использования электролиза водных растворов солей с активным анодом.
Вывод:
Лабораторная работа №4
на тему: «Химические свойства металлов.
Ряд стандартных окислительно-восстановительных потенциалов (СОВП) металлов»
Цель работы:
- научиться составлять уравнения ОВР, подбирать коэффициенты методом ионно-электронного баланса;
- научиться определять направление протекания ОВР;
- научиться пользоваться рядом стандартных ОВП;
- научиться сравнивать химическую активность металлов.
Краткая теория.
Ряд стандартных ОВП металлов – это последовательность, в которой металлы расположены в порядке ………………… ОВП для электрохимических систем:
Металл является ………………… формой данных электрохимических систем, катион металла - ………………… формой.
Чем меньше значение стандартного ОВП и левее стоит металл в ряду стандартных ОВП, тем ……….......восстановительная способность (химическая активность) металла.
Чем больше значение стандартного ОВП и правее стоит металл в ряду стандартных ОВП, тем …………...восстановительная способность (химическая активность) металла и …………………..окислительная способность катионов металла.
Укажите наиболее активный металл:
а) Ni б) Ag в) Ca г) Fe д) Cu
Металлы, стоящие ………………. водорода в ряду стандартных ОВП металлов, вытесняют молекулярный водород из кислот.
Металлы, стоящие ………………. водорода в ряду стандартных ОВП металлов, не вытесняют молекулярный водород из кислот.
Составьте уравнения возможных реакций:
1) Fe + HCl → 3) Ag + HCl →
2) Sn + HCl → 4) Na + HCl →
Рассчитайте ЭДС для реакций (1-4)
1) ЭДС = 3) ЭДС =
2) ЭДС = 4) ЭДС =
Более активный металл вытесняет …………………..металл, стоящий ……………………..в ряду стандартных ОВП металлов, из раствора его соли.
Составьте уравнения возможных реакций:
5) Sn + MgCl2 → 7) Al + CoCl2 →
6) Fe + CuCl2 → 8) Cu + AgNO3 →
Рассчитайте ЭДС для реакций (5-8)
5) ЭДС = 7) ЭДС =
6) ЭДС = 8) ЭДС =
Дата добавления: 2016-09-20; просмотров: 2434;
