Атомно-абсорбційне визначення міді, цинку та марганцю в соках та водах.
Мета роботи: 1. Ознайомитися з основними складовими частинами методу атомно-абсорбціонної спектроскопії.
2. Проаналізувати фруктові соки, або столові і мінеральні води на домішки важких металів.
1. Загальні відомості
Метод грунтується на вимірюванні абсорбції світла вільними атомами міді (цинку, марганцю), які утворюються при введенні
досліджуванного розчину в полум'я суміші ацетилену з повітрям або пропану з повітрям при довжині хвилі 324,7 нм (213,9 нм; 279,5 нм).
2. Апаратура, реактиви, розчини
Атомно-абсорбційний спектрофотометр;
Лампа з порожнистим мідним (цинковим, марганцевим) катодом;
Ацетилен за ДСТУ 5457-75; Компресор повітряний;
Мідь металева;
Цинк металевий;
Марганець;
Кислота азотна, хч, за ДСТУ 4461-77;
Стандартні розчини з вмістом міді, цинку, марганцю 1 г/л;
Кислота азотна з масовою часткою 1,5 %;
Піпетки на 1,0; 5,0; 10,0 мл;
Мірні колби на 100 мл;
Скляні стаканчики.
Стандартні розчини для атомно-абсорбційних визначень готують, розчинюючи метали або їх солі відомого складу в кислотах або воді. Із концентрованих стандартних розчинів (1 г/л) готують менш концентровані, розводячи аліквоти азотною кислотою з масовою часткою 1,5 %. Цем зберігаємо стандартні розчини довший час, бо підкислення до рН = 1 запобігає гідролізові іонів металів.
Ґрадуювальні розчини
Розчин А: 10 мл розчину, що містить 1 г/л міді (або цинку чи марганцю), переносять у мірну колбу на 100 мл, доводять до мітки дистильованою водою з масовою часткою HNO3 1,5 %, ретельно премішують. Масова концентрація розчину А − 0,1 мг/мл міді (або цинку чи марганцю).
Розчин Б: 1 мл розчину, що містить 1 г/л міді (або цинку чи марганцю), переносять у мірну колбу на 100 мл, доводять до мітки дистильованою водою з масовою часткою HNO3 1,5 %, ретельно перемішують. Масова концентрація розчину Б − 0,01 мг/мл міді (або цинку чи марганцю).
Щоб побудувати ґрадуювальний ґрафік, у 5 мірних колб місткістю 100 мл вносять відповідно 1,3; 3,0; 5,0; 7,0; 10,0 мл розчину Б, доводять до мітки розчином HNO3 з масовою часткою 1,5 %, ретельно перемішують. Масові концентрації цих розчинів відповідно 1.10‑4; 3.10-4; 5.10-4; 7.10-4; 10.10-4 г/л міді (або цинку чи марганцю).
Щоб приготувати розчин з масовою концентрацією іонів металу 30.10-4 г/л, 3 мл розчину А переносять в мірну колбу місткістю 100 мл, доводять до мітки розчином HNO3 з масовою часткою 1,5 %, ретельно перемішують.
Увімкнувши лампу з порожнистим мідним (або цинковим чи марганцевим) катодом на монохроматорі атомно-абсорбційного спектрометра виводять аналітичну лінію міді (цинку, марганцю) 324,7 нм (213,9 нм; 279,5 нм). Вимірюють світлопоглинання стандартних розчинів.
Досліджуванні розчини упарюють зі 100 мл до 10 мл.
Метод ґрадуювального ґрафіка
Вважають, що прилад ґрадуйовано, якщо для нього встановлено функціональний зв'язок між концентрацією аналізованого елемента у стандартних розчинах і показаннями приладу. Прилад ґрадуюють після прогрівання спектрофотометра протягом 30 хв. Стандартні розчини вживають у порядку зросту концентрацій, вводять їх у полум'я і фіксують показання приладу. Ці операції виконують з усіма приготовленими розчинами, по три рази з кожним, і обчислюють середнє арифметичне трьох вимірювань. Рекомендуємо ґрадуювальні вимірювання здійснювати на початку, в середині і в кінці аналізу. За одержаними даними будують ґрадуювальний ґрафік: по осі абсцис відкладають концентрації стандартних розчинів, сі, а по осі ординат – відповідні показання приладу, Аі.
Щоб визначити невідому концентрацію, сх, розчин вводять у атомізатор і після 10-15 с реєструють показання приладу Ах. Його відкладають на осі ординат ґрадуювального ґрафіка, і на осі абсцис знаходять відповідне значення концентрації, сх, яку визначають. Ґрадуювальний ґрафік має проходити через початок координат і, щоб відлік за ним був точнішим, під кутом, близьким до 45 о.
Звичайно, визначаючи концентрації досліджуваного елемента, враховуємо, що розчин упарювали, концентруючи його в 10 разів.
СПЕКТРОФОТОМЕТРІЯ
Спектрофотометричні методи аналізу базуються на законі Бугера, який виражають рівнянням
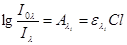 ,(1)
,(1)
де I0,l та Il − інтенсивність регулярного світлового потоку, що падає на зразок і проходить наскрізь відповідно; [I0,l] = [ Il] = лм;
Al − світлопоглинання, сигнал, що вимірюють непрямим способом через відношення фотострумів, пропорційних відповідно інтенсивності світлових потоків (безрозмірна величина); с − концентрація речовини, що поглинає світло, [с] = моль/л, г/л; l − товщина шару, що поглинає світло (внутрішній розмір кювети в напрямкі поширення світла), [l] = см; el − коефіцієнт поглинання, градуювальна характеристика, яка залежить від природи речовини, що поглинає світло і змінює значення при зміні довжини хвилі випромінювання, зміні середовища (розчинника, агрегатного стану тощо).
Якщо одиниця вимірювання [c] = моль/л, то el − молярний коефіцієнт поглинання (МКП) і одиниця вимірювання [el] = л/(моль·см). Застосовують і питомий коефіцієнт поглинання k, з одиницею вимірювання [k] = л/(г·см).
Закон Бугера справджується, якщо:
- промінь монохроматичний і плоско паралельний;
- частинки, що поглинають світло, не взаємодіють між собою і з іншими речовинами, що присутні в системі.
Порушення цих умов, а також різні види взаємодії світла з об’єктами зумовлюють різноманітність причин відхилення від закону Бугера. Їх поділяють на дві групи: інструментальні та фізико-хімічні.
У спектрофотометричному аналізі сигнал вимірюють за умов, коли інструментальні впливи на світлопоглинання постійні й їх можна врахувати або виключити, а фізико-хімічні – малі і ними можна знехтувати.
Дата добавления: 2016-08-07; просмотров: 1406;
