Ускладнення у визначенні областей переважання
Якщо послідовність усіх N ступінчатих констант спадна,
K1 > K2 > . . . > KN,
то у всіх N+1 реаґентів існують області переважання, з межами pL = lg Ki. Якщо ж Ki < Ki+1 (аномальна послідовність), то MLi не має області переважання. Якщо сусідніми є області переважання MLi і MLi+j (j > 1), то
MLi + j L D MLi+j,
lg K = lg bi+j – lg bi = lg Ki+1 + lg Ki+2 + . . . + lg Ki+j, (lg b0 = 0),
і, згідно ЗДМ,
lg ([MLi+j] / [MLi]) = lg K – j pL.
Межа областей переважання, [MLi+j] = [MLi] при pL = (lg K) / j, середньому від логарифмів констант.
Розглянемо приклад – комплекси Ag+ із NH3. Тут lg K1 = 3,31, lg K2 = 3,91, отже послідовність констант є аномальною, K1 < K2. На допоміжній смузі схеми косим штрихом (\\\ або ///) позначено області, де над AgNH3+ переважають інші комплекси. Згідно ЗДМ, [AgNH3+] < [Ag+] при pNH3 > lg K1 = 3,31; [AgNH3+] < [Ag(NH3)2+] при pNH3 < lg K2 = 3,91. Ці області перекриваються,
| Ag(NH3)2+ | Ag+ 0 | 2 | 4 | 6 | pNH3 |
| //////////////////////////////////|χχ|χχ|\\\\\\\\\\\\\\\\\\\\\\\\\\\\\\\\\\\\\\ |
Отже, у проміжному комплексі AgNH3+ немає області переважання. Реагенти з областями переважання взаємно перетворюються за реакцією
Ag+ + 2NH3 D Ag(NH3)2+, lg b2 = lg K1 + lg K2 = 7,22.
Для [Ag+] = [Ag(NH3)2+], як частинний випадок загальної умови, маємо межу областей, pNH3 = (lg b2) / 2 = 3,61.
Алґоритм побудови областей переважання:
1. Знайти межу областей переважання. Для спадної послідовності ступінчатих констант стійкості межі областей дорівнюють lg Ki. Якщо таку послідовність порушено (вона є аномальною), то проміжні комплекси ніде не переважають. Межі комплексів, найближчих за складом до ніде не переважаючих, дорівнюють середньому арифметичному логарифмів констант аномальної послідовності.
2. До комплексу МLі із найменшим числом координованих ліґандів L (і = 0 для вільного М) віднести праву область на осі рL; комплексам із зростаючим числом координованих ліґандів - області, що послідовно розташовані cправа наліво; пропускаємо комплекси, що ніде не переважають.
КЛД для систем із одноядерними комплексами.Для гомоґенних реакцій, змінюючи головну змінну pX = pL (або pH чи pe), міняємо дві залежних змінних – логарифми рівноважних концентрацій двох реагентів, і рівняння прямої вже несправедливе. Наближену асимптоту маємо, приймаючи, що майже весь M перетворився у переважаючий продукт MLi, і одна із залежних змінних є майже постійною, lg [MLі] » lg t(M), де t(M) − загальна концентрація компоненту M. Ґрафік іншої змінної стає лінійним. Наближення тим краще, чим глибше ми у області переважання MLі. У областях для різних MLі асимптоти різні, й наближений ґрафік - ламана.
Розглянемо приклад – кислотно-основні перетворення ацетату, t(HAc) = t = 0,10 моль/л. HAc переважає, якщо pH < lg KН = 4,76. Для [HAc] » t(Ac‑) = t наближеним ґрафіком є lg [HAc] » lg t, горизонтальний промінь від (-¥) до так званої точки системи (ТС), із абсцисою lg KН. Правіше за неї переважає Ac-, [Ac‑] » t = 0,10 моль/л, і, згідно ЗДМ
lg [HAc] = lg KН + lg [Ac-] – pH » lg KН + lg t – pH,
асимптота, промінь униз під кутом 45 о (танґенс ‑1) із ТС – кінця горизонтальної асимптоти. Підставляючи pH = lg KН у рівняння для lg [HAc], одержуємо lg t. Значить, й ця гілка наближеного ґрафіка йде через ТС.
Алґоритм побудови КЛД для систем із одноядерними продуктами. У простих випадках не записуємо реакцій та ЗДМ. Танґенс кута нахилу є різницею стехіометричних індексів при X у формулах частинок – тієї, що відповідає ґрафіку, й переважаючої у відповідній області.
Так, для lg [HAc] у області переважання HAc лінія горизонтальна, а у області переважання Ac- танґенс за абсолютною величиною дорівнює 1 (формули Ac- і HAc відрізняються на 1 H+). Знак танґенса такий, що lg [HAc] зменшується, віддаляючись від області переважання HAc: графік не перевищує горизонтальної асимптоти – максимуму функцій! Зломи замінюють плавними спряженнями. На межі областей, де найбільше порушуються наближення lg [HAc] » lg t або lg [Ac‑] » lg t, речовину з загальною концентрацією t поділено навпіл між НАс та продуктом Ac‑,
[HAc] = [Ac‑] = t / 2, lg [HAc] = lg [Ac-] = lg t – lg 2,
і згладжені ґрафіки перетинаються нижче за ТС на lg 2 » 0,3. Для lg [Ac-] наближений ґрафік – ламана, що складена з асимптот – від ТС до ¥ (горизонтальної) і від – ¥ до ТС (з танґенсом кута нахилу 1).
КЛД, рис. 3, доповнено графіками lg [H+] і lg [OH-]. Пряма lg [H+] йде через початок координат, а lg [OH‑] – через точку (pH = ‑lg Kw, 0). Танґенси їх кутів нахилу відповідно дорівнюють (‑1) й 1.
Там, де більше двох областей переважання, для кожної – інше наближене рівняння, пов’язане з ЗДМ реакції перетворення переважаючого реагенту (скажімо, MLі), у той, ґрафік якого досліджуємо (скажімо MLk),
MLi + (k - i) L D MLk, lg bk – lg bi.
lg [MLk] = (lg bk – lg bi) + lg [MLi] + (i – k) pL »
» (lg bk – lg bi) + lg t(M) + (i – k) pL .
Щоб координати точок перетину відрізків не знаходити з рівнянь, зауважимо, що функція неперервна, а ґрафік наближеної функції – ламана зі зломами на межах областей переважання. Графік почнемо із горизонтального відрізка між ТС і продовжимо похилими відрізками в інші області переважання. Отже, алґоритм побудови КЛД:
Обчислити значення головної змінної pL на межах областей переважання окремих частинок.
Нанести на діаґраму точки системи (ТС) з абсцисами, що обчислені на кроці 1, і ординатою lg t(M).
Почати наближений ґрафік lg [MLk] із відрізка, кінці якого у ТС на межах області переважання MLk, а для частинки, що не має області переважання – у ТС на межах областей переважання частинок, найближчих за складом до розгляданої.
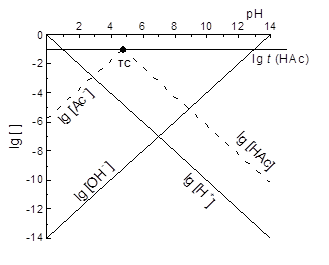
| a |
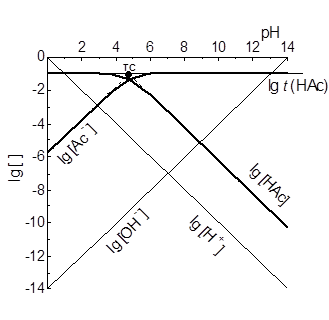
| b |
Рис. 3. КЛД для кислотно-основних перетворень ацетату, t(HAc) = t = 0,10 моль/л: (а) ескіз перед побудовою спряжень; (б) КЛД.
Продовжити ґрафік lg [MLk] ламаною у область переважання MLі. Танґенс кута нахилу відрізків ламаної дорівнює (i – k), різниці стехіометричних індексів при L для частинки MLі, що переважає у відповідній області, та MLk. Кінці відрізка – на межах областей (під ТС).
Якщо точність ґрафіків у околі ТС недостатня для аналізованої проблеми, то замінити зломи плавними спряженнями, точка перетину яких відхиляється на D = ‑ lg j за ординатою від зламу, де j – число сортів частинок, концентрації яких великі й майже рівні у ТС.
Алґоритм зручніший, ніж для гетероґенних систем. Лише за ступінчатими константами відтворюємо (навіть в уяві!) ґрафіки для найбільших концентрацій – горизонтальні відрізки та похилі, що безпосередньо від них відходять.
Щоб вирішити більшість проблем, потрібно розглядати лише декілька найбільших концентрацій, інформація про які міститься у верхній частині КДД, а подробиці поведінки ґрафіків біля ТС неістотні. Часто достатньо горизонтальних і перших похилих відрізків, без 5-го кроку.
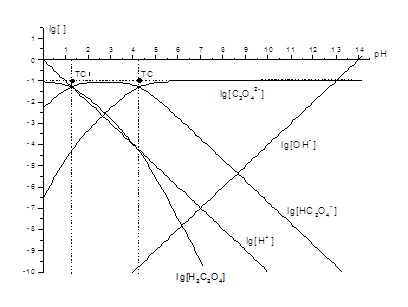
Рис. 4. КЛД для кислотно-основних перетворень оксалату, t(H2С2О4) = t = 0,10 моль/л.
Розглянемо КЛД для Н2С2О4, t(Н2С2О4) = t = 0,10 моль/л, головна змінна pH. Для продуктів приєднання іону Н+ до іона С2О42‑: lg KH1 = 4,266, lg KH2 = 1,256 [I = 0]. Це рН на межах областей переважання (крок 1). На кроці 2 наносимо ТС із координатами (1,3, ‑1) та (4,3, ‑1), ордината lg t = ‑1. На кроці 3 будуємо наближені ґрафіки. Ґрафік lg [Н2С2О4] починаємо з горизонтального променя на висоті –1, від ‑ ¥ до лівої ТС, ґрафік lg [НС2О4‑] – із відрізка між обома ТС, а lg [С2О42‑] – із променя від правої ТС на + ¥. На кроці 4 ґрафік lg [Н2С2О4] продовжуємо праворуч (де переважає іон НС2О4‑, що відрізняється від Н2С2О4 на іон Н+) відрізком із танґенсом кута нахилу (‑1). Напрям ухилу є очевидним, бо ґрафік порівняно з горизонтальним відрізком може лише спадати. Після правої ТС, де переважає С2О42‑, ґрафік продовжуємо променем із танґенсом кута нахилу (‑2). Аналоґічно будуємо похилі ділянки ґрафіків lg [НС2О4‑] та lg [С2О42‑], тільки тут вже наявні ділянки зростання функцій. На кроці 5 спрягаємо всі зломи (рис. 4).
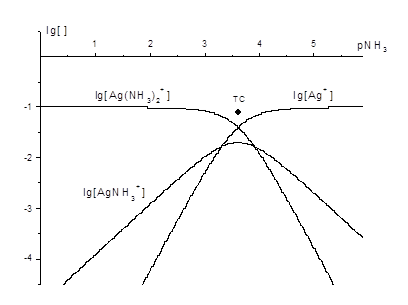
Рис. 5. КЛД для комплексів Ag+ із NH3, головна змінна pNH3, t(Ag+) = t = 0,10 моль/л.
На КЛД для t(Ag+) = t = 0,10 моль/л, головна змінна pNH3, області переважання мають Ag+ та Ag(NH3)2+. Горизонтальні відрізки наближених ґрафіків lg [Ag+] та lg [Ag(NH3)2+] переходять у похилі з танґенсами ± 2, бо переважаючі комплекси, відокремлені межею, pNH3 = (lg b2) / 2 = 3,61, відрізняються на 2 ліґанди NH3. Асимптоти перетинають горизонтальну лінію lg [] = lg t у точках із абсцисами – логарифмами ступінчатих констант. Для AgNH3+ ці точки не співпадають з ТС. Приймимо
lg K1 » lg K2 » (lg b2) / 2,
бо ступінчаті константи дуже близькі, й проведемо асимптоти графіка lg [AgNH3+] через ту саму ТС двома променями з танґенсами ± 1. У ТС
lg [Ag+] = lg [Ag(NH3)2+] » lg [AgNH3+] » lg (t / 3) = ‑ 1,5
й спряження проводимо на lg 3 » 0,5 нижче за ТС.
Дата добавления: 2016-08-07; просмотров: 749;
