ТЕРМОДИНАМІКА ХІМІЧНОЇ РІВНОВАГИ. КОНСТАНТА ХІМІЧНОЇ РІВНОВАГИ. ЗАКОН ДІЮЧИХ МАС.
Хімічною рівновагоюназивається такий стан оборотного процесу
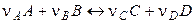 ,
,
при якому швидкість прямої реакції (  ) дорівнює швидкості зворотної (
) дорівнює швидкості зворотної (  ) реакції, і внаслідок цього сполукасистеми згодом не змінюється. Рівновага встановлюється не тому, що процес припинився, а в результаті протікання процесу у двох напрямках з однаковою швидкістю, тобто рівновага має динамічний характер. Крім того, стійкі рівновага характеризуються: незмінністю рівноважного стану системи при збереженні зовнішніх умов; можливістю підходу до стану рівноваги із двох протилежних сторін; рухливістю рівноваги.
) реакції, і внаслідок цього сполукасистеми згодом не змінюється. Рівновага встановлюється не тому, що процес припинився, а в результаті протікання процесу у двох напрямках з однаковою швидкістю, тобто рівновага має динамічний характер. Крім того, стійкі рівновага характеризуються: незмінністю рівноважного стану системи при збереженні зовнішніх умов; можливістю підходу до стану рівноваги із двох протилежних сторін; рухливістю рівноваги.
По основному постулаті кінетики швидкості прямого й зворотного процесів виражаються в такий спосіб:
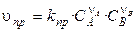 , (1)
, (1)
 , (2)
, (2)
т.ч. швидкість хімічної реакції прямо пропорційна концентрації реагуючих речовин, зведених у ступені, які дорівнюють їх стехіометричним коефициентам.
kпр і kобр — константи швидкості прямій і зворотної реакцій.
У рівновазі:
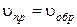 , (3)
, (3)
 . (4)
. (4)
Константи швидкості прямій і зворотної реакцій не залежать від концентрацій і при постійній температурі є постійними величинами. Тому їхнє відношення є деяка постійна величина КС -константа хімічної рівноваги:
 , (5)
, (5)
Дата добавления: 2016-06-02; просмотров: 859;
