Експериментальна частина. В конічну колбу на 250 мл наливають піпеткою або мірною колбою 50 мл досліджуваної води, додають 1-2 краплі розчину індикатора метилового червоного і
В конічну колбу на 250 мл наливають піпеткою або мірною колбою 50 мл досліджуваної води, додають 1-2 краплі розчину індикатора метилового червоного і підкиснюють 0,1н. розчином хлоридної кислоти. Розчин кип'ятять 3-5 хвилин для видалення карбонатної кислоти. До киплячого розчину додають 1 мл розчину барій хлориду, який містить йони Mg2+, і кип’ятять ще 10-15 секунд. Присутність в розчині йонів Mg2+ є необхідним для чіткого визначення кінця титрування.
Частина йонів Ва2+ витрачається на зв’язування йонів SO42- в барій сульфат, а частина залишається в розчині. Через 10-15 хвилин досліджувану воду нейтралізують 0,1н. розчином лугу NaOH. Додають його обережно краплями до переходу червоного забарвлення в жовте. Потім додають 5 мл амоніачного буферного розчину (NH4ОН + NH4Cl), декілька крапель індикатора еріохрому чорного Т і титрують 0,05 н. розчином трилону Б (VЗ). В окремій пробі визначають об’єм розчину трилону Б (V1), який необхідний для титрування одного мл розчину барій хлориду, що містить йони Mg2+. Для цього в мірну колбу на 50 мл наливають 1 мл цього розчину і доливають до мітки дистильовану воду. Вміст колби виливають в конічну колбу ємністю 250 мл, додають 5 мл амоніачного буферу, 6-7 крапель індикатора еріохрому чорного Т і титрують 0,05н. розчином трилону Б до зміни забарвлення на синє.
В другій окремій пробі досліджуваної води (50 мл) визначають об’єм розчину трилону Б(V2), який необхідний для титрування йонів Са2+ і Mg2+ (лаб.роб.№6). Вміст йонів SO42- визначають за формулою
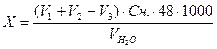 (мг/л),
(мг/л),
де Сн.– молярна концентрація еквівалента (нормальна концентрація ) трилону Б; 48 – Ме йону SO42-; V – об’єм досліджуваної води.
Результати звести в таблицю:
| V1, мл | V2, мл | V3, мл | Сн. | 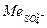
| Х, мг/л |
Запитання для самоконтролю
1. До якої категорії належать сульфат-йони в природних водах?
2. В яких водах вони переважають?
3. Присутність яких йонів лімітує вміст сульфат-йонів в природних водах?
4. В чому полягає сутність сульфаторедукції в природних водах?
5. В чому полягає сутність комплексонометричного методу визначення сульфатів в природних водах?
Дата добавления: 2016-05-16; просмотров: 905;
