Хімічні методи очистки забруднених газів. Очистка відпрацьованих газів від двоокису сірки ароматичними амінами
Хімічні методи очищення викидних газів засновані на хімічному зв'язуванні шкідливих забруднювальних речовин. Дуже поширеним методом є хемосорбція, коли очищуваний газ промивають розчином речовин, що реагують із забруднюючими домішками. Так, для вловлювання оксидів нітрогену застосовують торфолужні композиції з гідроксидом кальцію або аміаком. У результаті хемосорбції утворюється добриво з 6—8 %-м вмістом зв'язаного азоту у вигляді нітратів кальцію і амонію.
При хемосорбції компонент, що абсорбується, вступає в хімічну реакцію з поглиначем, утворюючи нові хімічні сполуки в рідкій фазі. Можливе протікання оборотної і необоротної реакцій. І в тому і в іншому випадках рівноважний парціальний тиск витягуваного компонента значно нижче в порівнянні з фізичною абсорбцією, тому хемосорбционні процеси, за інших рівних умов забезпечують більш повне витягання компонентів з газових сумішей. Регенерацію поглинаючих розчинів, що отримуються при протіканні оборотних хемосорбционних процесів, проводять тим же методом, що і при фізичній сорбції. Регенерацію поглинаючих розчинів, що отримуються в необоротних хемосорбционних процесах, здійснюють хімічними методами. До процесів хімічної абсорбції в азотній промисловості відносяться моноетаноламіновая очищення від СО2, мідноаміачне очищення від СО, аміачний і марганцевий метод очищення від двоокису сірки, метанірування СО і СО2 з газів, що відходять, із здобуттям метану, содові і аміачний - карбонатні методи уловлювання з'єднань фтору у виробництві фосфорних добрив із здобуттям фторидів. Більшість реакцій, що протікають при очищенні, є екзотермічними і оборотними, тому при підвищенні температури розчину хімічна сполука, що утворюється, розкладається з виділенням вихідних компонентів. Поглинаюча здатність розчину значною мірою залежить від константи рівноваги хімічної реакції. На відміну від фізичної абсорбції теплота розчинення при хемосорбції велика, відповідно розчинність сильно залежить від температури. Чим менше концентрація розчиненого газу, тим більше молярна теплота розчинення, тому при малих концентраціях газу в регенерованих розчинниках тиск над розчином різко зменшується з пониженням температури. Це дозволяє досягти тоншого очищення, ніж при фізичній абсорбції, отже, при тонкому очищенню хемосорбція ефективніша. Для абсорбції SО2 з газів кольорової металургії [концентрація SО2 в газі 1-2 % (о.)], що відходять, застосовують розчини ксилідину або діметіланіліну. У одному з розроблених процесів сульфідіновим абсорбентом є суміш (1 : 1) ксилідину і води. Ксилідин і вода зазвичай не змішуються, але при взаємодії SО2 з ксилідином утворюється деяка кількість ксилідінсульфата розчинного у воді:
2С6Н3(СН3)2NH2 + SO2 → 2C6H3(CH3)2NH2SO2 (5.123)
При концентрації SО2 100 кг/м3 суміш ставати гомогенною. Схема очищення газу від SО2 сумішшю ксилідин–вода приведена на рисунку 5.55. Після видалення пилу, газ з вмістом 0,5-8 % SО2 абсорбується в двох абсорберах. Концентрація SО2 після абсорбції знижується до 0,05-0,1 %. Пари ксилідину, що відносяться з абсорберів, рекуперують розбавленою сірчаною кислотою (5-10 %) в промивній колоні. Після цього газ видаляють в атмосферу. Насичений абсорбент з вмістом 130-180 г/дм3 SО2 і доданим розчином соди насосами подає у відпарну колону, в якій він нагрівається до 100 0С з глухою парою. Десорбований диоксид сірки з невеликим вмістом ксилідину промивають водою в колоні і направляють на подальшу переробку. При низькій концентрації SО2 в газі процес стає неекономічним унаслідок втрат ксилідину.

Рисунок 5.55 – Схема установки очищення газу від диоксиду сірки сумішшю ксилідин–вода: 1,2 – абсорбент; 3,4 – ємкості; 5 – холодильник; 6 – промивна колона газів, що відходять; 7 – відпарна колона; 8 – сепаратор; 9 – колона для промивання диоксиду сірки.
Для концентрації SО2 в газах, що відходять, вище 35 % (об.) диметиланілін є ефективнішим абсорбентом, ніж суміш ксилідин–вода. Спочатку газ очищають від твердих домішок в електрофільтрах. Потім після абсорбції промивають розчином карбонату натрію для видалення слідів SО2 і диметиланіліну, а потім розбавленою сірчаною кислотою, яка абсорбують сліди диметиланіліну. Видалення SО2 проводять у відпарній колоні. Після осушення SО2 переробляють в сірчану кислоту. Абсорбери і відпарна колона як контактні елементи забезпечені колпачковими тарілками. На 1 кг виділеного в цьому процесі диоксиду сірки витрачається 0,5 диметиланіліну, 16 г соди, 18 г сірчаної кислоти, а також 1,1 кг пари, 0,52 МДж енергії і 8,2 кг/годину води, що охолоджує. Апаратура. Для проведення процесів абсорбції диоксиду сірки використовують різні по конструкції абсорбери. Вони повинні задовольняти наступним вимогам: мати високі ефективність і пропускну спроможність по газу, низький гідравлічний опір (до 3 кПа), бути простими по конструкції і зручними в експлуатації, відрізнятися низькою металоємністю, не забиватися осіданнями що утворюються в процесі абсорбції. На практиці більш всього використовують порожнисті абсорбери з форсунками і скрубери Вентурі, одноступінчаті і двоступінчаті. Вдосконалення їх конструкцій йде по шляху створення апаратів з мінімальною внутрішньою поверхнею Високою ефективністю і простій в експлуатації володіє абсорбер типа СМ (рисунок 5.56), що поєднує порожнисту секцію з форсунками і секцію з барботажними тарілками. Досліджуються також абсорбери з рухливою кульовою насадкою з поліетилену або гуми. Перспективними є і абсорбери з крупнодирчатими тарілками.
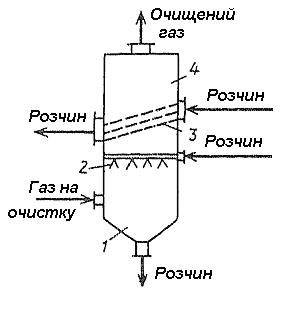
Рисунок 5.56 – Абсорбер типу СМ:
1 – секція очистки газа; 2 – форсунка; 3 – контактні тарелки; 4 – секція бризговидалення.
Дата добавления: 2016-03-27; просмотров: 1241;
