Клинические проявления
Симптоматика сахарного диабета у больных варьирует. Чаще всего они обращаются к врачу по поводу нарушений, связанных с гипергликемией (полиурия, полидипсия, полифагия), но первым сигналом может быть и острая декомпенсация метаболизма, приводящая к диабетической коме. Иногда вначале проявляются дегенеративные осложнения, такие как нейропатия, а симптомы гипергликемии отсутствуют. Нарушения метаболизма обусловлены относительной или абсолютной недостаточностью инсулина и относительным или абсолютным избытком глюкагона. Обычно к декомпенсации метаболизма приводит именно повышение молярного отношения глюкагон/инсулин. Это отношение может меняться вследствие как снижения уровня инсулина, так и возрастания концентрации глюкагона отдельно или вместе. Теоретически тот же эффект должно было бы давать изменение биологической реакции на любой из этих гормонов. Так, инсулинорезистентность могла бы вызывать метаболические эффекты, свойственные возрастанию отношения глюкагон/инсулин, хотя бы это отношение, рассчитанное по результатам радиоиммунологического определения обоих гормонов в плазме, и не было бы значительно изменено или даже оказывалось бы сниженным (если глюкагон биологически активен, а инсулин относительно неактивен). Связь между метаболическими нарушениями и дегенеративными осложнениями обсуждается ниже. В типичных случаях клинические проявления ИЗСД и ИНЗСД различны (табл. 327-3).
Инсулинзависимый диабет. Инсулинзависимый диабет возникает, как правило, в возрасте до 40 лет. В США наиболее часто заболевают лица в возрасте около 14 лет. Болезнь протекает остро. Жажда, чрезмерное мочеотделение, повышенный аппетит проявляются в течение нескольких дней, резко снижается масса тела. У некоторых больных наблюдается кетоацидоз, возникающий во время интеркуррентного заболевания или после хирургической операции. Больные диабетом I типа могут иметь нормальную массу тела или быть истощенными в зависимости от интервала времени между появлением симптомов и началом лечения (см. табл. 327-3). В характерных случаях уровень инсулина в плазме низок или вообще не определяется. Уровень глюкагона повышен, но под действием инсулина снижается. После появления симптомов необходима терапия инсулином. Иногда начальный эпизод кетоацидоза сменяется бессимптомным периодом (период «медового месяца»), когда лечения не требуется. Вероятное объяснение этого феномена дано на рис. 327-2.
Инсулиннезависимый диабет. Заболевание поражает обычно лиц среднего или пожилого возраста. В типичном случае больной страдает ожирением. Симптомы развиваются
Таблица 327-3. Общая характеристика ИЗСД и ИНЗСД
| Характеристика | ИЗСД | ИНЗСД |
| Генетический локус | 6-я хромосома | 11-я хромосома (?) |
| Возраст больного в начале болезни | Менее 40 лет | Более 40 лет |
| Телосложение | От нормального до истощенного | Ожирение |
| Инсулин в плазме | От низкого уровня до полного отсутствия | От нормального до высокого |
| Глюкагон в плазме | Высокий уровень, подавляемый | Высокий уровень, неподавляемый |
| Острые осложнения | Кетоацидоз | Гиперосмолярная кома |
| Инсулинотерапия | Эффективна | Эффективна или неэффективна |
| Лечение препаратами сульфонилмочевины | Неэффективно | Эффективно |
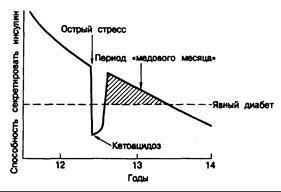
Рис. 327-2. Схематические изображение периода «медового месяца».
На рисунке показана постепенно снижающаяся способность к секреции инсулина у человека, который вскоре заболеет диабетом. В возрасте около 13,5 лет инсулина стало недостаточно, чтобы удерживать уровень глюкозы в плазме крови в нормальных пределах. В 12-летнем возрасте возник эпизод кетоацидоза, например, в связи с острым аппендицитом. По-видимому, вызванный стрессом выброс адреналина блокировал секрецию инсулина и вызвал этот синдром. У здорового человека запас инсулина таков, что обеспечивает адекватную секрецию инсулина, несмотря на стресс. После того, как стрессовое состояние было ликвидировано, способность секретировать инсулин возвратилась к исходному уровню и оставалась на достаточном уровне еще в течение 1 года, что изображено заштрихованной областью. Это и есть период «медового месяца».
медленнее, чем при ИЗСД, и диагноз часто ставят по повышенному уровню глюкозы, обнаруженному при лабораторном исследовании, у лица, не предъявляющего никаких жалоб. В отличие от инсулинзависимого диабета уровень инсулина в плазме в абсолютных единицах нормальный или повышен, хотя и ниже того, которого следовало бы ожидать, исходя из концентрации глюкозы в плазме, т. е. имеется относительная инсулиновая недостаточность. Иначе говоря, у здоровых людей при повышении содержания глюкозы в плазме до диабетического уровня концентрация инсулина должна была бы быть выше. Это свидетельствует об упомянутом ранее дефекте секреции инсулина при ИНЗСД. Метаболизм глюкагона при инсулиннезависимом диабете подчиняется сложным закономерностям. Хотя его повышенная концентрация в плазме натощак и может снижаться под влиянием больших доз инсулина, усиленная реакция глюкагона на пищевые вещества оказывается неподавляемой, т. е. функция a-клеток нарушается. По неизвестным причинам у больных инсулиннезависимым диабетом кетоацидоз не развивается. При декомпенсации они впадают в гиперосмолярную некетозную кому. Одна из гипотез, объясняющих отсутствие кетоацидоза при стрессе, заключается в том, что печень таких больных резистентна к глюкагону и уровень малонил-КоА остается высоким, ингибируя окисление жирных кислот по кетогенному пути (см. ниже). Если удается снизить массу тела, больным не требуется иного лечения, кроме диетотерапии. Большинство больных, которым диетотерапии недостаточно, реагируют на препараты сульфонилмочевины, но у многих из них гипергликемия и в этом случае снижается в меньшей степени, чем нужно для компенсации диабета. Именно поэтому многие больные с ИНЗСД получают инсулин.
Лечение
Диета. Вначале оценивают суточную потребность в количестве калорий, исходя из идеальной массы тела (определяемой по таблицам страхования жизни). На основании этого рассчитывают необходимые количества углеводов, жиров и белка и составляют диету с учетом системы эквивалентов, разработанной Американской Диабетологической Ассоциацией. Рекомендации Совета по пищевым продуктам и питанию для взрослых лиц со средней физической активностью с возрастом уменьшаются и колеблются от 42 ккал/кг массы тела для 18-летних юношей до 33 ккал/кг для 75-летних женщин. Как правило, следует потреблять несколько меньшее количество калорий, чем указано в официальных рекомендациях: мужчинам целесообразно начинать с 36 ккал/кг, женщинам с 34 ккал/кг. Но иногда для достижения желаемой массы тела может потребоваться некоторое увеличение или уменьшение этих показателей.
Минимальная потребность в белке при хорошем питании составляет примерно 0,9 г/кг массы тела в день. Рекомендуемое содержание углеводов — 40—60% от общей калорийности диеты, но в отдельных случаях оно может быть увеличено до 85%. К белково-углеводной пище добавляют достаточное количество жиров, чтобы довести потребление калорий до желаемого уровня. Хотя из диеты больных диабетом сахарозу обычно исключают, но ряд исследований свидетельствует о том, что при умеренном потреблении сахара гипергликемия после еды не усиливается. В настоящее время большинство диет для больных диабетом предусматривает включение полиненасыщенных жиров в качестве противоатерогенного средства. Часто также рекомендуют увеличить содержание пищевых волокон.
После принятия решения относительно необходимого потребления калорий и их распределения между жирами, белками и углеводами составляют диету с указанием конкретных эквивалентов (табл. 327-4)'. Например, диета в 2200 ккал, в которой 50% калорийности составляют углеводы, а количество белка равно 1—1,5 г/кг массы тела, может включать 2 молочных, 7 фруктовых, 12 хлебных, 8 мясных, 4 жировых эквивалента и неограниченное количество овощей типа А (табл. 327-5). На практике обычно используют предварительно рассчитанные диеты с определенным содержанием калорий, которые составлены Американской Диабетологической Ассоциацией. Особое внимание следует уделять тем продуктам, которые больной любит и которые ему доступны. Продукты целесообразно сначала взвесить и измерить. Диету для больных диабетом устанавливают надолго, поэтому необходимо учитывать все ее стороны. Однако разовые или двухразовые нарушения в приеме пищи возможны. Так, больным диабетом подросткам можно в качестве особого поощрения разрешить съесть обычно запрещаемый десерт, но они должны понимать, что завтра необходимо будет вернуться к диете. Даже у взрослых методика «поощрения» часто обеспечивает лучшее соблюдение диеты, чем более жесткие требования. В идеальном случае больные должны пройти обучение у диетологов по определенной программе. Такие уроки можно организовать в крупных лечебных учреждениях. Если больной живет в небольшом селении, ему, вероятно, следует пройти начальное обучение в более крупном центре.
Для больных диабетом, получающих инсулин, также важно распределять калории, чтобы исключить гипогликемию. Типичная схема могла бы быть следующей: 20% от общей калорийности на завтрак, 35% — на ленч, 30% — на обед и 15% — на ужин. Иногда оказывается необходимым и полдник. При разном образе жизни необходимо по-разному распределять калории в течение дня: так, человек, работающий по вечерам или ночью, должен изменить время максимального приема пищи.
Определение реальных реакций гликемии на потребление пищи поставило под сомнение традиционный подход к диетотерапии. В настоящее время установлено, что продукты одного веса и содержащие одинаковое количество жиров, углеводов или белков могут обусловливать разный прирост глюкозы в плазме после еды. Для отражения этих различий введено понятий «гликемический индекс». При расчете гликемического индекса определяют средний уровень глюкозы в плазме на 2—3-часовой период после приема данного продукта и сравнивают этот уровень с таковым после приема стандартной пищи известного состава, например хлеба. В принципе такой подход оправдан, поскольку он дает представление о реальной реакции гликемии на пищевые продукты. Однако применять его ко всем больным диабетом пока нельзя. Нужно проверить продукты и их возможные сочетания, прежде чем диеты, основанные на гликемических индексах, удастся сравнить с диетами, основанными на стандартных эквивалентах, в обычных условиях.
Значение диеты при лечении больных зависит от типа заболевания. У больных, нуждающихся в инсулине, особенно у тех, кто находится на интенсивном инсулиновом режиме, состав диеты не играет решающей роли, так как инсулинотерапию можно «подстроить» под широкие колебания рациона. Больные инсулиннезависимым диабетом, не получающие экзогенного инсулина, должны более строго придерживаться назначенной диеты, поскольку эндогенные резервы инсулина у них ограничены. Такие больные могут реагировать на возросшие потребности, создаваемые избытком калорий или большим потреблением легко всасывающихся углеводов. Таким образом, у лиц с инсулиннезависимым диабетом диета имеет первостепенное значение.
Таблица 327-4. Состав пищевых эквивалентов1
| Эквивалент | Калории | Углеводы, г | Жиры, г | Белок, г |
| Молоко | ||||
| Овощи2 | — | |||
| Фрукты | — | — | ||
| Хлеб | 703 | — | ||
| Мясо | 753 | — | ||
| Жир | — | — |
1 Приведен состав одного эквивалента.
2 Овощи типа А содержат мало углеводов, жиров или белка, и их можно есть в любом количестве. Приведены эквиваленты дня овощей типа Б.
3 Расчетная цифра для эквивалента хлеба—68 кал, а для эквивалента мяса—73 кал, исходя из 4 ккал/г для углеводов и белка и 9 ккал/г для жира. Цифры 70 и 75 кал привены для облегчения расчетов.
Таблица 327-5. Диета для больных диабетом, рассчитанная на 2200 кал (50 % углеводов)
| Эквивалент | Количество | Калории | Углеводы, г | Жир, г | Белок, г |
| Молоко | |||||
| Овощи1 | Потребление овощей типа А не ограничено | ||||
| Фрукты | — | — | |||
| Хлеб | — | ||||
| Молоко | — | ||||
| Жир | — | — | |||
| Всего. . . | |||||
| (50%) | (33%) | (17%) |
1 К овощам типа Б относятся свекла, морковь, лук, зеленый горошек, тыква, брюква, кабачки и репа. По желанию полчашки—чашку можно заменить на один фруктовый эквивалент. Потребление всех других распространенных овощей не ограничивается.
Инсулин. Инсулин необходим всем больным диабетом I типа и многим больным с инсулиннезависимым диабетом. Если врач не назначает лекарственные препараты перорально (см. ниже), то все больные с ИНЗСД, не реагирующие на диетотерапию, должны получать инсулин. Контролировать симптомы диабета с помощью инсулина очень легко, но даже при проведении множественных инъекций обычного инсулина или использовании инфузионных насосов трудно поддерживать нормальный уровень сахара крови круглосуточно. Еще труднее сделать это с помощью традиционной инсулинотерапии, предполагающей одну или две инъекции гормона в сутки. У здорового человека концентрация глюкозы в плазме постоянно сохраняется в узких пределах, несмотря на эпизодический характер приема пищи. Во время еды секреция инсулина быстро возрастает, и всасываемые углеводы быстро поступают в печень и другие ткани. В результате даже после еды содержание глюкозы в плазме у здорового человека не достигает гипергликемического или глюкозурического уровня. По мере того как концентрация глюкозы под действием инсулина падает, секреция гормона тормозится и в кровь выделяются контррегуляторные гормоны, предупреждающие возникновение гипогликемии. Так, обеспечивается плавная регуляция уровня глюкозы в плазме в ходе всего процесса всасывания пищи. У больных диабетом, получающих инъекции инсулина, эти физиологические реакции не воспроизводятся. Если вводить такое количество инсулина, которое будет достаточно для сохранения нормального уровня глюкозы после еды, то по завершении процесса всасывания количество инсулина окажется слишком большим и возникнет гипогликемия. Та же проблема существует и при использовании инфузионных насосов или множественных инъекций инсулина с целью жесткого контроля за течением диабета.
Несмотря на эти трудности, интенсивную инсулинотерапию рекомендуют часто, поскольку считается, что при поддержании нормальной или почти нормальной концентрации глюкозы в плазме в течение суток можно предотвратить или частично снять некоторые возникающие осложнения. Существ уют три режима инсулинотерапии: обычный, множественные подкожные инъекции (МПИ) и постоянная подкожная инфузия инсулина (ППИИ). Обычная инсулинотерапия предполагает одну или две инъекции в сутки инсулина промежуточного действия, такого как цинк-инсулин (инсулин ленте) или инсулин-изофан (NPH-инсулин) с добавлением небольших количеств обычного инсулина или без него. Если при постановке диагноза у больного нет других остро протекающих заболеваний, лечение можно начинать амбулаторно, обеспечив пациента инструкциями в отношении диеты, применения инсулина и оценки своего состояния, причем должна быть возможность телефонной консультации у врача. Лечение взрослых больных с нормальной массой тела можно начинать с дозы 15—20 ЕД в сутки (рассчитанная скорость продукции инсулина у лиц с нормальной массой тела без диабета составляет примерно 25 ЕД в сутки). При ожирении из-за инсулинорезистентности лечение можно начинать с 25—30 ЕД в сутки. Целесообразно в течение нескольких суток не менять дозу инсулина. Исключение составляют случаи гипогликемии, когда дозу инсулина необходимо немедленно снизить, если только гипогликемия не носит случайного характера (например, чрезмерная физическая нагрузка). Как правило, при каждой смене дозы инсулина ее нельзя менять больше чем на 5—10 ЕД. Однократная инъекция инсулина в сутки, вероятно, бывает достаточной только у тех больных, у которых сохранилась остаточная способность к секреции инсулина. Если контролировать состояние больного не удается, дозу нужно дробить: примерно 2/3 общего количества инсулина вводить перед завтраком, а остальное — перед ужином. При общей дозе инсулина 50—60 ЕД в сутки почти всегда показаны две инъекции, но и при меньшей общей дозе предпочтительнее две инъекции, так как срок максимального действия промежуточных инсулинов, по-видимому, зависит от дозы т. е. в малой дозе максимальная активность инсулина проявляется быстрее, но и снижается раньше, чем в большой. Многие врачи даже в начале лечения добавляют обычный инсулин к препарату промежуточного действия. Таким образом, если схема лечения предполагает однократную дозу, можно начинать с 20 ЕД инсулина промежуточного действия и 5 ЕД обычного инсулина, а не с 25 ЕД только препарата промежуточного действия. Это обосновано тем, что обычный инсулин быстро снижает уровень глюкозы в плазме, после чего медленнее всасывающийся инсулин лишь поддерживает сниженный уровень. Большинство больных, находящихся на двух инъекциях инсулина в сутки, также получают смесь инсулинов обычного и промежуточного действия, например 25 ЕД NPH плюс 10 ЕД обычного инсулина перед завтраком и 10 NPH плюс 5 ЕД обычного инсулина перед ужином. Все больные должны помнить о необходимости снижать дозу инсулина перед дополнительной физической активностью или работой. Степень такого снижения определяют методом проб и ошибок, хотя для начала целесообразно уменьшить дозу на 5—10 ЕД. Снижение уровня глюкозы в крови при физической нагрузке обусловлено главным образом ростом энергопотребностей ранее не сокращавшихся мышц. Более быстрое всасывание инсулина из мест введения играет меньшую роль. И наоборот, перед приемом пищи, содержащей дополнительные калории, или потреблением обычно исключаемых из диеты продуктов (например, когда больной диабетом должен быть на банкете или когда подросток позволяет себе лакомство) следует дополнительно вводить некоторое количество обычного инсулина. Больным, желающим самостоятельно контролировать уровень глюкозы в плазме, можно предложить алгоритм изменения режима инсулинотерапии. Такого рода протокол приведен в табл. 327-6. Больных, которым трудно контролировать свое состояние, нужно поместить в стационар, где с
Таблица 327-6. «Подстройка» доз инсулина при обычной инсулинотерапии1
| Уровень сахара в крови, мг% | Обычный инсулин, ЕД (смешивать с дозой инсулина промежуточного действия) | |
| завтрак | ужин | |
| 51—100 | ||
| 101—150 | ||
| 151—200 | ||
| 201—250 | ||
| 251—300 | ||
| Выше 300 |
1Если уровень сахара в крови больного находится в приемлемых границах (60—200 мг%), можно рекомендовать изменение доз обычного инсулина, как показано в таблице. Данная схема принята для больного, достаточно компенсированного в условиях введения 25 ЕД NPH плюс 10 ЕД обычного инсулина перед завтраком и 10 ЕД NPH плюс 5 ЕД обычного инсулина перед ужином. Изменение метаболического состояния может потребовать как изменения доз инсулина промежуточного действия, так и использования скользящей шкалы доз обычного инсулина.
помощью частых определений уровня глюкозы в плазме можно подобрать режим терапии.
Методика множественных подкожных инъекций инсулина предусматривает однократное введение промежуточного или долгодействующего инсулина вечером и инъекции обычного инсулина перед каждым приемом пищи. Чтобы проверить эффективность этого метода и нормализовать уровень глюкозы в плазме, необходим самоконтроль гликемии в домашних условиях. Один из подходов к началу такой терапии заключается во введении перед сном 25% суточной дозы инсулина промежуточного действия (NPH или ленте), которую больной получал ранее, а остальные 75% в виде простого инсулина, разделенные на 40,30 и 30% за 30 мин до завтрака, ленча и ужина соответственно. Альтернативная схема предусматривает инъекции без введения инсулина промежуточного действия ночью, но с применением долгодействующего инсулина [например, депо цинк-инсулина (ультраленте) или протамин-цннк-инсулина (ПЦИ)] перед ужином. Дозы «подстраивают» в соответствии с уровнем глюкозы в плазме. Применяют множество разных схем, и все они представляют собой скользящие шкалы, учитывающие уровень глюкозы в плазме. Типичная схема, базирующаяся на результатах определения уровня глюкозы в плазме в домашних условиях, показана в табл. 327-7. Некоторые больные нуждаются в иных дозировках. Конкретные детали можно найти в публикациях, посвященных данной методике (например, Schiffrin и Belmonte или монография Schade и соавт.).
МПИ могут оказаться эффективным средством нормализации гликемии и, по некоторым данным, не уступают в этом отношении ППИИ.
Методика постоянной подкожной инфузии инсулина основана на использовании небольшого насоса на батарейках, который подает инсулин под кожу стенки живота обычно через иглу 27-го размера с лепестками. При ППИ инсулин поступает с базальной скоростью непрерывно в течение суток, но существует программа увеличения скорости его поступления перед приемом пищи. Дозировку меняют в соответствии с результатами определения глюкозы в капиллярной крови, как это делается и при МПИ. Как правило, с базальной скоростью вводят 40% общей суточной дозы инсулина, а остальной — в виде разовых инъекций перед едой. Вряд ли можно сомневаться о том, что с помощью ППИ содержание сахара удается контролировать лучше, чем путем общепринятой терапии. По мере улучшения контроля улучшается и самочувствие большинства больных. Тем не менее, хотя инсулиновые инфузионные насосы привлекают внимание больных и многих врачей, их нельзя применять без разбора. У больных, которые постоянно поддерживают уровень глюкозы в плазме ниже 100 мг% (1000 мг/л), существует реальная опасность гипогликемии, особенно по ночам. Снижение уровня глюкозы в плазме на 50 мг% (500 мг/л) может и не иметь значения, когда исходный ее уровень равен 150 мг% (1500 мг/л), но если он составляет всего 60 мг% (600 мг/л), то такое снижение может оказаться смертельным. Среди больных, пользовавшихся насосами, имелось несколько смертельных случаев от гипогликемии. По мнению автора, насосы следует применять только у очень дисциплинированных и стремящихся к этому больных, которые находятся под наблюдением врачей, имеющих большой опыт работы с такими аппаратами. Помимо опасности гипогликемии, могут наблюдаться местные реакции на инсулин и нагноения.
Таблица 327-7. «Подстройка» доз инсулина при методике множественных инъекций1
I. Начало терапии
А. 0,6—0,7 ЕД инсулина на 1 кг массы тела Б. 25% NPH в 9 ч вечера; 75% — обычный инсулин в дробных дозах (40% перед завтраком, 30% перед ленчем, 30% перед ужином) В. Изменение дозы NPH каждые 48 ч, исходя из уровня глюкозы в крови натощак: менее 60 мг% — снять 2 ЕД более 90 мг% — прибавить 2 ЕД
Г. Изменение дозы обычного инсулина каждые 48 ч, исходя из гликемии через 1 ч после еды: менее 60 мг% — снять 2 ЕД более 140 мг% — прибавить 2 ЕД
Дата добавления: 2016-03-05; просмотров: 903;
