Нахождение в природе.
Ароматические углеводороды встречаются в растительных смолах и бальзамах. Фенантрен в частично или полностью гидрированном виде содержится в структурах многих природных соединений, например стероидов, алкалоидов.
Получение аренов:
1. сухая перегонка каменного угля;
2. дегидрирование циклоалканов
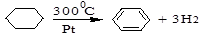
3. дегидроциклизация алканов с 6 и более атомами углерода в составе
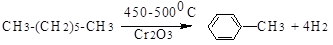
4. алкилирование

5. декарбоксилирование и восстановление кислородсодержащих соединений
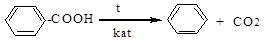
Изомерия.Для гомологов бензола характерна структурная изомерия: различное строение углеродного скелета бокового радикала и различные состав и расположение радикалов в бензольном кольце. Например, изомеры ароматических углеводородов состава С9Н12 (пропилбензол, изопропилбензол, о-метилэтилбензол и 1,2,4-триметилбензол):
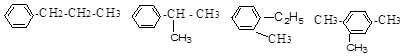
Строение.Ароматические углеводороды имеют целый ряд особенностей в электронном строении молекул.
Структурную формулу бензола впервые предложил А. Кекуле. Это шестичленный цикл с чередующимися двойными и одинарными связями , при этом двойные связи перемещаются в структуре:

.
В обеих формулах углерод четырехвалентен, все атомы углерода равноценны и дизамещенные бензола существуют в виде трех изомеров (орто-, мета-, пара-). Однако такая структура бензола противоречила его свойствам: бензол не вступал в характерные для непредельных углеводородов реакции присоединения (например, брома) и окисления (например, с перманганатом калия), для него и его гомологов основной тип химического превращения - реакции замещения.
Современный подход к описанию электронного строения бензола разрешает это противоречие следующим образом. Атомы углерода в молекуле бензола находятся в sр2-гибридизации. Каждый из атомов углерода образует три ковалентные σ-связи - 2 связи с соседними атомами углерода ( sр2-sр2-перекрывание орбиталей) и одну с атомом водорода (sр2-s- перекрывание орбиталей). Негибридизованные р-орбитали за счет бокового перекрывания образуют π-электронную сопряженную систему (π,π-сопряжение), содержащую шесть электронов. Бензол представляет собой плоский правильный шестиугольник с длиной связи углерод-углерод 0,14нм, связи углерод-водород 0,11нм, валентными углами 1200 :

Молекула бензола стабильнее циклических соединений с изолированными двойными связями, поэтому бензол и его гомологи склонны к реакциям замещения (бензольное кольцо сохраняется), а не присоединения и окисления.
Сходство в строении и свойствах (ароматичность) с бензолом проявляют и другие циклические соединения. Критерии ароматичности (Э. Хюккель, 1931г.):
а) плоская циклическая структура , т.е. атомы, образующие цикл, находятся в sр2-гибридизации; б) сопряженная электронная система; в) число электронов (N) в кольце равно 4n+2, где n - любое целочисленное значение - 0,1,2,3 и т.д.
Критерии ароматичности применимы как к нейтральным, так и заряженным циклическим сопряженным соединениям, поэтому ароматическими соединениями будут, например:
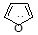


или
фуран катион циклопропенила.
Для бензола и других ароматических соединений наиболее характерны реакции замещения атомов водорода при углеродных атомах в цикле и менее характерны реакции присоединения по π-связи в цикле.
Дата добавления: 2016-02-20; просмотров: 10164;
