Реакции бензола с нарушением ароматической системы.
Ароматические углеводороды имеют прочный цикл, поэтому реакции с нарушением ароматической системы (окисление, радикальное присоединение) протекают в жестких условиях (высокие температуры, сильные окислители).
а) радикальное присоединение:
1. гидрирование
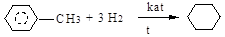
толуол циклогексан
2. хлорирование
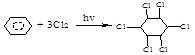
бензол 1,2,3,4,5,6-гексахлорциклогексан (гексахлоран).
Продукт этой реакции представляет смесь пространственных изомеров.
Ориентация электрофильного замещения в ароматических соединениях.Заместители в бензольном кольце по своему ориентирующему влиянию делятся на два типа: орто-, пара-ориентанты (заместители 1 рода) и мета-ориентанты (заместители 2 рода).
Заместители 1 рода - это электронодонорные группы, которые повышают электронную плотность кольца, увеличивают скорость реакции электрофильного замещения и активируют бензольное кольцо в этих реакциях:
D(+I-эффект): - R, -СН2ОН, -СН2NН2 и т.д.
D(-I,+М-эффекты): -NH2,-OH, -OR, -NR2, -SH и т.д.
Заместители 2 рода – электроноакцепторные группы, которые понижают электронную плотность кольца, уменьшают скорость реакции электрофильного замещения и дезактивируют бензольное кольцо в этих реакциях:
А (-I-эффект): -SO3H, -CF3, -CСl3 и т.д.
А (-I, -М -эффект): -НС=О, -СООН, -NO2 и т. д.
Атомы галогенов занимают промежуточное положение - они понижают электронную плотность кольца, уменьшают скорость реакции электрофильного замещения и дезактивируют бензольное кольцо в этих реакциях, однако это о-,п-ориентанты.
Если в бензольном кольце находится два заместителя, то их ориентирующее действие может совпадать (согласованная ориентация) или не совпадать (несогласованная ориентация). В реакциях электрофильного замещения соединения с согласованной ориентацией образуют меньшее количество изомеров, во втором случае образуется смесь из большего числа изомеров. Например:

п-гидроксибензойная кислота м-гидроксибензойная кислота
(согласованная ориентация) (несогласованная ориентация)
Полициклические конденсированные ароматические углеводороды (нафталин, антрацен, фенантрен и т.д.), в основном, по свойствам похожи на бензол, но вместе с тем имеют некоторые отличия.
Применение:
1. ароматические углеводороды - сырье для синтеза красителей, взрывчатых веществ, лекарственных препаратов, полимеров, поверхностно-активных веществ, карбоновых кислот, аминов;
2. жидкие ароматические углеводороды хорошие растворители органических соединений;
3. арены - добавки для получения высокооктановых бензинов.
Знаете ли вы, что
-В 1649 году немецкий химик Иоганн Глаубер впервые получил бензол.
-В 1825 году М. Фарадей выделил из светильного газа углеводород и установил его состав - С6Н6.
-В 1830 году Юстус Либих назвал полученное соединение бензолом (от араб. Вen-аромат + zoa-сок + лат. ol[eum]-масло).
-В1837 году Огюстом Лораном назван радикал бензола С6Н5 - фенил (от греч phenix-освещать).
-В 1865 году немецкий химик-органик Фридрих Август Кекуле предложил формулу бензола с чередующимися двойными и одинарными связями в шестичленном цикле.
-В 1865-70-х годах В. Кернер предложил использовать приставки для обозначения взаимного расположения двух заместителей: 1,2 положение - орто- (orthos - прямой);1,3- мета ( meta - после) и 1,4- пара (para - напротив).
-Ароматические углеводороды - высокотоксичные вещества, вызывают отравление и поражение некоторых органов, например почек, печени.
-Некоторые ароматические углеводороды - канцерогены (вещества, вызывающие раковые заболевания), например бензол (вызывает лейкемию), один из сильнейших - бензопирен (содержится в табачном дыме).
ЛЕКЦИЯ № 9.
Дата добавления: 2016-02-20; просмотров: 1989;
