ЭФФЕКТЫ ПРИ ПОВТОРНОМ ПРИЕМЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ Кумуляция
Кумуляция (от лат. cumulatio - «увеличение, скопление») - накопление в организме молекул лекарственных средств (материальная кумуляция) или их эффектов (функциональная кумуляция).
Материальная кумуляция характерна для липофильных лекарственных средств, обладающих низким печеночным и/или почечным клиренсом и длительным периодом полуэлиминации. В клинической практике необходимо учитывать кумуляцию фенобарбитала, бромидов, гликозидов наперстянки (дигитоксина, ланатозида Ц, дигоксина), антикоагулянтов непрямого действия.
Кумуляция имеет как положительное, так и отрицательное значение. Положительное значение связано с пролонгированием действия лекарственных средств, возможностью их редкого приема. Например, больные ХСН избавлены от необходимости принимать сердечный гликозид дигоксин ночью. Отрицательное значение заключается в опасности интоксикации в результате суммирования введенных доз лекарственного средства. Для того чтобы предотвратить интоксикацию кумулирующими лекарствами, необходимо рассчитать поддерживающую дозу таким образом, чтобы количество принятого вещества было равно количеству, элиминируемому из организма за сутки. Для расчета используют коэффициент элиминации - долю выводимого за сутки лекарственного средства в процентах:
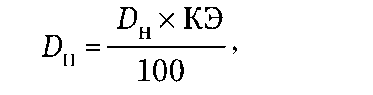
где Dп - поддерживающая доза; Dн - нагрузочная (начальная) доза; КЭ - коэффициент элиминации.
Относительная материальная кумуляция связана не с фармакокинетическими свойствами лекарственного средства, а с недостаточностью систем элиминации. Она развивается при заболеваниях печени и почек, а также у детей и пожилых людей. При патологии печени возможна кумуляция активных метаболитов лекарственных средств.
Функциональная кумуляция характеризуется сохранением фармакодинамических эффектов после элиминации лекарственного средства из организма. Примерами функциональной кумуляции служат хронический алкоголизм при злоупотреблении этанолом, паралич центров продолговатого мозга при отравлении свинцом.
Привыкание (толерантность)
Привыкание (толерантность) - ослабление эффектов лекарственных средств при повторном приеме. Для возобновления терапевтического действия необходимо повышение дозы. Так, противотревожные свойства диазепама обычно проявляются при приеме всего 5-10 мг/сут, но на фоне привыкания доза возрастает до 1000 мг/сут.
В основе привыкания лежат фармакокинетические и фармакодинамические механизмы.
Известны следующие фармакокинетические механизмы привыкания.
• Нарушение всасывания. Известно, что мышьяковистый ангидрид всасывается из кишечника только при условии щелочной среды кишечного сока. Прием мышьяка вызывает воспалительный процесс (энтерит), в результате чего в кишечнике создается кислая среда. Это ослабляет резорбтивное токсическое действие. Так, собаки, получавшие в течение двух лет мышьяковистый ангидрид в малых дозах внутрь, могут употребить 2,5 г токсина без симптомов отравления, но его парентеральное введение в дозе всего 2 мг вызывает гибель.
• Изменение активности ферментов метаболизма. Индукция метаболической трансформации сопровождается привыканием, если лекарственные средства преобразуются в неактивные продукты. Ингибирование приводит к привыканию при применении пролекарств, требующих метаболической активации. Например, из-за истощения ресурса восстановленных тиолов в эндотелии сосудов прекращается восстановление нитрогруппы в функциональную группу NO.
• Повышение активности гликопротеина Р. Гликопротеин Р, удаляя лекарственные средства из эпителия кишечника, гепатоцитов, нефроцитов, эндотелия гистогематических барьеров, препятствует их взаимодействию с циторецепторами. При высокой активности гликопротеина Р развивается множественная лекарственная устойчивость.
Фармакодинамические механизмы привыкания могут быть следующими.
• Десенситизация (снижение чувствительности) циторецепторов.
- Гетерологическая десенситизация - ослабление реакции циторецепторов на многие вещества под влиянием одного агониста.
- Гомологическая десенситизация - ослабление реакции только на агониста, вызывающего десенситизацию.
• Снижение количества циторецепторов (down-регуляция). Количество циторецепторов уменьшается из-за нарушения транскрипции генов, деградации мРНК, протеолиза и секвестрации в клетке.
• Подавление выделения нейромедиаторов. Агонисты циторецепторов тормозят выделение нейромедиаторов по принципу отрицательной обратной связи. Так, опиоидные анальгетики нарушают выделение эндогенных пептидов - энкефалинов, β-эндорфина и динорфина.
• Снижение возбудимости чувствительных нервных окончаний. Такой механизм лежит в основе привыкания к слабительным средствам при их длительном применении.
• Включение компенсаторных механизмов регуляции функций. Например, терапевтическое действие антигипертензивных средств ослабляется либо в связи с тахикардией и ростом минутного сердечного выброса, либо из-за ухудшения почечного кровотока, уменьшения диуреза и повышения объема циркулирующей крови (ОЦК).
Известно привыкание вследствие обучения. В таких ситуациях жизненный опыт и повышенная бдительность позволяют исправлять внешние проявления нарушений, вызываемых химическими веществами. Например, больные хроническим алкоголизмом обучаются ходить по прямой линии после приема этанола, несмотря на функциональные расстройства в двигательной сфере.
Тахифилаксия (от греч. tachys - «быстрый» и phylaxis - «бдительность, охрана») - особый вид привыкания, характеризуется быстрым, в течение нескольких часов, развитием толерантности к лекарственным средствам.
Тахифилаксия чаще всего обусловлена истощением ресурсов медиатора в синаптических окончаниях. Например, адреномиметик непрямого действия эфедрин стимулирует выброс медиатора норадреналина из секреторных гранул в адренергических синапсах и тормозит его нейрональный захват. Это сопровождается опустошением гранул и ослаблением гипертензивного действия эфедрина.
Толерантность к разным эффектам лекарственных средств может развиваться не одновременно. При длительном приеме фенобарбитала ослабляется его снотворное действие, но сохраняется противосудорожная активность. Терапия анксиолитиками сопровождается ослаблением миорелаксирующего эффекта, хотя противотревожное действие не изменяется.
При перекрестном привыкании (кросстолерантности) применение одного лекарственного средства ведет к уменьшению реакции на другое.
Дата добавления: 2016-02-20; просмотров: 2398;
