Коагуляция растворов высокомолекулярных соединений.
Растворы высокомолекулярных веществ в термодинамически равновесном состоянии аналогично истинным растворам обладают абсолютной агрегативной устойчивостью, что определяется наличием на поверхности частиц двух оболочек: электрической и сольватной (гидратной). Для коагуляции коллоидов высокомолекулярных соединений необходимо не только нейтрализовать заряд коллоидной частицы, но и разрушить жидкостную оболочку. Выделение высокомолекулярных соединений из растворов по своему характеру отличается от, коагуляции типичных гидрофобных коллоидов. Так, если для гидрофобных золей достаточно незначительных добавок электролита, чтобы вызвать коагуляцию, то для высокомолекулярных веществ этого недостаточно. Для выделения дисперсной фазы полимеров необходимы высокие (вплоть до насыщенных растворов) концентрации электролитов. Например, яичный глобулин выделяется при полунасыщении раствора сульфатом аммония, а яичный альбумин — только при полном насыщении.
Явление выделения в осадок растворенного ВМС под действием большой концентрации электролита получило название высаливания. К высаливанию неприменимо правило Шульце—Гарди, поэтому нельзя отождествлять высаливание с явлением обычной электролитной коагуляции. Явление высаливания высокомолекулярных веществ в отличие от гидрофобных золей не связано с дзета-потенциалом коллоидных мицелл и заключается в нарушении сольватной (гидратной) связи между макромолекулами полимера и растворителем, т. е., иначе, в понижении растворимости полимера. При введении соли часть молекул растворителя, которая была в сольватной связи с макромолекулами ВМС, сольватирует молекулы введенной соли. Чем больше будет введено соли, тем большее число молекул растворителя покинет макромолекулы полимера и сольватирует соль. Таким образом, высаливающее действие соли заключается в ее собственной сольватации (гидратации) за счет десольватации (дегидратации) молекул высокомолекулярных веществ.
Многочисленные исследования показали, что всякое соединение, способное сольватироваться растворителем данного ВМС и понижать его раствори  мость, пригодно для высаливания. Так, спирт и ацетон способны отлично высаливать желатину из ее водных растворов. Аналогично происходит осаждение спиртом белка из водного раствора или осаждение ацетоном каучука из раствора бензола.
мость, пригодно для высаливания. Так, спирт и ацетон способны отлично высаливать желатину из ее водных растворов. Аналогично происходит осаждение спиртом белка из водного раствора или осаждение ацетоном каучука из раствора бензола.
Рис.6.16
Учитывая механизм осаждающего действия электролитов и других десольватирующих веществ, Кройт в свое время предложил общую схему осаждения высокомолекулярных веществ (рис. 6.16). Для осаждения макромолекул, как видно на схеме, необходимо удалить водную оболочку (спиртом или другим дегидратирующим веществом) и снять заряд ее путем прибавления электролита. Последовательность этих операций не имеет значения. Схема Кройта учитывает только действие электролитов и дегидратирующих веществ, т. е. снятие заряда и водной оболочки, но совершенно не учитывает специфичности этих веществ.
В ряде случаев для осаждения многих высокомолекулярных соединений белков, полисахаридов) снятие заряда не является обязательным условием, так как главным фактором их устойчивости служит гидратная оболочка, удерживаемая полярными, но не диссоциированными группами (эфирными и пептидными связями, спиртовыми группами). Некоторые высокомолекулярные соединения обладают высокой стойкостью к высаливанию. Например, при засолке рыбы в раствор (рассол) переходят значительные количества белковых соединений, коорые остаются в нем в состоянии золя, несмотря на то, что он является почти насыщенным раствором соли. Такая высокая устойчивость к высаливанию объясняется особо сильной гидратацией белков.
Таким образом, при высаливании высокомолекулярных веществ решающую роль играет не зарядность ионов, а их способность к гидратации и к адсорбции на коллоидно-дисперсных частицах.
По своему высаливающему действию все катионы и анионы, можно расположить в лиотропные ряды:
С2О42-> SO42- > СН3СОО- > Сl- > NO3- > I- > CNS
Li+ > Na+ >K+ > Pb+ > Cs+ > Mg2+ > Ca2+ > Sn2+ > Ba2+
Расположение ионов в лиотропных рядах связано не с величиной их заряда, как в случае обычной коагуляции, а со степенью их гидратации. Чем больше ион способен связывать растворитель, тем больше его высаливающее действие. Основная роль в высаливании, как и в набухании, принадлежит анионам, катионы же оказывают, меньшее воздействие на высаливание.
Большое влияние на процесс высаливания оказывает также и степень растворимости самого полимера в данном растворителе: чем она ниже, тем полнее и быстрее происходит высаливание. В свою очередь растворимость полимерного соединения зависит от длины макромолекул и молекулярной массы полимера: чем они больше, тем меньше растворимость данного полимера, следовательно, тем легче он высаливается. На этом принципе основан метод так называемого фракционного высаливания, сущность которого заключается в последовательном высаливании из раствора все возрастающими порциями высаливателя отдельных фракций полимеров, начиная с полимеров наивысшей степени полимеризации (с наибольшей молекулярной массой). Так, на тонком сочетании действия спирта, солей и охлаждения до 268 К основаны способы детального фракционирования белковых смесей по Кону. Из сыворотки крови этим методом можно выделить свыше 12 различных белков.
Для фракционирования применяют также способ постепенного понижения температуры при постоянном составе жидкости. Препаративное разделение высокомолекулярных соединений широко применяется при научных исследованиях для характеристики полидисперсности полимеров.
Как показали исследования, высокомолекулярные вещества, выделенные из раствора высаливанием, после отмывки их от электролитов могут быть снова переведены в раствор (явление обратимо). Коллоиды, которые при устранении фактора, вызвавшего коагуляцию, способны переходить из состояния геля в состояние золя, носят название обратимых коллоидов. Однако высокомолекулярные вещества могут при определенных условиях осаждаться и необратимо. Такое необратимое осаждение высокополимеров, в частности белков, под влиянием высокой температуры, при воздействии концентрированных кислот и щелочей, дубильных веществ, лучистой энергии называется денатурацией. При денатурации происходит не только осаждение полимеров, но и изменение их химической природы. Белки при денатурации становятся нерастворимыми и в большинстве случаев утрачивают способность к набуханию.
Высаливание имеет большое практическое значение в целом ряде технологических процессов, например в мыловарении, в производстве красителей, канифоли и многих других искусственных волокон.
Коацервация.
В растворах высокомолекулярных соединений при изменении температуры, рН или при введении низкомолекулярных веществ иногда наблюдается явление коацервации. Внешне процесс коацервации характеризуется отделением от золя изолированных друг от друга макроскопических капель жидкости или целого жидкого слоя. Такая капля (рис. 6.20) содержит рой ультрамикроскопических капелек. Каждая из них состоит из нескольких первичных сольватированных частиц, сохранивших свою самостоятельность. Таким образом, от высаливания коацервация отличается тем, что вещество дисперсной фазы не отделяется от растворителя, а собирается в невидимые простым глазом жидкие капельки, которые постепенно сливаются в капельки больших размеров — вплоть до видимых невооруженным глазом, пока процесс этот не закончится полным расслоением системы на два жидких слоя. Вязкая фаза, содержащая все или почти все высокомолекулярное вещество, называется коацерватом.
Частицы высокомолекулярного соединения, входящие в состав коацерватных капель, по-видимому, отделены друг от друга тонкими гидратными оболочками. Об этом свидетельствует то, что явление коацервации обратимо. При изменении условий, вызвавших коацервацию
Рис.6.17 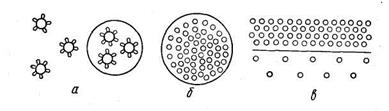
(уменьшение концентрации электролита, изменение рН и температуры), коацерватные капли могут исчезать и система вновь переходит в однофазную. В то же время, изменяя условия в сторону усиления процесса дегидратации макромолекул высокополимера, можно вызвать разрушение коацерватных капель и полное осаждение растворенного вещества.
коацервацию можно наблюдать также и при взаимодействии желатина и лецитина. При комплексной коацервации по существу происходит высаливание одного золя другим. Здесь возможны следующие наиболее типичные случаи.
. По некоторым своим физико-химическим свойствам коацерваты напоминают свойства протоплазмы, поэтому считают, что именно процесс коацервации имел исключительно большое значение в истории возникновения жизни на Земле.
Дата добавления: 2016-02-20; просмотров: 2371;
