ПОЛУЧЕНИЕ КОЛЛОИДНЫХ РАСТВОРОВ
И ИЗУЧЕНИЕ ИХ СВОЙСТВ
Цель работы.
1. Получить коллоидные растворы методами диспергирования и конденсации.
2.Определить пороги коагуляции разных электролитов и проверить правило Шульца-Гарди.
3. Изучить метод защиты коллоидов.
4. Определить величину ИЭТ желатина.
5. Изучить влияние рН среды на набухание ВМС (желатина).
При выполнении задания 1 проделывают опыты 1, 2, 3, 5, 6, 7,8,10 ; для задания 2-го – опыты 1,3, 4, 5, 6,7, 8, 9.
ПОЛУЧЕНИЕ КОЛЛОИДОВ МЕТОДОМ КОНДЕНСАЦИИ
Опыт 1. Получение гидрозоля серы (методом замены растворителя).
В 3-5 см3 дистиллированной воды по каплям вливают 0,5-1 см3 насыщенного раствора серы в абсолютном спирте, непрерывно взбалтывая содержимое. Образуется молочно-белый опалесцирующий золь.
Понаблюдайте и запишите, как изменяется окраска золя в отражении и в проходящем свете. Дайте объяснение.
Опыт 2. Получение золя Fe(OH)3 путем гидролиза.
В термостойкий стакан помещают 50 см3 дистиллированной воды и нагревают до кипения. В кипящую воду добавляют по каплям 10 см3 3% раствора трихлорида железа. Получается интенсивно окрашенный коричнево-красный коллоидный раствор тригидроксида железа.
При этом происходят следующие реакции:
FeCl3 + 3H2O = Fe(OH)3  + 3HCl
+ 3HCl
Fe(OH)3 + HCl → FeOCl + 2H2O
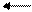
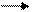 FeOCl FeO+ + Cl-
FeOCl FeO+ + Cl-
Напишите схему строения мицеллы полученной коллоидной системы. Полученный коллоидный раствор сохраните для дальнейшей работы.
Опыт 3. Получение золя берлинской лазури методом конденсации. Перезарядка поверхности коллоидных частиц.
А)В пробирку наливают 20 см3 0,01%-ного раствора железистосинеродистого калия K4[Fe(CN)6] и прибавляют 8-10 капель 2%-ного раствора хлорного железа FeCl3.
При этом протекает реакция:
3K4[Fe(CN)6] + 4FeCl3 → Fe 4 [Fe(CN)6] 3 ↓ + 12КCl
берлинская лазурь
Так как соединение K4[Fe(CN)6] находится в избытке, то оно и является стабилизатором при образовании золя берлинской лазури (синего цвета ). Строение мицеллы этого золя запишите.
В) Отбирают 1 см3 золя, полученного ранее, и по каплям прибавляют к нему 2%-ного раствора FeCl3 происходит перезарядка поверхности вследствие замены потенциалопределяющих ионов, а, следовательно, и противоионов. Роль стабилизатора в этом случае выполняет FeCl3. Образование этого коллоида можно пронаблюдать визуально по изменению окраски золя (переходит в зеленую ).
Изобразите строение мицеллы этого золя.
Опыт 4. Получение золя железа методом конденсации
К 20 см3 насыщенного раствора FeCl3 добавляют по каплям 2 н раствор (NH4)2CO3. Если есть осадок, то по каплям добавляют еще FeCl3. Схема протекания реакции:
2FeCl3 - 3(NH4)2CO3 + Н2О →2FeО(ОН) ↓+ 6 NH4Cl + 3СО2
Дата добавления: 2016-02-20; просмотров: 1438;
