Общая характеристика элементов I А группы. Особенности лития и его соединений. В периодической системе всего 14 s -элементов (включая водород и гелий)
В периодической системе всего 14 s -элементов (включая водород и гелий). Это элементы I А и II А групп. Элементы I А группы – щелочные металлы Li, Na, K, Rb, Cs, Fr. Все они имеют на внешнем электронном уровне атома по одному электрону ns1, сильно удаленному от ядра, с низким потенциалом ионизации. Всегда проявляют степень окисления +1.
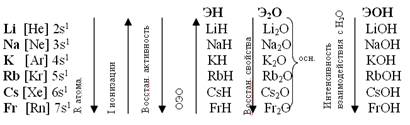
Сверху вниз в подгруппе возрастает радиус атома элементов за счет возникновения новых электронных уровней.
В группах по мере увеличения числа энергетических уровнейатомные радиусы растут. Переход нейтрального атома в катион 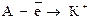 , сопровождается уменьшением радиуса поскольку в катионе заряд ядра удерживает меньшее число электронов. Очевидно, с возрастанием заряда ионный радиус катиона будет падать.
, сопровождается уменьшением радиуса поскольку в катионе заряд ядра удерживает меньшее число электронов. Очевидно, с возрастанием заряда ионный радиус катиона будет падать.
Энергия ионизации– это та энергия, которую необходимо затратить на отрыв внешнего электрона у невозбужденного атома. Строение внешних оболочек ns1, поэтому они имеют низкие энергии ионизации, уменьшающиеся при переходе по подгруппе сверху вниз. Связь электрона с ядром ослабевает при этом за счет увеличения радиуса атома и экранирования заряда ядра предшествующими внешнему электрону оболочками, увеличивается расстояние электрона от ядра и энергия ионизации уменьшается.
С ростом заряда ядра от Na к Fr усиливаются восстановительные свойства, это самые активные металлы. Их стандартные электродные потенциалы j° отрицательные и имеют большое абсолютное значение. Наиболее отрицателен j° лития равный -3,02 В по сравнению с ионами других щелочных металлов (ион Li+ имеет среди них наименьший радиус), хороший комплексообразователь. Энтальпия гидратации катионов лития велика (∆Н° гидрат.= - 486,6 кДж/моль). Чем меньше алгебраическая величина потенциала, тем выше восстановительная способность этого металла и тем ниже окислительная способность его ионов. Металлический литий – самый сильный восстановитель, а ион Li+ самый слабый окислитель.
Дата добавления: 2016-01-30; просмотров: 1517;
