Решение кинетических задач для гетерогенно-каталитических процессов
Пусть на поверхности твердого катализатора протекает химическая реакция первого порядка. Все участники реакции - газы.
В ® gG + rR.
Реакция осуществляется в реакторе закрытого типа (V = const.).
Случай 1. На поверхности катализатора наблюдается слабая адсорбция только вещества В.
Для решения кинетической задачи запишем два уравнения:
а) скорость реакции на основе обычных представлений о скорости
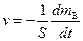 ; (5.76)
; (5.76)
б) скорость реакции на основе закона действующих поверхностей равна:
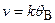 . (5.77)
. (5.77)
Если 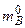 – исходное количество молей вещества В, участвующее в реакции, а (
– исходное количество молей вещества В, участвующее в реакции, а ( 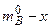 ) – количество молей вещества В к моменту времени t , то:
) – количество молей вещества В к моменту времени t , то:
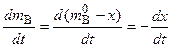 . (5.78)
. (5.78)
Тогда:
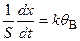 . (5.79)
. (5.79)
Так как реакция протекает в газовой фазе, продукты реакции не адсорбируются, поэтому степень заполнения поверхности катализатора реагентом можно выразить через уравнение Лэнгмюра:

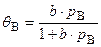 . (5.80)
. (5.80)
Объединяя (5.79) и (5.80) получим:

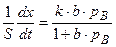 . (5.81)
. (5.81)
Так как адсорбция вещества В- слабая, то b∙рB <<1, поэтому:
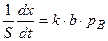 . (5.82)
. (5.82)
В уравнении (5.82) три переменные величины - t, x и рB. Так как вся реакция протекает в газовой фазе, то число молей компонента В связано с парциальным давлением этого компонента уравнением Менделеева- Клапейрона:
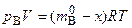 , (5.83)
, (5.83)
где V - объем реактора.
Из уравнения (5.83) можно найти производную 
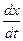 :
:
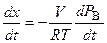 . (5.84)
. (5.84)
Уравнение (5.84) подставим в уравнение (5.82), разделим переменные и проинтегрируем полученное уравнение:
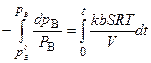 . (5.85)
. (5.85)
В результате интегрирования получим:
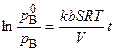 . (6.86)
. (6.86)
Из этого уравнения можно вычислить константу скорости гетерогенной каталитической химической реакции первого порядка в случае слабой адсорбции исходного вещества:

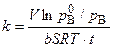 . (5.87)
. (5.87)
Если параметры реактора остаются постоянными, то уравнение принимает вид обычного уравнения для реакции первого порядка с константой скорости каталитического процесса равной:
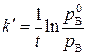 . (5.88)
. (5.88)
Случай 2. Вещество В адсорбируется умеренно (0< b >1), продукты реакции не адсорбируются.
В этом случае справедливо уравнение (5.81). Подставим в это уравнение соотношение (5.84):
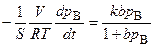 . (5.89)
. (5.89)
Разделим переменные и проинтегрируем уравнение (5.89):
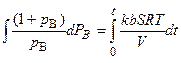 . (5.90)
. (5.90)
После интегрирование получим уравнение:
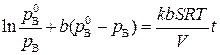 . (5.91)
. (5.91)
Из этого уравнения можно вычислить константу скорости гетерогенной каталитической химической реакции первого порядка в случае средней адсорбции исходного вещества:
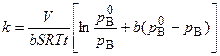 . (5.92)
. (5.92)
Случай 3. Вещество В адсорбируется слабо, вещество G - сильно, вещество R – не адсорбируется.
Степень заполнения поверхности катализатора реагентом можно выразить через уравнение, куда войдут характеристики адсорбции исходного вещества и одного из продуктов реакции:
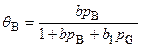 . (5.93)
. (5.93)
Учтем, что адсорбция В слабая, а адсорбция G - сильная, тогда:
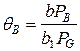 . (5.94)
. (5.94)
Подставим (5.94) в (5.79) и учтем, что
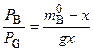 . (5.95)
. (5.95)
Тогда:
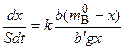 . (5.96)
. (5.96)
Разделим переменные и проинтегрируем полученное уравнение:
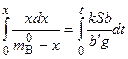 . (5.97)
. (5.97)
После интегрирования, получим уравнение:
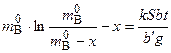 . (5.98)
. (5.98)
Константа скорости данной реакции будет равна:

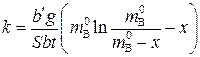 . (5.99)
. (5.99)
Дата добавления: 2016-01-09; просмотров: 1127;
