Параметры, уравнение состояния идеального газа
Задача 1. Ртутный вакууметр, присоединенный к сосуду с метаном СН4, показывает разряжение 0,056 МПа. Атмосферное давление по ртутному барометру составляет 768 мм рт. ст. (0,102 МПа). Определить абсолютное давление в сосуде и плотность метана, если температура в сосуде равна 20°С. Показания вакуумметра и барометра приведены к температуре 0°С.
Решение. Абсолютное давление в сосуде определяется по формуле Рабс=В0-Рвак=0,102-0,056=0,046 МПа. Плотность газа находим из уравнения состояния, предварительно определив газовую постоянную:
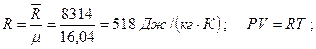

Задача 2. Баллон с кислородом емкостью 20 л находится под давлением 1,0 МПа при t=15°С. После израсходования части кислорода давление понизилось до 0,76 МПа, а температура уменьшилась до 10°С. Определить массу израсходованного кислорода.
Решение. Из уравнения состояния PV=GRT находим, что до расходования кислорода его масса в баллоне была равна:
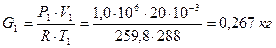
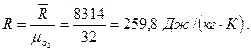
После израсходования части кислорода масса его в баллоне будет равна:
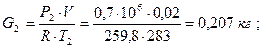
следовательно, расход кислорода составит:
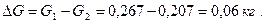
Задача 3. Определить удельный объем пропана (С3Н8) как идеального газа при следующих условиях: температура газа t=20°С, манометрическое давление газа в баллоне 5,6 МПа, абсолютное давление газа в помещении равно 0,099 МПа.
Решение. Абсолютное давление газа в баллоне
Рабс=Рман+В0=5,6+0,099=5,699 МПа;
удельная газовая постоянная пропана
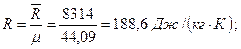
абсолютная температура газа
Т=273+20=293 К;
удельный объем пропана в рассматриваемых условиях
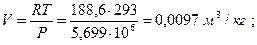
удельный молярный объем пропана при тех же условиях равен:
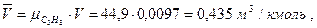
или, что то же самое:
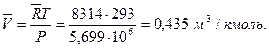
Дата добавления: 2015-10-13; просмотров: 3736;
