Абсолютная энтропия идеального кристалла при ОК равна нулю.
В идеальном кристалле при О К все частицы находятся в одном энергетическом состоянии, т.к. кристалл упорядочен, тепловое движение
отсутствует, то для идеального кристалла возможно только 1 состояние полной упорядоченности, т.е.
W=1
S=K ln 1=0
Энтропии веществ как и их теплота образования принято относить к
определенным условиям ( 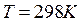 и
и 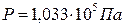 )
)
Энтропию при этих условиях называют стандартной энтропией образования и её значения сведены в таблицу
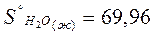 Дж/моль* К Дж/моль* К
| 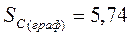 Дж/моль* К Дж/моль* К
| |
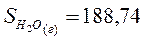 Дж/моль* К Дж/моль* К
| 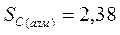 Дж/моль* К Дж/моль* К
|
Энтропия является функцией состояния системы и ее изменения в ходе химических реакций рассчитывается как разница суммарных энтропии продуктов реакций и исходных веществ
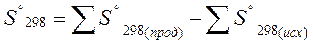 |
Вывод:
Изменение энтропии указывает на термодинамическую вероятность самопроизвольного протекания процесса. Если S > 0, то процесс, наиболее вероятен. S < 0, то процесс менее вероятен, но он может быть осуществлен.
Дата добавления: 2015-09-07; просмотров: 1188;
