Специфические свойства оксикислот
1. Отношение оксикислот к нагреванию. Оксикислоты в зависимости от положения ОН-группы по разному себя ведут при нагревании. Это позволяет отличить α, β, γ и другие оксикислоты друг от друга,
а) α-гидроксикислоты:
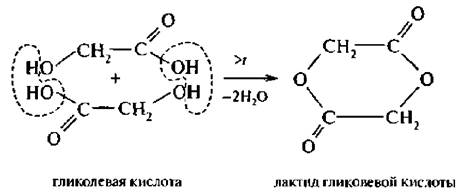
В случае α-оксикислот происходит взаимодействие между двумя молекулами кислоты, при этом выделяются две молекулы воды, и образуется циклический сложный эфир, который называется лактидом.
б) β-гидроксикислоты:
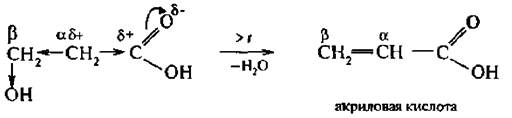
На β-углеродном атоме электронная плотность уменьшается, вследствие чего водород становится подвижен – отщепляется молекула воды и образуется непредельная кислота. Таким образом β-оксикислоты образуют α, β-непредельные кислоты.
в) γ-гидроксикислоты:
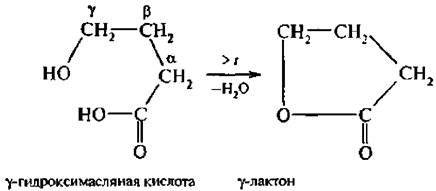
При нагревании γ-гидроксикислоты претерпевают внутримолекулярную циклизацию с образованием циклических сложных эфиров, которые называются лактонами
Расщеплении α-гидроксикислот: Для α-оксикислот характерна еще одна специфическая реакция. При действии концентрированной серной кислоты а-оксикислоты разлагаются с разрывом С-С связи:
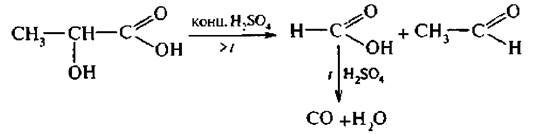
В этих условиях, как правило, образуется муравьиная кислота и соответствующий альдегид или кетон. Образовавшаяся муравьиная кислота при действии концентрированной серной кислоты и нагревании разлагается с выделением оксида углерола (II) и воды. Это реакция используется для определения α-гидроксикислот.
Несколько слов о молочной кислоте, так как из α-гидроксикислот она имеет наиболее важное значение.
МОЛОЧНАЯ КИСЛОТА (α-оксипропионовая)
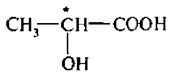
Она содержится в кислом молоке, откуда и получила свое название.
В промышленности молочную кислоту получают молочнокислым брожением углеводов:
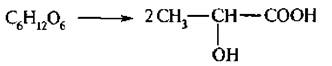
Получают молочную кислоту и при восстановлении пировино-градной кислоты:

В молочной кислоте содержится один ассиметрический атом углерода. Поэтому она существует в виде двух оптических изомеров:
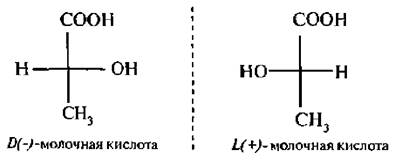
Представителями двухосновных гидроксикислот являются яблочная (оксиянтарная) кислота и винная (диоксиянтарная) кислота.
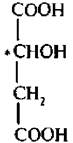
яблочная кислота
Яблочная кислота – это двухосновная трехатомная кислота. Молекула яблочной кислоты содержит один асимметрический атом углерода, поэтому существует в виде двух оптических изомеров и оптически неактивной рацемической форме:
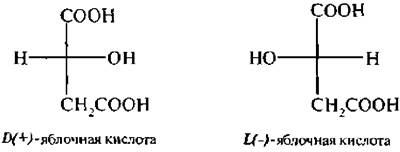
В природе встречается L(–)-яблочная кислота.
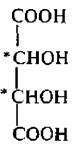
ВИННАЯ КИСЛОТА
Винная кислота – двухосновная, четырехатомная. Молекула винной кислоты содержит два асиметрических атома углерода и существует в виде трех стереоизоизомеров: D-винная кислота, L-винная кислота и мезовинная кислота.
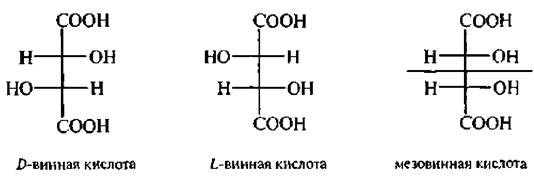
При хранении вина она выделяется в виде нерастворимой кислой калиевой соли (калий виннокислый).
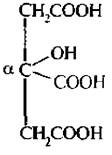
ЛИМОННАЯ КИСЛОТА
Это четырехатомная, трехосновная кислота. Относится к α-гидроксикислотам.
Как и все α-оксикислоты. лимонная кислота при нагревании с концентрированной H2SO4 разлагается с выделением муравьиной кислоты и ацетонадикарбоновой кислоты:
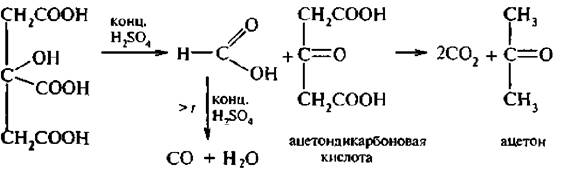
Ацетондикарбоновая кислота при нагревании декарбоксилируется с образованием ацетона. Соли лимонной кислоты называют цитратами. Лимонная кислота, также как и винная, относится к пищевым кислотам. Цитрат натрия используется при консервировании крови.
Дата добавления: 2015-09-29; просмотров: 11702;
