Экспериментальная часть. Электропроводность растворов электролитов рассчитывают по электрическому сопротивлению, которое измеряется с помощью кондуктометров различных конструкций
Электропроводность растворов электролитов рассчитывают по электрическому сопротивлению, которое измеряется с помощью кондуктометров различных конструкций. Работа кондуктометра основана на принципе мостика Кольрауша (рис. 3.2).С помощью подвижного контакта (К) находят такое положение, при котором ток через боковую цепь (СК) идти не будет (рис. 3.2). Такое состояние моста называется балансом. Принципиальная схема реохордного моста Р38 и порядок работы на нем приведена в приложении.
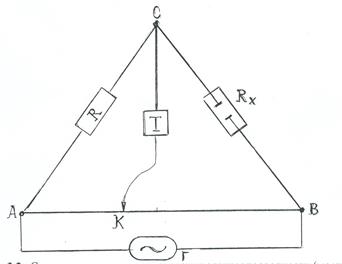
Рис. 3.2.Схема установки для определения электропроводности (мостик Кольрауша).АВ - реохорд;К – подвижный контакт; Г – звуковой генератор; Т – телефон или осциллограф; Rx – стакан сисследуемым раствором; R – магазин сопротивлений.
Последовательность выполнения работы по измерению молярной электропроводности слабого электролита и определению его константы диссоциации следующий.
1. Определяют константу электродов, так как в электролитической ячейке неизвестны ни сечение электродов, ни расстояние между ними. Константа электродов определяется по раствору хлорида калия (KCl) с известной удельной электропроводностью:
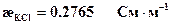
С помощью кондуктометра измеряют сопротивление раствора KCl, который наливают так, чтобы раствор был выше уровня электродов более чем на 2 см. Вычисляют константу электродов:
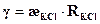
2. Определяют молярную электропроводность исследуемого раствора. Сначала измеряют сопротивление исследуемого раствора (R) на кондуктометре, заливая электролитическую ячейку также, как и в случае с раствором KCl.
Затем рассчитывают удельную электропроводность исследуемого раствора:
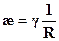
После этого, зная молярную концентрацию исследуемого раствора (с) в 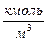 , находят молярную электропроводность:
, находят молярную электропроводность:
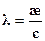
3. Вычисляют константу диссоциации слабого электролита по формуле (3.6):
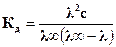
Значения молярной электропроводности при бесконечном разведении ( 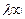 ) [См×м2 кмоль-1] приведены в таблице.
) [См×м2 кмоль-1] приведены в таблице.
Таблица
| Температура, 0С | |||||||||
| l∞ HCOOH | 36,2 | 36,8 | 37,4 | 38,0 | 38,6 | 39,2 | 39,8 | 40,4 | 41,0 |
| l∞ CН3СOOH | 34,9 | 35,5 | 36,1 | 36,7 | 37,3 | 37,8 | 38,5 | 39,1 | 39,6 |
Дата добавления: 2015-09-28; просмотров: 1542;
