ГЛАВА 11. геном хозяина с весьма серьезными последствиями, если при этом затрагивается какой-то важный ген или происходит злокачественная трансформация клетки
геном хозяина с весьма серьезными последствиями, если при этом затрагивается какой-то важный ген или происходит злокачественная трансформация клетки. Однако такое развитие событий считается крайне маловероятным. Скорее всего такая ДНК какое-то время просуществует в клетке в виде нереплицирующегося внехромосомного элемента, а затем разрушится. Генную иммунизацию пока используют для выработки иммунитета к некоторым патогенным микроорганизмам (вирусу гриппа А, вирусу иммунодефицита человека типа I, вирусу бычьего герпеса, вирусу бешенства, Plasmodium sp., вызывающему малярию, вирусу гепатита В) у животных, но не у человека.
Для облегчения доставки ДНК в клетки животных при проведении генной иммунизации был создан модифицированный штамм Shigella flexneri. Эта бактерия проникает в эпителиальные клетки животных путем фагоцитоза, и присутствующая в ней плазмидная ДНК попадает в цитоплазму клетки-хозяина, где и происходят транскрипция и трансляция переносимого ею гена, находящегося под контролем эукариотического промотора. Shigella — это патогенный микроорганизм, и как таковой он не может использоваться для доставки ДНК. Ее непатогенный штамм можно получить, введя делецию в ген asd, кодирующий фермент аспартат-β-полуальдегид—дегидрогеназу, который участвует в синтезе компонента клеточной стенки диаминопимелиновой кислоты.
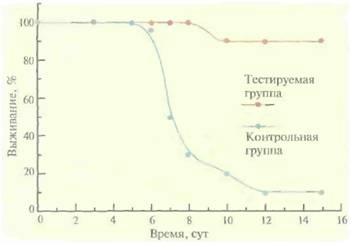
| Рис. 11.5. Выживание мышей, иммунизированных вирусной ДНК, Тестируемых мышей иммунизировали Е. соli-плазмидой, несушей кДНК нуклеопротеина вируса гриппа А под контролем промотора вируса саркомы Рауса. Контрольным мышам вводили только плазмидную ДНК, По оси абсцисс отложено время, прошедшее после контакта животных с вирусом гриппа. |
Штаммы с мутацией в asd-гене растут только в присутствии диаминопимелиновой кислоты и их можно использовать для доставки плазмидной ДНК в эпителиальные клетки животных, поскольку они в них не пролиферируют.
Эксперименты, в которых в качестве вектора для доставки ДНК в клетки использовалась SftigeHa, были проведены на морских свинках, и хотя они оказались успешными, судить о безопасности данной системы можно будет лишь после проведения клинических испытаний. Огромным преимуществом этого подхода является возможность перорального введения вакцин.
Аттенуированные вакцины
В некоторых случаях в качестве живых вакцин можно использовать генетически модифицированные (рекомбинантные) микроорганизмы (бактерии или вирусы). Такие вакцины содержат либо непатогенные микроорганизмы, синтезирующие антигенные детерминанты определенного патогенного агента, либо штаммы патогенных микроорганизмов, у которых модифицированы или делетированы гены вирулентности, В этих случаях основные антигенные детерминанты являются составными компонентами бактериальных или вирусных частиц и имеют такую же конформацию, какую они принимают в болезнетворном микроорганизме. Изолированный же антиген часто утрачивает исходную конформацию и вызывает лишь слабый иммунный ответ.
Вакцины 235

|
| Иммунизация с помощью пептида, синтезированного исходя из данных о нуклеотидной последовательности РНК вируса ящура J. L. Bittle, R. A. Houghten, H. Alexander, T. M. Shinnick, J. G. Sutcliffe, R. A. Lerner, D. J. Rowlands, F. Brown Nature 298: 30-33, 1982 |
| Начиная с первой вакцины, созданной Дженнером более 200 лет назад, большинство человеческих противовирусных вакцин содержали убитые или аттенуированные патогенные вирусы или сходные с ними непатогенные штаммы. Этот подход достаточно эффективен и предотвращает распространение ряда вирусных инфекций, однако его применение ограничено по ряду причин: не все вирусы могут расти в культуре, что не позволяет создавать вакцины против них; производство традиционных вакцин - дорогостоящая и потенциально опасная процедура; не все вирусные заболевания можно предотвратить с помощью традиционных вакцин. С развитием молекулярной биотехнологии во многих лабораториях были предприняты попытки создания более безопасных и | эффективных и в то же время менее дорогих вакцин, не имеющих ограничений в применении. Введение вакцины индуцирует выработку антител к антигенным детерминантам, в норме присутствующим на поверхности вирусной частицы, поэтому разумно было предположить, что аналогичный иммунный ответ могут вызвать короткие синтетические пептиды с такой же аминокислотной последовательностью, как у вирусной антигенной детерминанты. Конечно, такой подход применим лишь в том случае, когда антигенная область представляет собой короткий, но непрерывный домен. Биттл и др. выделили и охарактеризовали РНК вируса ящура и определили аминокислотную последовательность основного вирусного белка — VP1. Проведя | соответствующие эксперименты, они пришли к выводу, что его антигенные детерминанты находятся на N- или С-конце белковой молекулы. Определив их аминокислотные последовательности, они синтезировали серию пептидов, которые сшили с белками-переносчиками и ввели кроликам. В ответ на иммунизацию С-концевыми пептидами VP1 у кроликови морских свинок вырабатывались антитела, защищающие их от инфекции интактным вирусом ящура. Эта работа показала, что для индукции синтеза антител, нейтрализующих ин-тактные вирусные частицы, достаточно одного (или нескольких) домена (доменов) специфического вирусного белка, и, следовательно, можно создавать вакцины нового типа, не содержащие патогенных вирусов. |
Противохолерные вакцины
Живые вакцины, как правило, гораздо более эффективны, чем неживые или субъединичные. Основное требование, предъявляемое к ним, -отсутствие в инокуляционном материале вирулентных микроорганизмов. Это требование учитывалось и при создании живой противохолерной вакцины. Холера — быстро развивающаяся кишечная инфекция, характеризующаяся лихорадкой, диареей, болью в животе, дегидратацией; передается через питьевую воду, загрязненную фекалиями. В развивающихся странах, где системы очистки воды и удаления сточных вод недостаточно развиты, угроза холеры вполне реальна. Возбудителем холеры является Vibrio choierae. Бактерия размножается в тонком кишечнике и выделяет в большом количестве энтеротоксин, который и ответствен за патогенный эффект. Энтеротоксин — это гексамерный белок: он состоит из одной субъединицы А, которая обладает ADP-рибозилирующей активностью и стимулирует аденилатциклазу, и пяти субъединиц В, которые специфически связываются с клеточным рецептором слизистой кишечника. Субъединица А имеет два функциональных домена: А1, обладающий токсической активностью, и А2, отвечающий за ее связывание с субъединицами В. В настоящее время используется противохолерная вакцина, содержащая убитые фенолом холерные вибрионы; она обеспечивает только частичную защиту от инфекции и лишь в течение 3—6 мес. Поэтому были предприняты попытки создать другие типы противохолерной вакцины.
Как показали проведенные ранее исследования, субъединичная вакцина, содержащая инак-тивированный холерный энтеротоксин, не приводит к выработке полноценного иммунитета.
Дата добавления: 2015-07-14; просмотров: 788;
