Термодинамика гальванического элемента.
На Е влияют следующие факторы: температура, природа реагирующих веществ, концентрация реагирующих веществ.1. Природа реагирующих веществ:
1) 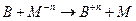
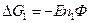 n – валентность, Ф – число Фарадея
n – валентность, Ф – число Фарадея
2) 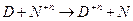
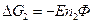 Работе противостоит сила внешнего давления.
Работе противостоит сила внешнего давления.
2.Влияние температуры на Э.Д.С.
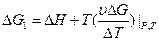
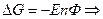
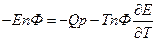
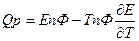
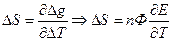 - изменение энтропии. Если
- изменение энтропии. Если 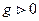 то
то 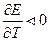 Если
Если 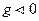 то
то 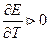
3. Зависимость Е от концентрации
Пусть в гальваническом элементе протекает реакция следующего типа:
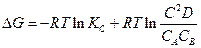 где С – концентрация
где С – концентрация
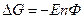 левую и правую части делим на
левую и правую части делим на 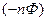
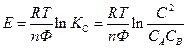
Если температура постоянная, то 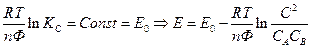
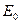 - стандартная Э.Д.С., соответствующая тому простому случаю, когда
- стандартная Э.Д.С., соответствующая тому простому случаю, когда 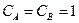
Для стандартных условий: Т=298 К, р=1атм 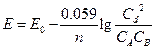 - уравнение Нериста для гальванического элемента. Ф = 96500
- уравнение Нериста для гальванического элемента. Ф = 96500 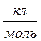
14.5. Водородный электрод сравнения и измерение ЭДС..Водородный электрод сравнения удобен тем, что стандартный электродный потенциал водорода равен нулю. φ02H+|H2= 0,00В.Водородный электрод представляет собой сосуд, в котором находится H2SO4 с концентрацией [H+] = 1 моль/л. Электрод выполняется из платины, которая сверху покрыта слоем рыхлой платины. Платина, особенно рыхлая, является прекрасным адсорбентом газообразного водорода. Извне в этот сосуд подается газообразный водород под давлением в 1атм. Платиновый электрод поглощает водород и практически становится водородным электродом. Электроды сравнения необходимы по той причине, что не существует методов непосредственного измерения электродных потенциалов. Возможно только измерение ЭДС гальванического элемента и вычисление неизвестного потенциала по известному. Для определения потенциалов электродов по водородной щкале собирают гальванический элемент, одним из электродов которого является измеряемый, а вторым –стандартный водородный электрод с электродом из того металла, потенциал которого необходимо измерить.
Измерение ЭДС данного гальванического элемента производится компенсационным методом. Схема включает в себя реохорд, рис.3. 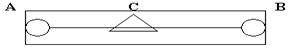
Реохорд - длинная деревянная линейка, по краям которой находятся металлические зажимы, между зажимами туго натянута стальная струна определенного сопротивления. По струне перемещается металлический движок. В схему включены аккумулятор и гальванометр. Движок реохорда перемещают до тех пор, пока стрелка гальванометра не остановится на нуле. Это - состояние компенсации, для которого справедливо соотношение:
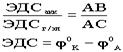 ,где ЭДСакк- ЭДС аккумулятора, ЭДСг/эл - ЭДС гальванического элемента, AB - длина линейки, AC - расстояние до движка (состояние компенсации).
,где ЭДСакк- ЭДС аккумулятора, ЭДСг/эл - ЭДС гальванического элемента, AB - длина линейки, AC - расстояние до движка (состояние компенсации).
14.6.Потенциал редокси-электродов. 

Концентрационные гальванические элементы
Особенностью концентрационного гальванического элемента является то, что оба электрода выполнены из одного и того же метала. Эти электроды отличаются друг от друга только концентрациями солевых растворов.
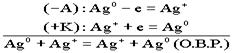 . По формуле Нерста рассчитаем ЭДС концентрационного элемента.
. По формуле Нерста рассчитаем ЭДС концентрационного элемента. 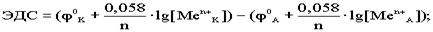
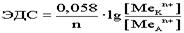 Недостатки концентрационных гальванических элементов: разрушаемый анод, малая ЭДС. Концентрационные элементы используются в тех случаях, где необходима малая ЭДС. Окислительно - восстановительные (ОВ) гальванические элементы:Особенностью данных элементов является то, что окислительно - восстановительный процесс протекает только в растворах. Оба электрода являются инертными, или пассивными, т.е. сами они не принимают участия в ОВ процессах, а выполняют роль проводников электронов.
Недостатки концентрационных гальванических элементов: разрушаемый анод, малая ЭДС. Концентрационные элементы используются в тех случаях, где необходима малая ЭДС. Окислительно - восстановительные (ОВ) гальванические элементы:Особенностью данных элементов является то, что окислительно - восстановительный процесс протекает только в растворах. Оба электрода являются инертными, или пассивными, т.е. сами они не принимают участия в ОВ процессах, а выполняют роль проводников электронов. 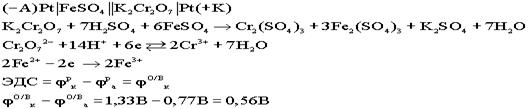
Топливные элементы(ТЭ)Электрохимические реакции очень медленные. Для ускорения процессов советский инженер Давтян предложил ввести в окислительно – восстановительные гальванические элементы катализаторы. Суть топливных элементов заключается в том, что электроды являются одновременно и катализаторами. Топливо, т.е. восстановитель и окислитель, хранится вне гальванических элементов и подаётся на электроды по мере необходимости, рис.2.  Электроды выполняются из пористого Ni или пористой Pt, то есть тех металлов, которые являются катализаторами электродных процессов. В качестве электролита используется раствор гидроксида калия.
Электроды выполняются из пористого Ni или пористой Pt, то есть тех металлов, которые являются катализаторами электродных процессов. В качестве электролита используется раствор гидроксида калия.
Схема кислородно- водородного ТЭ может быть записана в виде: 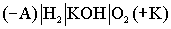 .
.
На аноде элемента протекает реакция окисления водорода:
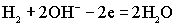 .На катоде восстанавливается кислород:
.На катоде восстанавливается кислород:
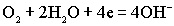 .Суммированием анодной и катодной реакций получаем уравнение токообразующей реакции:
.Суммированием анодной и катодной реакций получаем уравнение токообразующей реакции: 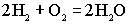 ,в результате которой химическая энергия непосредственно превращается в электрическую.Пример применения топливных элементов - использование их в мобильниках фирмы Toshiba.
,в результате которой химическая энергия непосредственно превращается в электрическую.Пример применения топливных элементов - использование их в мобильниках фирмы Toshiba.
Дата добавления: 2015-08-08; просмотров: 1873;
