Липиды, классификация, отдельные представители. Фосфолипиды как структурные компоненты клеточных мембран. Пероксидное окисление липидов
Название липиды произошло от греческого слова lipos – жир. Под термином липиды объединяют большую и разнородную группу веществ – жиры и жироподобные вещества, являющиеся органическими соединениями растительного и животного происхождения, различающиеся по составу, но близкие по физико-химическим свойствам. Липиды не растворимы в воде, но хорошо растворяются в неполярных органических растворителях, таких как диэтиловый эфир, бензол, петролейный эфир и др. В живых организмах липиды выполняют следующие функции:
- липиды являются структурными компонентами биологических мембран, обеспечивают их полупроницаемость;
- липиды – форма, в которой организм запасает энергию;
- липопротеиды – транспортная форма липидов, в которой транспортируется запасенная энергия;
- липиды – растворители жирорастворимых витаминов;
- липиды выполняют терморегуляторную функцию;
- липиды образуют защитный слой на клеточных стенках бактерий, листьях высших растений, на коже позвоночных, выполняя т.о. защитную функцию.
Классификация липидов представлена на схеме:
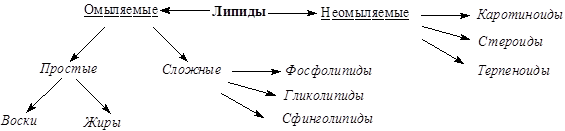
По отношению к гидролизу липиды делят на омыляемые и неомыляемые. К омыляемым липидам относятся вещества, которые гидролизуются водными растворами щелочей (подвергаются омылению). В химическом плане омыляемые липиды являются сложными эфирами. Простые липиды являются двухкомпонентными, так как при щелочном гидролизе образуются два класса органических соединений – спирт и соль карбоновой кислоты. Три и более продукта, относящиеся к разным классам органических веществ, образуются при гидролизе сложных липидов. Таким образом, сложные липиды состоят из трех и более компонентов. Неомыляемые липиды не подвергаются гидролизу и относятся к однокомпонентным соединениям.
Воски представляют собой сложные эфиры, образованные высшими насыщенными жирными кислотами и высшими насыщенными спиртами:

Воски – исторически сложившееся название разных по составу и происхождению продуктов, преимущественно природных, которые по свойствам близки пчелиному воску. Природные воски представляют собой пластичные легко размягчающиеся при нагревании продукты, большинство из которых имеет температуру плавления в интервале 40-90°С. Большинство природных восков содержит сложные эфиры одноосновных насыщенных кислот нормального строения и спиртов с 12-46 атомами углерода в молекуле. Такие воски по химическим свойствам близки к жирам, но омыляются только в щелочной среде.
Жиры – это вещества животного, растительного и микробного происхождения, состоящие в основном (до 98%) из триглицеридов (триацилглицеринов) – полных эфиров глицерина и жирных кислот. В составе жиров содержатся также ди- и моноглицериды (1-3%), фосфолипиды, гликолипиды (0,5-3%), свободные жирные кислоты, стерины и их эфиры (0,05-1,7%), красящие вещества (каротин, ксантофил), витамины А, D, Е и К, полифенолы и их эфиры. Жиры, как и воски, являются двухкомпонентными системами:
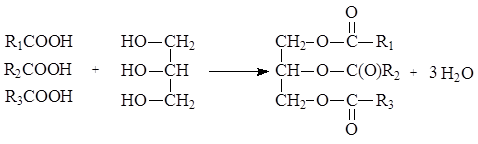
Химические и биологические свойства жира определяются входящими в его состав триацилглицеринами и в первую очередь длиной цепи, степенью ненасыщенности остатков жирных кислот и их расположением в триглицериде. В состав жиров входят в основном неразветвленные углеводородные радикалы жирных кислот, содержащие четное число атомов углерода (от 4 до 26), как насыщенные, так и моно- и полиненасыщенные. Наиболее часто в составе жиров встречаются миристиновая, пальмитиновая и стеариновая кислоты – представители насыщенных одноосновных карбоновых кислот, и олеиновая, линолевая, линоленовая – представители ненасыщенных одноосновных карбоновых кислот.
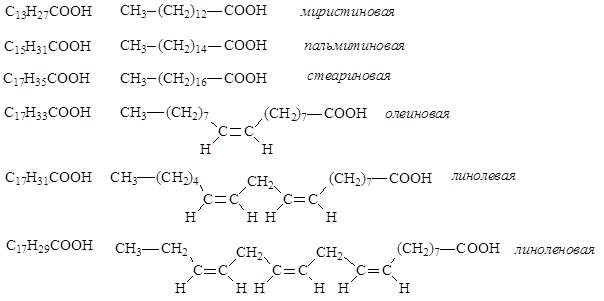
Почти все ненасыщенные кислоты, входящие в состав жиров растительного происхождения, и большинство ненасыщенных кислот, входящих в состав жиров животного происхождения, являются цис-изомерами. Жидкие смешанные триацилглицерины растительного происхождения называют маслами (оливковое, льняное, конопляное и т.д.).
Химические свойства триацилглицеринов
Триацилглицерины, как сложные эфиры, подвергаются гидролизу в щелочной (необратимый) и кислой (обратимый) средах. В организме гидролиз происходит под действием ферментов, называемых липазами, которые активируются желчными кислотами.
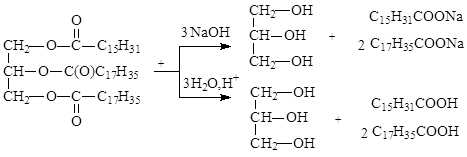
Триацилглицерины, содержащие остатки ненасыщенных жирных кислот, могут вступать в реакции присоединения и окисления по двойным связям, как алкены. При гидрогенизации растительных масел получают твердый продукт, называемый саломас, и используемый для изготовления маргарина.
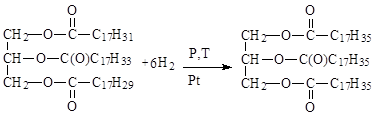
Степень ненасыщенности триацилглицеринов характеризуется йодным числом, которое показывает максимальную массу йода, которая может присоединиться к 100 г жира.
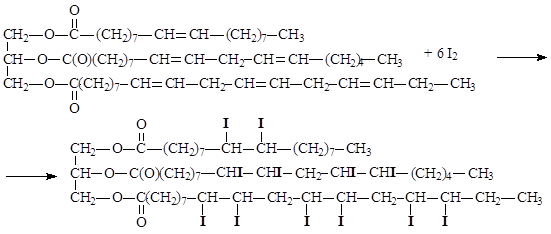
Чем больше значение йодного числа, тем выше степень ненасыщенности триацилглицерина. Ненасыщенные триацилглицерины подвергаются окислению кислородом воздуха, этот процесс сопровождается гидролизом сложноэфирных связей. Окисление двойных связей, сопровождаемое гидролизом, является составной частью процесса прогоркания жиров. Остатки ненасыщенных кислот, входящие в состав липидов, и сами ненасыщенные кислоты окисляются под действием водного раствора перманганата калия с образованием диольных фрагментов по месту двойных связей, окисление в жестких условиях приводит к разрыву двойных связей и образованию карбоновых кислот с меньшим числом атомов углерода.
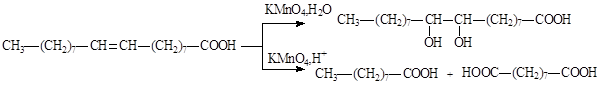
Фосфолипиды представляют собой, также как и жиры, сложные эфиры глицерина. В отличие от триацилглицеринов, третья спиртовая группа глицерина связана не с карбоновой кислотой, а с фосфорной. Другая особенность фосфолипидов состоит в том, что остаток фосфорной кислоты связан сложноэфирной связью с аминоспиртом. Фосфолипиды являются производными фосфатидной кислоты, которая образуется в результате этерификации двух ОН групп глицерина жирными карбоновыми кислотами, а третья ОН группа глицерина этерифицируется фосфорной кислотой.
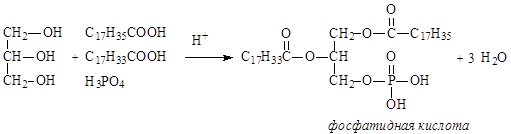
В зависимости от того, какой аминоспирт образует сложный эфир с фосфатидной кислотой, различают фосфатидилколамины (коламинкефалины), фосфатидилсерины (серинкефалины), фосфатидилхолины (лецитины).

В условиях организма третья гидроксильная группа фосфорной кислоты ионизирована, как и другие ионогенные группы.

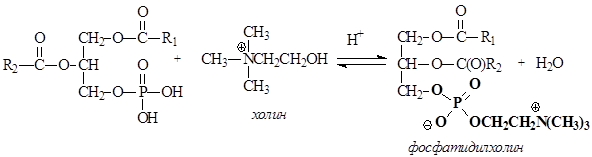
Фосфолипиды являются бифильными веществами, так как содержат в своей структуре неполярные углеводородные радикалы карбоновых кислот (гидрофобная часть) и полярный ионизированный фрагмент, образованный аминоспиртом и фосфорной кислотой (гидрофильная часть), который в формулах выделен жирным шрифтом. Благодаря бифильности, фосфолипиды частично растворимы в воде и способны транспортироваться кровью из печени в органы и ткани, где формируют структуру клеточных мембран.
Как сложные эфиры, фосфолипиды подвергаются гидролизу в кислой или щелочной средах:
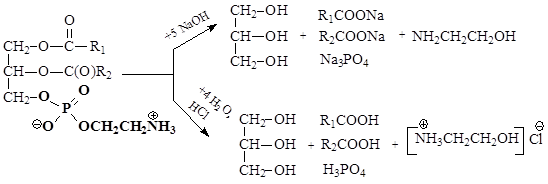
Сфинголипиды, – какпредставители сложных липидов, - представляют собой многокомпонентные соединения. Они являются сложными эфиры двухатомного аминоспирта сфингозина с высшими насыщенными и ненасыщенными кислотами и фосфорной кислотой, которая, в свою очередь, образует также сложноэфирную связь с аминоспиртом.
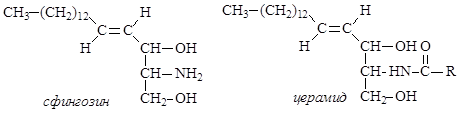
В нервных тканях обнаружены производные сфингозина – сфингомиелины. При гидролизе сфингомиелины образуют одну молекулу жирной кислоты, одну молекулу сфингозина, одну молекулу азотистого основания (чаще это холин) имолекулу фосфорной кислоты. Именно поэтому сфингомиелины относятся к классу фосфолипидов.
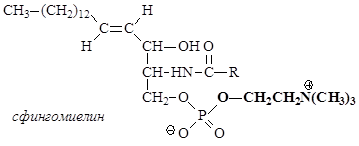
Сфингомиелины являются наиболее распространенными сфинголипидами. Они в основном находятся в мембранах животных и растительных клеток. Особенно богата ими нервная ткань; сфингомиелины обнаружены также в ткани почек, печени и других органов.
Гликолипиды – многокомпонентные соединения, являющиеся производными сфингозина, не содержащими фосфорной кислоты и холина, но содержащие в своем составе углеводный фрагмент. Аминогруппа сфингозина ацилирована высшей жирной кислотой, а гидроксильная группа у первого атома углерода сфингозина связана с остатком углевода (моносахарида или олигосахарида).

Гликолипиды играют существенную роль в функционировании биологических мембран. Они содержатся преимущественно в ткани мозга, но имеются также в кровяных клетках и других тканях. Известны три основные группы гликолипидов: цереброзиды, ганглиозиды и сульфатиды. В состав цереброзидов входят гексоза (обычно D-галактоза), которая связана гликозидной связью со сфингозином. Кроме того, в состав цереброзида входит жирная кислота, имеющая 24 углеродных атома. Сульфатиды отличаются от цереброзидов тем, что содержат в молекуле остаток серной кислоты, т.е. представляют собой цереброзид, в котором у третьего углеродного атома гексозы образуется сложноэфирная связь с серной кислотой. В мозге млекопитающих сульфатиды, как и цереброзиды, находятся в белом веществе. Однако их содержание в мозге намного ниже, чем цереброзидов. Ганглиозиды в структурном отношении сходны с цереброзидами с той лишь разницей, что вместо одного остатка галактозы они содержат сложный олигосахарид. В отличие от цереброзидов и сульфатидов, ганглиозиды находятся преимущественно в сером веществе мозга и сосредоточены в плазматических мембранах нервных и глиальных клеток.
Фосфолипиды, являясь бифильными веществами, выступают как эмульгаторы на границе раздела фаз. Как и мыла, молекулы фосфолипидов в контакте с водой стремятся расположиться так, чтобы неполярные углеводородные цепи находились в контакте только с другими аналогичными цепями. Таким образом формируется двойной слой толщиной в две молекулы. Такие липидные бислои, содержащие включения мембранных белков, составляют основу клеточных мембран.

Гидрофобные участки мембранных белков размещаются во внутренней полости мембраны, а ионизированные остатки аминокислот находятся на ее поверхности. Вода может проходить через такой двойной слой, а большие полярные молекулы и ионы не проходят. Таким образом, мембраны сохраняют концентрационные различия между различными частями клетки или между клеткой и ее водным окружением. Тонкие различия в физических свойствах клеточных мембран контролируются степенью ненасыщенности остатков жирных кислот в молекулах фосфолипидов. Мембраны, состоящие из ненасыщенных фосфолипидов, являются более мягкими (низкие температуры плавления) и позволяют молекулам проходить через них быстрее, чем через аналогичные мембраны, построенные из сложных эфиров насыщенных кислот. Чтобы полярные вещества и ионы могли пройти через внутреннюю полость мембраны, необходимо участие в этом процессе мембранных белков.
Наряду с процессами нормальной жизнедеятельности в клетке происходят процессы, связанные с нарушением тех или иных функций отдельных ее частей. Одним из процессов «мембранной патологии» является повреждение клеточных мембран, возникающее при воздействии ионизирующих излучений, авитаминозах, отравлениях.
Основной причиной повреждения клеточных мембран является пероксидное (перекисное) окисление липидов, инициируемое свободными радикалами. Свободные радикалы в организме образуются при окислении ионов Fe2+ кислородом или гидропероксидами:
Fe2+ + O2 + H+ ® Fe3+ + H-O-O× +
Fe2+ + R-O-O-H ® Fe3+ + HO- + R-O×
Свободные радикалы возникают и в результате воздействия на клетку ионизирующих излучений. В такой сложной среде, как живая материя, молекулы, являющиеся наиболее распространенными, больше других подвергаются воздействию ионизирующих излучений. При облучении живой материи, на 70-90% состоящей из воды, большая часть энергии излучения будет поглощаться молекулами воды. Рентгеновские лучи, g-излучение, нейтроны сами по себе не вызывают ионизации. Ионизация производится почти исключительно быстрыми заряженными частицами. Рентгеновские лучи, g-излучение, нейтроны называются «ионизирующими» потому, что при прохождении через вещество они вызывают образование быстрых заряженных частиц. Таким образом, особенности воздействия этих излучений связаны с их вторичным действием. В результате действия ионизирующего излучения в воде появляются первичные продукты радиолиза воды – возбужденные молекулы воды, электроны и катион-радикалы Н2О+ :
Н2О ® Н2Ó+ + е-
Н2О ® Н2О*
Возбужденные молекулы воды дезактивируются соседними молекулами, однако часть из них распадается на атомы водорода и гидроксильный радикал, или на атом кислорода и молекулу водорода. Образовавшиеся электроны «тормозятся» кулоновским полем «материнских» положительных зарядов, сольватируются и превращаются в частицы радикального характера – гидратированные электроны е- ×Н2О:
Н2О* ® Н× + ×ОН Н2О* ® Н2 + О
Н2О + е- ® е-×Н2О или Н2О-
Н2О+ + Н2О ® Н3О+ + ×ОН
Гидратированные электроны и катион-радикалы воды являются неустойчивыми частицами и далее подвергаются диссоциации с образованием свободного радикала и иона:
е- ×Н2О или H2О- ® Н× + ОН-
Н2Ó+ ® Н+ + ×ОН
Образовавшиеся продукты могут реагировать друг с другом или с молекулами воды:
Н× + ×Н ® Н2 Н2О + Н× ® Н2 + ×ОН
Н× + ×ОН ® Н2О Н2О2 + ×ОН ® Н2О + НÓ2
НО× + ×ОН ® Н2О2 Н3О+ + ОН- ® 2Н2О
При радиолизе воды пероксидные радикалы исчезают в результате рекомбинации: НÓ2 + НÓ2 ® Н2О2 + О2.
В результате протекания указанных реакций в результате радиолиза воды образуются е- × Н2О, ×ОН, Н×, О, Н2О2, Н3О+ и ОН-. Радиационно-химический выход О весьма низок, вследствие чего его образованием при радиолизе воды можно пренебречь. Гидратированный электрон, радикалы Н× и ×ОН называют свободно-радикальными продуктами радиолиза воды, а Н2, О2, Н2О2 – молекулярными продуктами.
Гидроксильный радикал является эффективным окислителем, в реакциях с насыщенными органическими соединениями он реагирует, как правило, отщепляя атом водорода, с ненасыщенными – может присоединяться по двойной связи. В реакциях с ионами металлов переменной валентности гидроксильный радикал выступает как окислитель: Fe2+ + ×ОН ® Fe3+ + :ОН- ; Сr2+ + ×ОН ® Cr3+ + :ОН-
Процесс пероксидного окисления липидов можно разделить на три этапа:
I-й этап – инициирование. На этом этапе образуются свободные радикалы, которые атакуют атомы Н метиленовых групп СН2, находящихся в a-положении по отношению к двойной связи. В результате образуются свободные радикалы аллильного типа, стабилизированные р,p-сопряжением.
II-й этап – рост цепи. На этом этапе происходит взаимодействие аллильных радикалов с молекулами кислорода. В результате такого взаимодействия образуются пероксидные радикалы, которые, взаимодействуя с водой или другими водородсодержащими соединениями (RH), отщепляют от них атомы Н. При этом пероксидные радикалы превращаются в неустойчивые гидропероксиды, а из воды или водородсодержащих молекул образуются свободные радикалы (НО× или R×). Образующиеся радикалы (НО× или R×) далее участвуют в реакциях образования аллильных радикалов, т.е поддерживают первый этап реакции – инициирование.
III-й этап – разрыв связей углерод-углерод, находящихся в a-положении по отношению к двойной связи гидропероксидов, в результате чего образуются енолы и альдегиды, которые окисляются далее до соответствующих кислот.
Молекулу фосфолипида, содержащую остаток непредельной кислоты (в данном случае олеиновой), представим как сложный эфир следующим образом:
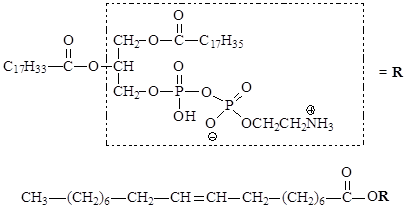
Тогда механизм пероксидного окисления липидов можно представить следующим образом:
Инициирование:
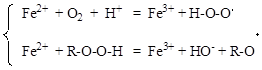
Рост цепи:
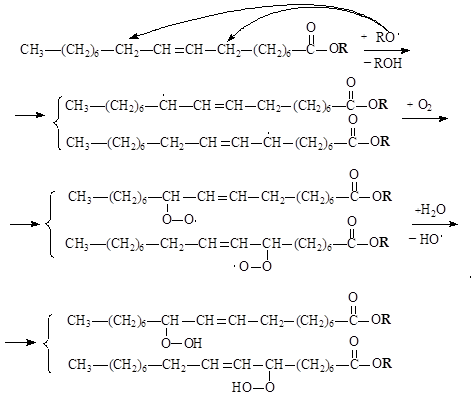
Разрыв углеродных связей:
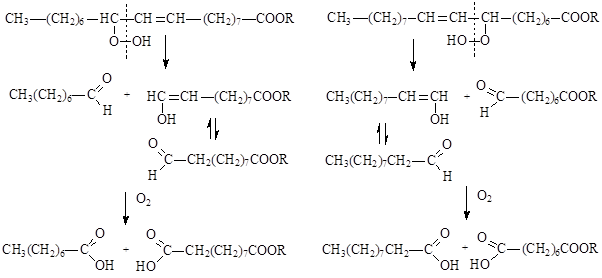
Глубина пероксидного окисления липидов зависит в первую очередь от состава липидов: с увеличением степени ненасыщенности жирных кислот, входящих в состав липидов, скорость окисления возрастает. Пероксидное окисление липидов приводит к повреждению клеточных мембран, структурными элементами которых являются липиды. Антиоксидантами по отношению к ненасыщеным липидам являются витамины группы Е – токоферолы, которые ингибируют процесс пероксидного окисления. Антиокислительная функция токоферолов определяется наличием подвижного атома Н и способностью реагировать с активными радикалами с образованием малоактивных радикалов, стабилизированных р,p-сопряжением.
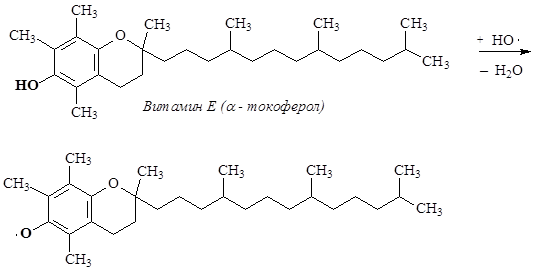
Дата добавления: 2015-08-08; просмотров: 8884;
