Реакции элиминирования у насыщенного атома углерода
Реакциям нуклеофильного замещения очень часто сопутствуют конкурирующие с ними реакции отщепления (элиминирования). Реакциям SN1 сопутствуют реакции мономолекулярного элиминирования Е1, реакциям SN2 сопутствуют реакции бимолекулярного элиминирования Е2. Это обусловлено основностью нуклеофильных частиц. Одна и та же частица может проявлять одновременно свойства основания (предоставлять пару электронов для образования связи с протоном) и свойства нуклеофила (предоставлять пару электронов для образования связи с электрофилом – атомом углерода, или другим атомом, имеющим частичный положительный заряд).
Реакции бимолекулярного элиминирования Е2
Если условия неблагоприятны для протекания реакции по механизму бимолекулярного нуклеофильного замещения, то можно ожидать, что основность нуклеофила, как донора пары электронов, определит направление реакции между субстратом и атакующей нуклеофильной частицей. В случаях, когда стерические препятствия затрудняют атаку нуклеофильной частицей атома углерода, нуклеофильная частица действует как основание и атакует С-Н кислотный центр в молекуле субстрата. Конечным итогом этой атаки на атом водорода будет b-элиминирование.
Общая схема механизма реакций Е2:
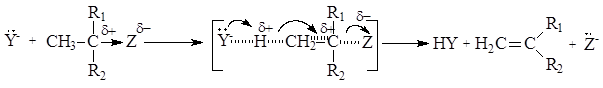
Реакции Е2 протекают через образование переходного состояния, в котором участвуют две частицы, при этом синхронно происходит образование s-связи Y-H и p-связи С=С и разрыв s-связей Н®С и С®Z. Скорость реакции зависит как от концентрации субстрата, так и от концентрации реагента. В качестве примера рассмотрим взаимодействие изопропилбромида и этоксида (этилата)натрия:
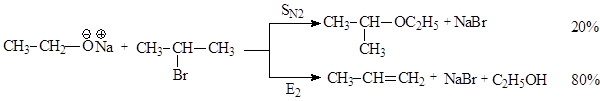
В молекуле субстрата вторичный атом углерода, связанный с двумя метильными группами, труднодоступен для нуклеофильной атаки этоксид-ионом, вследствие чего в результате реакции только 20% 2-бромпропана превращаются в 2-этоксипропан, являющийся продуктом реакции бимолекулярного нуклеофильного замещения. Более доступным для атаки этоксид-ионом является атом водорода в b-положении к уходящей группе (СН-кислотный центр):
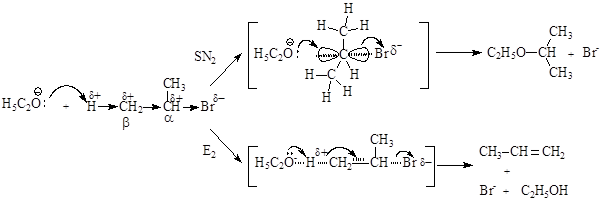
Этоксид-ион, атакуя атом водорода, выступает уже в качестве основания, так как предоставляет свою пару электронов для образования связи не атому углерода, а атому водорода. По мере образования связи О-Н синхронно происходит гетеролитический разрыв связи С-Н, высвобождающаяся пара электронов идет на образование p-связи между атомами углерода, что приводит к гетеролитическому разрыву связи С-Br и отщеплению иона брома.
Направление элиминирования. Правило Зайцева
При взаимодействии галогеналканов, содержащих различные типы b-водородных атомов, может образовываться несколько продуктов элиминирования. О преимущественном образовании одного из них говорит правило Зайцева: если в соединении все b-водородные атомы не могут стать одинаково доступными, то образующийся в результате элиминирования алкен содержит при двойной связи наибольшее число заместителей.
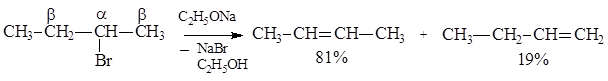
Реакции мономолекулярного элиминирования Е1
Реакциям мономолекулярного нуклеофильного замещения SN1 часто сопутствуют реакции мономолекулярного элиминирования Е1, что обусловлено наличием общей лимитирующей стадии – образование карбкатиона:
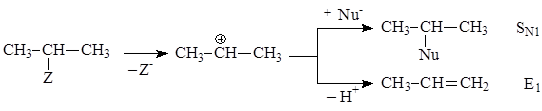
Алкилгалогениды, протонированные спирты и другие субстраты могут ионизироваться, образуя карбкатионы, которые затем, соединясь с нуклеофилом, завершают последовательность стадий SN1. Выход продукта в этих реакциях зачастую оказывается невысоким, основными побочными продуктами являются алкены.
Рассмотрим механизм элиминирования Е1 на примере катализируемой кислотами дегидратации спиртов:
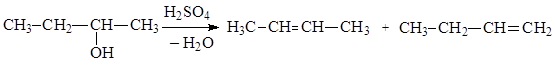
На первом этапе происходит протонирование атома кислорода гидроксильной группы, приводящее к превращению её в хорошо уходящую группу. Отщепление воды от оксониевого катиона приводит к образованию карбкатиона, который стабилизируется путем отщепления протона от возникающих СН-кислотных центров. В итоге реакции получится смесь двух алкенов, в которой будет преобладать более стабильный алкен, содержащий при двойной связи большее число заместителей.
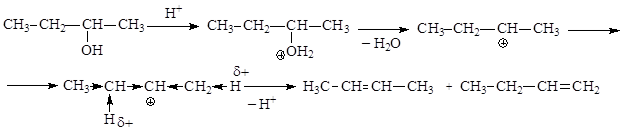
Таким образом, дегидратация спиртов протекает согласно правилу Зайцева, которое можно сформулировать и в таком виде: при дегидрогалогенировании несимметричных галогеналканов и дегидратации несимметричных спиртов атом водорода преимущественно отщепляется от менее гидрогенизированного атома углерода.
Лекция № 6
Дата добавления: 2015-08-08; просмотров: 3361;
