Дисперсные системы.
Дисперсные системы – это смесь веществ, то есть системы, содержащие много компонентов в общем случае, находящиеся в разных фазах: гомогенные, гетерогенные, их разделяют на макрогетерогенные и микрогетерогенные.
Макрогетерогенные системы– это системы имеющие сплошную поверхность раздела.
Микрогетерогенные системы – это системы имеющие прерывную поверхность раздела.
Большинство технических процессов связано с использованием дисперсных систем.
Дисперсные системы характеризуют величиной, которую называют дисперсность (дисперсия есть распределение).
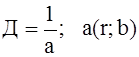 , где
, где
Д- дисперсность;
а – величина, характеризующая размер частиц;
r - радиус частицы;
l - длина волокна.
Дисперсная среда (ДС) – сплошная непрерывная дисперсной системы.
Дисперсная фаза (Дф) – фаза с прерывной поверхностью.
Молекулярные дисперсии – гомогенные дисперсии размер частиц, которых совпадает с размерами молекул и атомов – растворы.
Растворы.
Раствор - однородная смесь двух или более компонентов относительное содержание которых изменяется во всех объемных пределах и может изменятся в широких пределах.
Концентрация растворённого вещества – относительное содержание растворенного вещества в растворе. Так как содержание веществ характеризуется по массе, по количествам, по объёму и точно также отображает состояние растворителя, растворённого вещества, растворов.
1) Массовая доля растворённого вещества (ω(В), где В – формула растворённого вещества)
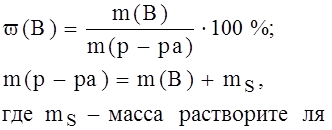
На практике можно измерить плотность любого раствора (ρ) используя ареометр.
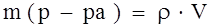
2) Молярная концентрация.
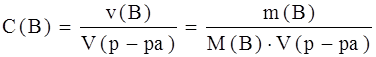
3) Ковалентная концентрация
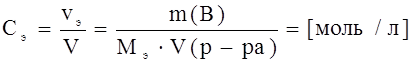
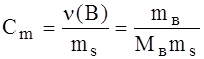 - моляльность.
- моляльность.
Применение закона эквивалента для реакции идущих в растворах.
Пример: реакция нейтрализации: ее используют для определения содержания кислот или щелочей в различных жидких системах, путем определения их концентрации.
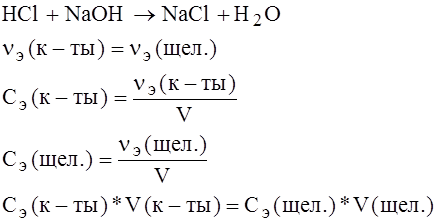
Дата добавления: 2015-08-08; просмотров: 1067;
