Стандартное состояние.
Чтобы сравнивать между собой тепловые эффекты различных реакций необходимо стандартизировать условия, в которых эти реакции протекают (исходные вещества взяты в стехиометрических отношениях ). Состояние каждого вещества создается как стандартное состояние. Это физическое состояние, в котором вещество более устойчиво, при P0=101кПа=1атм. и T=298К=25˚С.
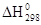 - тепловой эффект реакции протекающий при стандартных условиях.
- тепловой эффект реакции протекающий при стандартных условиях.
Термохимические уравнения –это уравнения химических реакций, в которых рядом с формулой участвующих реакций символом в скобках указывается состояние вещества (твердое – (т), кристаллическое – (к), жидкое – (ж), газообразное – (г), раствор – (р)) и после уравнения через точку с запятой указывается, величена теплового эффекта, при стандартных условиях.
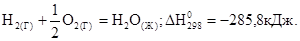
В данной реакции из простых веществ 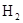 и
и 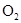 образуется сложное вещество
образуется сложное вещество 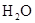 тепловой эффект таких реакций называется теплотой образования вещества.
тепловой эффект таких реакций называется теплотой образования вещества.
Стандартная терлота образования вещества ( 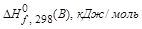 ) – это тепловой эффект образования 1 моль вещества из простых веществ, находящихся в стандартном состоянии.
) – это тепловой эффект образования 1 моль вещества из простых веществ, находящихся в стандартном состоянии.
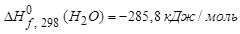 .
.
Стандартная теплота образования простых веществ условно принимается равной нулю. Стандартные теплоты образования сложных веществ имеются в справочной таблице.
Термохимические законы и расчёты по ним:
1. Закон Гесса.
Тепловой эффект реакции протекающий в несколько стадий равен сумме тепловых эффектов отдельных стадий.
Окисление графита.
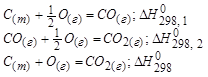
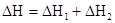
Следствие из закона Гесса:
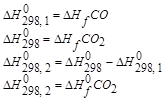
То есть тепловой эффект процесса зависит только от вида исходных веществ и продуктов реакций, но не зависит от пути перехода.
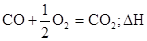
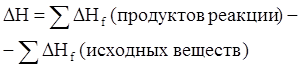
Тепловой эффект реакции равен разности сумм теплот образования продуктов реакции и исходных веществ. Теплоты образования участников реакции рассчитываются в последующем выражении с учетом коэффициента уравнения реакции. Последнее выражение используется для расчета тепловых эффектов химических реакций, протекающих при стандартных условиях, с использованием справочных данных, по стандартным теплотам образования участников реакций.
2. Закон Лавуазье-Лапласа.
Теплота образования вещества численно равна теплоте разложения вещества с противоположным знаком.
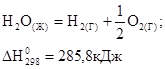
Направленность химических реакций.
aA+bB=cC+dD
Всякая химическая реакция обратима, т.е. может протекать как в прямом, так и в обратном направлении. Поэтому в реакционной смеси всегда присутствуют как исходные вещества, так и продукты реакции. Но отношение будет зависеть от условий, в которых находятся реагирующие вещества. Все реакции обратимы, но в определенных условиях они могут протекать в определенном направлении.
Термодинамика позволяет определить направление протекания данной реакции при данных условиях (при t=const и P=const). Самопроизвольно протекают процессы связанные с уменьшением свободной энергии системы. Исходя из этого, самопроизвольно могут протекать реакции в ходе, которых уменьшается свободная энергия системы. При экзотермической реакции теплосодержание уменьшается такие реакции должны идти самопроизвольно ( 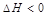 ), однако данный критерий не является единственным. Изменение свободной энергии определяется также величиной ещё одной термодинамической функции – энтропией. Можно привести пример реакций, которые являются экзотермическими, но самопроизвольно не протекают.
), однако данный критерий не является единственным. Изменение свободной энергии определяется также величиной ещё одной термодинамической функции – энтропией. Можно привести пример реакций, которые являются экзотермическими, но самопроизвольно не протекают.
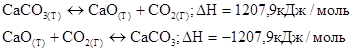
Следовательно, принцип Бертло-Томсона не распространяется на все реакции. Это объясняется тем, что изменение свободной системы связано не только с изменением ее теплосодержанием, но и с изменением энтропии.
Процессы могут протекать и без изменения внутренней энергии 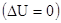 и без изменения теплосодержания
и без изменения теплосодержания 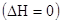 .
.
Энтропия (S, Дж/К) – это термохимическая функция, мера беспорядка системы, функция вероятности состояния системы. Таким образом, самопроизвольно идут процессы, в ходе которых энтропия увеличивается, то есть растет хаотизация. Обратный процесс требует затраты энергии.
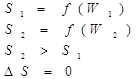
Самопроизвольно может протекать расширение газа в пустоту или в вакуум и процессы смешения.
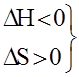 Критерии самопроизвольного
Критерии самопроизвольного
протекания процесса.
Стандартная энтропия вещества ( 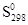 (В), Дж/моль*К) предназначена для сопоставления и определения энтропии в химической реакции. Можно оценить энтропию для 1 моль любого вещества для стандартных условий. Для энтропии соблюдаются следствия из закона Гесса.
(В), Дж/моль*К) предназначена для сопоставления и определения энтропии в химической реакции. Можно оценить энтропию для 1 моль любого вещества для стандартных условий. Для энтропии соблюдаются следствия из закона Гесса.
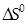 - изменение энтропии при стандартных условиях в ходе химической реакции.
- изменение энтропии при стандартных условиях в ходе химической реакции.
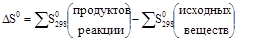
Изменение энтропии не зависит от способа перехода системы из начального состояния в конечное состояние, а определяется лишь исходным и конечным состоянием реагирующих веществ. И если 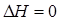 , то реакции идут самопроизвольно при условии, что
, то реакции идут самопроизвольно при условии, что 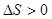 .
.
Энтропия вещества зависит от его физического состояния и при переходе из кристаллического в жидкое и газообразное энтропия будет увеличиваться. Энтропия пропорциональна температуре.
Изобарно-изотермический потенциал системы – это величина свободной энергии системы при постоянном давлении и температуре, при стандартных условиях, она обозначается G0. В ходе химической реакции имеет место изменение изобарно-термического потенциала.
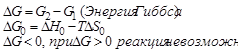
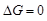 - состояние равновесия, т. е. прямой и обратный процесс протекает с одинаковыми скоростями и оба направления равновероятны. При
- состояние равновесия, т. е. прямой и обратный процесс протекает с одинаковыми скоростями и оба направления равновероятны. При 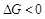 она может при данных температуре и давления протекать самопроизвольно, обратная реакция не возможна.
она может при данных температуре и давления протекать самопроизвольно, обратная реакция не возможна.
Дата добавления: 2015-08-08; просмотров: 2538;
