Основной закон термохимии (закон Гесса).
Тепловой эффект химической реакции не зависит от пути проведения процесса, числа и вида промежуточных стадий, а зависит только от начального и конечного состояния реагирующих веществ, при условии постоянства давления или постоянства объёма.
1-ое следствие закона Гесса. Тепловой эффект процесса равен сумме тепловых эффектов промежуточных стадий.
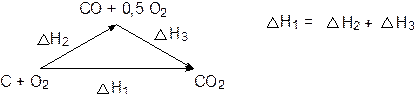
2-ое следствие закона Гесса.Тепловой эффект процесса равен алгебраической разности между суммой теплот образований продуктов реакции и суммой теплот образования исходных веществ, причём коэффициенты в уравнении учитываются как сомножители теплот образований.
сС + dD = аА + bВ;
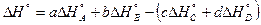 ;
;
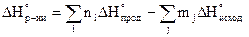
Пример расчёта теплового эффекта химической реакции:
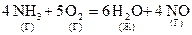 ; DН = ?
; DН = ?
| Вещество | ΔН0298, кДж/моль |
| NH3(г) | -46,2 |
| О2(г) | |
| Н2О(ж) | -285,8 |
| NO(г) | 90,3 |
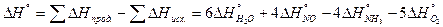 =
=
= 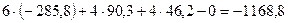 кДж.
кДж.
Дата добавления: 2015-08-08; просмотров: 1159;
