Хімічні основи виникнення та проведення нервових імпульсів
18.2.1. Роль нейромедіаторів у передачі нервових імпульсів. Зв’язок мільярдів нейронів мозку здійснюється за допомогою численних медіаторів (нейротрансміттерів): ацетилхоліну (Ах), норадреналіну (НА), дофаміну, адреналіну, серотоніну, гістаміну, ГАМК тощо. Одним з основних медіаторів у нервовій системі є ацетилхолін.
Ацетилхолін — це складний ефір оцтової кислоти та холіну. Він синтезується в нервовій клітині з холіну й активної форми ацетату — ацетил-КоА за допомогою спеціального ферменту холінацетилтрансферази (холінацетилази).
Передача імпульсів з нейрона на нейрон або з нейрона на ефекторний орган відбувається за допомогою синапса. Синапс можна уявити собі як вузький простір (щілину), обмежений з одного боку пресинаптичною, а з іншого – постсинаптичною мембраною (рис.18.4). Пресинаптична мембрана складається з внутрішнього шару, що належить цитоплазмі нервового закінчення, і зовнішнього, утвореного нейроглією. Мембрана в деяких місцях потовщена й ущільнена, в інших – тонша і має отвори для сполучення цитоплазми аксона з синаптичним простором. Постсинаптична мембрана менш щільна, не має отворів. Подібним чином побудовані і нервово-м’язові синапси, але вони мають складнішу будову мембранного комплексу.
Передачу нервового імпульсу за участі Ах можна відобразити наступним чином. У синаптичних нервових закінченнях є міхурці (везикули) діаметром 30 – 80 нм, що містять нейромедіатори.
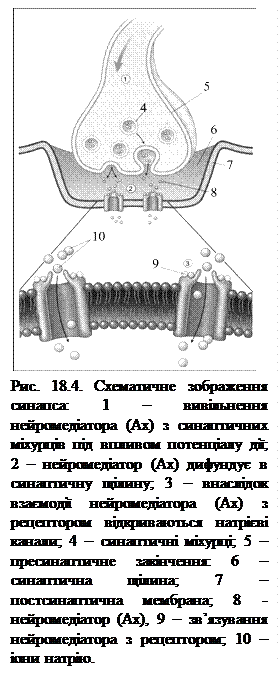 Ці везикули вкриті оболонкою, яка утворена білком клатрином (М.м. 180 000 Да). У холінергічних синапсах кожний міхурець діаметром 80 нм містить приблизно 40 000 молекул Ах. Під час нервового збудження вивільнення медіатора відбувається “квантами”, тобто шляхом повного випорожнення кожного окремого міхурця. За умов норми під впливом імпульсу виділяється приблизно 100 – 200 квантів медіатора. Ця кількість достатня для ініціації потенціалу дії в постсинаптичному нейроні. Відбувається це, очевидно, у такий спосіб: деполяризація мембрани синаптичних закінчень викликає швидкий потік іонів кальцію у пресинаптичну ділянку синапсу, тимчасове збільшення внутрішньоклітинної концентрації цих іонів стимулює злиття мембрани синаптичних міхурців із плазматичною мембраною й, у такий спосіб, запускає процес вивільнення їх вмісту. Виділений у синаптичну щілину Ах дифундує до постсинаптичної мембрани.
Ці везикули вкриті оболонкою, яка утворена білком клатрином (М.м. 180 000 Да). У холінергічних синапсах кожний міхурець діаметром 80 нм містить приблизно 40 000 молекул Ах. Під час нервового збудження вивільнення медіатора відбувається “квантами”, тобто шляхом повного випорожнення кожного окремого міхурця. За умов норми під впливом імпульсу виділяється приблизно 100 – 200 квантів медіатора. Ця кількість достатня для ініціації потенціалу дії в постсинаптичному нейроні. Відбувається це, очевидно, у такий спосіб: деполяризація мембрани синаптичних закінчень викликає швидкий потік іонів кальцію у пресинаптичну ділянку синапсу, тимчасове збільшення внутрішньоклітинної концентрації цих іонів стимулює злиття мембрани синаптичних міхурців із плазматичною мембраною й, у такий спосіб, запускає процес вивільнення їх вмісту. Виділений у синаптичну щілину Ах дифундує до постсинаптичної мембрани.
Взаємодія між рецептором і медіатором запускає низку реакцій, які змушують постсинаптичну нервову клітину або ефекторну клітину виконувати свою специфічну функцію.
Рецептор Ах – це трансмембранний олігомерний глікопротеїновий комплекс, який складається з 6 субодиниць: 2 – альфа, 2 – бета, 1 – гама і 1 – дельта. У присутності Ах бокові взаємодії між субодиницями підтримують канал у відкритому стані та створюють умови для транспорту іонів. За відсутності Ах змінюється орієнтація субодиниць і канал закривається. Щільність розташування білків-рецепторів у постсинаптичній мембрані дуже велика – біля 20 000 молекул на 1 мкм2. Просторова структура рецептора строго відповідає конформації медіатора. При взаємодії з Ах білок-рецептор так змінює свою конформацію, що,як зазначалося вище, всередині нього формується натрієвий канал. Його катіонна селективність обумовлена тим, що ворота каналу сформовані негативно зарядженими амінокислотами. У такий спосіб підвищується проникність постсинаптичної мембрани для натрію, виникає новий імпульс (або скорочення м’язового волокна). Деполяризація постсинаптичною мембрани викликає дисоціацію комплексу «Ах-білок-рецептор» і Ах вивільняється в синаптичну щілину, де за 40 мкс гідролізується.
Розщеплення Ах у холінергічних синапсах відбувається двома шляхами: перший –ферментативний, другий – енергозалежний активний транспорт Ах у нейрон, де він нагромаджується для наступного повторного використання.
Гідролітичний розпад Ах на оцтову кислоту і холін каталізується ферментом, що отримав назву ацетилхолінестераза.

Незворотне інгібування ацетилхолінестерази викликає смерть внаслідок зупинки дихання. Інгібіторами цього фермента є фосфорорганічні сполуки (хлорофос, дихлофос, табун, зарин, зоман, бінарні отрути), які ковалентно зв’язуються з серином у його активному центрі. Зворотні інгібітори ацетилхолінестерази використовують у якості лікарських препаратів для лікування глаукоми та атонії кишок.
У нервовій тканині існують й інші естерази, які можуть гідролізувати Ах, але значно повільніше, ніж, наприклад, бутирилхолін. Ці естерази називаються псевдохолінестеразами.
До числа холінергічних систем належать моторні нейрони, що утворюють нервово-м’язові веретена, усі прегангліонарні нейрони автономної нервової системи і постгангліонарні нейрони парасимпатичної нервової системи. Велика кількість холінергічних рецепторів виявлено також у різних відділах головному мозку. У залежності від чутливості до тої чи іншої групи хімічних сполук, холінергічні нейрони поділяють на мускаринові (активуються мускарином) і нікотинові (активуються нікотином) (табл. 18.4).
Таблиця 18.4. Функції мускаринових рецепторів мозку
| Тип рецептора | Функції |
| М1 | Беруть участь у деяких рухових і судомних процесах |
| М2 | Регулюють секрецію катехоламінів |
| М3 | Пригнічують апетит, індукують схуднення |
| М4 | Беруть участь у процесах формування пам’яті, гальмують деякі форми рухової активності, гальмують вихід ГАМК |
| М5 | Беруть участь у релаксації судин мозку |
Інгібітори мускаринових рецепторів (атропін, принзепін, скополамін) широко застосовують у якості лікарських засобів. Так, наприклад, атропін використовують для зняття м’язових спазмів, зниження стимульованої Ах секреції бронхіальних, потових і травних залоз. Проте слід зважати, що передозування атропіну може викликати рухове та мовне збудження.
Нікотинові рецептори мають обмеженіші функціональні можливості, відома їх участь у регуляції рухових функцій, просвіту судин мозку, їх синапси знаходяться у гангліях і скелетних м’язах.
Норадреналін – важливий медіатор, який синтезується з тирозину за участі фермента тирозингідроксилази, здебільшого, у нейронах симпатичної нервової системи. НА взаємодіє з a- і b-адренергічними рецепторами (табл. 18.5).
Таблиця 18.5. Фізіологічні ефекти норадреналіну
| Тип рецепторів | Вторинний месенджер | Ефект | Тип рецепторів | Вторинний месенджер | Ефект |
| α1 | ІФ3 | глікогеноліз ↑, звуження бронхів, перистальтика кишок↓, скорочення матки ↑ | β1 | цАМФ | Ліполіз ↑, стимуляція активності серця |
| α2 | цАМФ | ренін ↑, статева активність у чоловіків↓, перистальтика кишок↓, гіпотензія | β2 | цАМФ | Ліполіз ↑, глікогеноліз ↑, секреція інсуліну ↑, розширення бронхів і коронарних судин, скорочення матки ↓ |
| β3 | цАМФ | Ліполіз ↑ |
У метаболізмі катехоламінових медіаторів особлива роль належить ферменту моноаміноксидазі (МАО), який відщеплює аміногрупу в молекулах НА, серотоніну, дофаміну й адреналіну, у такий спосіб інактивуючи зазначені медіатори.
Серотонін. Нейрони, які містять цей медіатор, зосереджені в ядрах мозкового стовбура. Серотонін вважають поліфункціонльним нейромедіатором, оскільки він має велику кількість типів і підтипів рецепторів з найрізноманітнішою локалізацією (табл. 18.6).
Таблиця 18.6. Фізіологічні ефекти серотоніну в ЦНС
| Тип рецептора | Вторинний месенджер | Фізіологічний ефект |
| 5НТ1А | цАМФ | Пригнічення стану тривожності та депресії, агресивності, статевої активності, температури тіла. Підвищення апетиту, участь у механізмах сну та регуляції захисної поведінки, синтез мелатоніну в епіфізі |
| 5НТ1В | Посилення стану тривожності, спраги. Зниження апетиту | |
| 5НТ1D | Звуження базальних судин мозку, мігрень | |
| 5НТ2А | ІФ3, Са2+ | Моторне гіперзбудження, індукція елементів шизофренії, регуляція нейроторфінів |
| 5НТ2В | Пригнічення стану тривожності в процесі соціальної взаємодії, зниження спраги | |
| 5НТ3 | Nа+, K+ | Нудота, блювання, поглиблення алкоголізації, пригнічення формування пам’яті |
Дослідження, проведені з інгібітором синтезу серотоніну п-хлорфенілаланіном, а також з іншими інгібіторами, дають підстави вважати, що серотонін впливає на процеси сну. Індукторами сну також є g-аміномасляна кислота (ГАМК), ейкозаноїд D2, тоді як до пробуджувальних середників належать гістамін, дофамін (а також його аналоги та індуктори), ейкозаноїд Е2. На початку 50-х років фармакологи з’ясували, що відомий галюциноген диетиламін лізергінової кислоти (ЛСД) не тільки подібний за хімічною будовою до серотоніну, але і нейтралізує деякі його фармакологічні ефекти (блокуючи рецептори серотоніну). Тому було висловлено припущення, що порушення обміну серотоніну може бути причиною виникнення особливих психічних захворювань. Також відомо, що у людей співвідношення між певними субтипами рецепторів серотоніну та дофаміну (D2, 5HT2A, 5HT2C, D4) впливає на схильність до вживання алкоголю.
Гама-аміномасляна кислота (ГАМК) – важливий нейромедіатор, який утворюється при декарбоксилуванні глутамінової кислоти. ГАМК збільшує проникність постсинаптичних мембран для іонів калію і в такий спосіб віддаляє мембранний потенціал від граничного рівня, при якому виникає потенціал дії, викликаючи гальмування нервового імпульсу. Вона також посилює дихальну активність нервової тканини, покращує кровопостачання головного мозку. У формі фармпрепаратів (гамалон, аміналон) її застосовують при судинних захворюваннях головного мозку (атеросклероз, гіпертонія), порушеннях мозкового кровообігу, розумовій відсталості, ендогенних депресіях і травмах головного мозку, а також захворюваннях ЦНС, пов’язаних із надмірним збудженням кори мозку (епілепсії).
Глутаматміститься в головному мозку в дуже великій кількості (до 10 мкмоль/г тканини). Він є одним із основних збуджувальних медіаторів у корі, гіпокампі, смугастому тілі та гіпоталамусі; бере участь у регуляції процесів пам’яті, слугує складовою частиною глутатіону, у вигляді піроглутамату (циклічна форма) входить до низки нейропептидів (тиреоліберину, нейротензину, бомбезину тощо); слугує постачальником a-кетоглутарату для ЦТК, бере участь у знешкодженні аміаку. Порушення глутаматергічної системи відбувається при низці патологічних станів ЦНС: епілепсії, розладах вестибулярного апарату, ішемії тощо. Його застосовують при хронічній недостатності амінокислотного обміну, вегето-судинній дистонії, епілепсії (у якості попередника ГАМК – гальмівного медіатора).
Гліцин –найважливіший після ГАМК гальмівний нейромедіатор у спинному та проміжному мозку. Концентрація його у плазмі крові незначна, тому в мозок надходить недостатня його кількість. У мозку він може синтезуватися з глюкози, а розпад цієї амінокислоти відбувається трьома шляхами: шляхом перетворення на серин; розпадом до аміаку, оксиду вуглецю та метилен-Н4-фолату; окисненням під впливом оксидази амінокислот.
Гіпергліцинемія розвивається у ранньому дитячому віці і супроводжується епізодичним блюванням, пригніченням моторної активності, порушенням електроенцефалограми та часто закінчується летально.
18.2.2. Роль нейромедіаторів у регуляції пам’яті. Пам’ять не зосереджена в одній строго локалізованій ділянці мозку, як, наприклад, центр зору, слуху, мови тощо, пам’ять – це властивість усього мозку в цілому. Субстратом пам’яті людини є нейрони. Її не можна розглядати у відриві від діяльності людини, тому що не пізнання пізнає, не мислення мислить, не пам’ять запам’ятовує і відтворює, а пізнає, мислить, запам’ятовує і відтворює людина, визначена особистість.
В останні роки показано, що навчання тварини нових навичок проектується на хімізмі нейронів: змінюються кількість уридину в цитоплазматичній РНК, ступінь метилування ДНК і фосфорилування ядерних мембран. Застосування стимуляторів і речовин-попередників РНК полегшує навчання, а введення блокаторів синтезу РНК, навпаки, утруднює цей процес. Існують дані, що після запам’ятовування інформації змінюється антигенний склад нервової тканини. Прийнято виділяти декілька форм біологічної пам’яті: генетичну, імунологічну та нейрологічну. Біохімічні основи генетичної пам’яті пов’язані з ДНК клітини. Такою за складністю формою пам’яті є імунологічна пам’ять. Цей вид пам’яті хоч і включає елементи генетичної пам’яті, але знаходиться на вищому щаблі складності. Нарешті, система нейрологічної пам’яті ще складніша. Ця форма, своєю чергою, може бути розділена на короткочасну пам’ять (КП) і довготривалу (ДП) (рис. 18.5).
В основі КП, цілком ймовірно, лежить “циркуляція” інформації, яка отримана у вигляді імпульсів по замкнутих ланцюгах нейронів. При цьому синаптичний ефект, зміни ядерно-ядерцевого апарату, викид у цитоплазму нейрона біологічно активних речовин і супутні цим процесам перебудови обміну речовин клітини можна розцінювати як показники функціонування КП.
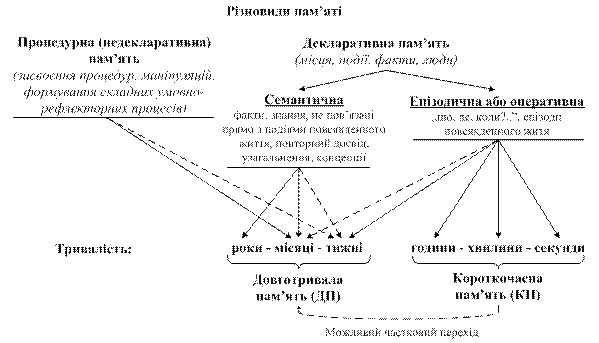
Рис. 18.5. Схематична класифікація пам'яті
Вмикання блоків ДП забезпечується приблизно через 10 хв після поступлення інформації в клітину. За цей час відбувається перебудова біологічних властивостей нервової клітини. Низка вчених вважають, що аферентна імпульсація, що приходить у нервові клітини під час навчання, викликає кількісну активацію синтезу РНК і білків, що може призводити до встановлення нових синаптичних зв’язків і перебудови існуючих або активація синтезу нуклеїнових кислот і білків носить цілеспрямований, специфічний характер, а синтезовані молекули є формою зберігання інформації (рис. 18.6).
Шлях формування ДП зв’язаний з унікальними рецепторами глутамату (у тому числі NMDA-рецепторами), для включення яких необхідне поєднання двох сигналів: повторної імпульсації нервових закінчень з виділенням у синаптичну щілину глутамату, який зв’яжеться з рецептором, і деполяризації постсинаптичної мембрани за рахунок імпульсів, які надходять ззовні до нейрона-реціпієнта і спричинюють виведення іонів Mg2+, які блокують канал рецептора (рис. 18.6). Далі іони Са2+, які заходять через відкритий канал, активують кальмодулінзалежну протеїнкіназу, яка забезпечує фосфорилування низки білків нейрона-реціпієнта. Одночасно відбувається автофосфорилування цього ензиму, завдяки чому підтримується його активність і активність нейрона-реціпієнта впродовж тривалого часу. Цей час відповідає тривалості пам’яті. Під впливом цАМФ відбувається керований розпад регуляторних субодиниць протеїнкінази А, що спричинює поступлення іонів Са2+ у нейрон у великій концентрації. Медіатора виділяється більше. У ядрі активований білок CREB-1 (фактор транскрипції) активує кілька генів ранньої відповіді. Відбувається зростання кількості синапсів, їх площі та формування нових рецепторів.
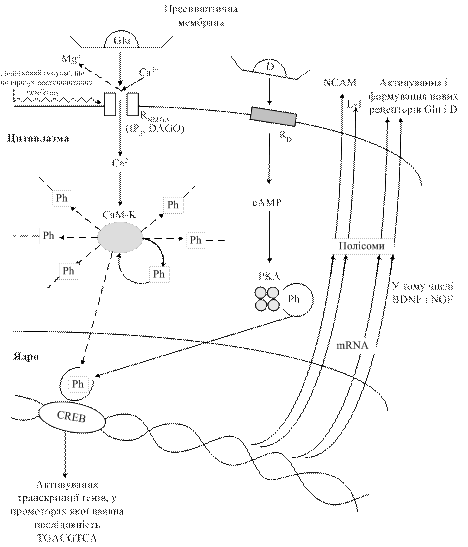
Рис.18.6. Формування довготривалої пам’яті (за И.П.Ашмариным, 2007): Сам-К – кальмодулінзалежна протеїнкіназа; РКА – протеїнкіназа, активована цАМФ; Рh – залишки ортофосфату; NCAM – молекули адгезії нейронів, у тому числі полімери сіалової кислоти – L-1; BDNF i NGF – нейротрофіни; CREB – цАМФзалежна ділянка зв’язуючого білка; NMDA – N-метил-D-аспартат (ділянка рецептора глутамату); IP3 – інозитол-3-фосфат; DAGO - [D-Аla, Phe, gly]-енкефалін
Процеси пам’яті тісно пов’язані з основними медіаторами (ацетилхоліном, норадреналіном, дофаміном, серотоніном, ГАМК). Наприклад, доведено, що зниження вмісту ацетилхоліну в мозку інгібіторами холінацетилази порушує навчання, а його підвищення прискорює напрацювання оборонних навичок. Серотонін полегшує формування та збереження навичок, заснованих на позитивному підкріпленні, і негативно впливає на формування оборонних реакцій. За існуючими уявленнями, норадренергічна і серотонінергічна системи є, значною мірою, антагоністами відносно процесів пам’яті. Можливо, вироблення навичок залежить не стільки від абсолютного рівня вмісту того або іншого медіатора, скільки від співвідношення активності цих систем. Варто зауважити, що існують численні дані, які свідчать про виражений гальмівний вплив ГАМК на процеси запам’ятовування та навчання.
Гормон задньої частки гіпофізу вазопресин також має яскраво виражений позитивний вплив на вироблення умовних реакцій у тварин. Стимуляція вазопресином процесів пам’яті не пов’язана з його гормональною дією, тому що таку ж стимулюючу дію мають деякі його аналоги і фрагменти, що не викликають властивих вазопресину гормональних реакцій. Є всі підстави вважати, що АКТГ і вазопресин не тільки стимулюють запам’ятовування при введенні їх ззовні, але постійно функціонують у мозку як регулятори процесів пам’яті (Ашмарін І.П. і ін., 1996). Кількість фармакологічних препаратів, спроможних стимулювати запам’ятовування, дуже велика. До специфічних стимуляторів традиційно належить пірацетам, на сьогоднішній день найпривабливішими вважають пептиди, що містять послідовність адренокортикотропін 4-7. прикладом стимуляторів формування пам’яті без впливу на базові механізми пам’яті вважать глюкозу, ω3-поліненасичені жирні кислоти, сумарні препарати РНК і ДНК.
18.2.3. Нейропептиди.Нейропептиди – широкий клас сполук пептидної природи, що синтезуються переважно в клітинах ЦНС, складаючи її пептидергічну систему, і здатні суттєво впливати на біохімічні та нейрофізіологічні процеси в головному мозку, а також регулюють як психофізіологічні, так і соматовегетативні функції організму. Найбільшу увагу привертають нейропептиди, що є ендогенними лігандами морфінових (опіатних) рецепторів мозку – опіоїдні пептиди. Вони, подібно до наркотичного анальгетика морфіну і близьких до нього сполук, взаємодіючи з опіоїдними рецепторами, мають сильно виражену знеболювальну активність і специфічну дію на головний мозок людини, що проявляється розвитком складного психоемоційного стану ейфорії з покращенням настрою, відчуттям душевного комфорту, позивним сприйняттям довкілля. Проте, вони мають суттєвий недолік – при застосуванні таких речовин можливе виникнення патологічної пристрасті (наркоманія і алкоголізм).
Пептиди з морфіноподібною активністю є похідними b-ліпотропного гормона гіпофізу. b-Ендорфін – це фрагмент b-ліпотропного гормона з 61 по 91 амінокислотний залишок, g-ендорфін – з 61 по 77, а a-ендорфін – з 61 по 76. Енкефаліни – також фрагменти b-ліпотропіну, але вони значно менші – пентапептиди. Вони легко руйнуються протеїназами, тому їх фармакологічний ефект незначний.
Здебільшого нейропептиди виконують функцію не лише нейромедіаторів, а й гормонів, до них належать нейрогіпофізарні гормони (вазопресин, ліберини, статини), гастроінтестинальні пептиди (гастрит, холецистокінін тощо), пептиди сну, пам’яті тощо (табл. 18.7).
Таблиця 18.7. Фізіологічні ефекти нейропептидів
| № з/п | Пептиди | Фізіологічні ефекти | |
| Опіоїди | Енкефаліни | Аналгезія (при центральному введенні), ко-трансміттер під час регуляції тонусу судин | |
| β-ендорфін | Аналгезія, індукція внутрішнього підкріплення | ||
| Ендоморфіни | Потужний аналгезуючий ефект | ||
| Ноціцептини | Посилення сприйняття болю | ||
| Брадикінін | Місцево – вазодилятація, посилення сприйняття болю, участь у запальному процесі; гіпотензія, участь у алергійних реакціях – спазм гладких м’язів бронхів, тонкої кишки, матки | ||
| Речовина Р | Участь у сприйнятті болю, у нейрогенному запаленні, антистресорна дія | ||
| Пептид дельта-сну (ПДС) | Посилення дельта-хвильового компоненту електроенцефалограми, супутнього сну | ||
| Нейротензини | Участь у системі «внутрішнього підкріплення», шляхом модулювання рівня дофаміну; анальгетики неопіоїдного типу, поєднання гіпотензивної та гіпотермічної дію; нейролептики | ||
| Ендотеліни ЕТ1 ЕТ2, ЕТ3 | Модулювання діяльності серця, нирок і скоротливості бронхів Вазоконстрикція Вазодилятація | ||
| Ангіотензин ІІ | Потужна вазоконстрикція, гіпертензивна дія, індукція виходу альдостерону, деяких простагландинів | ||
| Тіреоліберин | Індукція виходу тиреотропіну в гіпофізі, прямий вплив на низку функцій мозку, у тому числі на рівень позитивних емоцій і когнітивні процеси | ||
| Атріопептиди, натрій-уретичні пептиди (ANP, BNP, CNP) | Потужні натрійуретики (особливо ANP), гіпотензивні Стимулювання використання води (BNP, CNP) | ||
| Вазопресин Окситоцин Вазотоцин | Антидіуретичний, гіпертензивний Констрикція матки, секреція молока, індукція материнської поведінки Властивості вазопресину та окситоцину | ||
| Ко-кальцигенін (CGRP) | Потужний вазодилятатор, регулятор просвіту артеріол і кровопостачання органів, модулювання передачі сенсорних сигналів у ЦНС | ||
| Гонадоліберин | Стимулювання синтезу та виходу гонадотропінів (ЛГ і ФСГ), статевої поведінки | ||
| Нейропептид Y | Ко-трансміттер норадреналіну, індукує скорочення кровоносних судин, підвищення артеріального тиску, гальмування ефектів блукаючого нерва, пригнічення продукції антитіл (Ig G, Ig M) після імунізації | ||
| Ендозепіни | Індукування агресивної, проконфліктної поведінки, страх | ||
| Кортиколіберин | первинний індуктор стресу, тривоги, виходу проопіомеланокортину і його фрагментів | ||
| Адренокортико-тропін | Реалізація каскаду реакцій стресу, які запускаються кортиколіберином, шляхом стимулювання синтезу глюкокортикоїдів і мінералокортикоїдів; покращення запам’ятовування, продовження тривалості пам'яті, зниженняретроградної амнезії | ||
| Гастрин | Стимулювання секреції хлоридної кислоти та пепсиногену в шлунку | ||
| Холецистокінін-33 | Стимулювання скорочення жовчного міхура | ||
| Холецистокінін-8 | Пригнічення почуття голоду | ||
| Холецистокінін-4 | Індукування стану тривожності, панічного страху | ||
| Гастрит-рилізинг пептид | Стимулювання секреції інсуліну. Індукування вивільнення гастрину | ||
| Вазоактивний інтестинальний пептид | Розширення судин і бронхів, нейропротекція, стимулювання росту низки клітин, посилення секреції в тонкій кишці, стимулювання (через NO) ерекції, стимулювання статевої поведінки | ||
| Соматостатин | Гальмування активності гормону росту, регулювання тонусу судин слизової оболонки шлунка | ||
| Галанін | Інгібування холінергічної трансмісії в мозку, пригнічення розвитку судомних станів, стимулювання їжодобувної поведінки та скоротливості гладких м’язів травного тракту та сечо-статевої системи | ||
| Мотилін | Стимулювання перистальтики шлунка та дванадцятипалої кишки | ||
| Гліпроліни-2,3 | Гальмування згортання крові та тромбоутворення, захист слизової оболонки шлунка (антивиразкування) | ||
| Грелін | Участь у механізмах регулювання ваги тіла, стимулювання енергетичного метаболізму та вивільнення гормону росту | ||
| Дифенсини, протегрини | Забезпечення внутрішньоклітинного знищення бактерій і деяких вірусів |
Синтез нейропептидів відбувається двома шляхами – рибосомним і нерибосомним. Характерною особливістю генетично залежного синтезу нейропептидів є те, що на рівні геному клітини кодується його попередник, з якого потім утворюється нейропептид. Відщеплення амінокислот від молекули білка-попередника може відбуватися з N-кінця (за допомогою амінопептидаз) і з С-кінця (за допомогою карбоксипептидаз). Інактивація нейропептидів – ферментативна деградація.
Дата добавления: 2015-07-07; просмотров: 2585;
