Кинетика ферментативных процессов
В живой природе в процессах жизнедеятельности организма протекает огромное количество процессов связанных с синтезом и распадом различных веществ. Все процессы протекают с участием ферментов (энзимов). Фермент является биокатализатором процессов. Чаще всего ферменты - Это белки, либо нуклеиновые кислоты. Активность фермента определяется 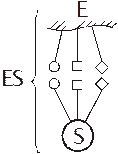 оптимальным условием PH среды, а также наличием ко-ферментов, ко-факторов, т. е. веществ, активизировающих работу фермента. Любые процессы связаны с биологической очисткой сточных вод,
оптимальным условием PH среды, а также наличием ко-ферментов, ко-факторов, т. е. веществ, активизировающих работу фермента. Любые процессы связаны с биологической очисткой сточных вод,
включая в себя ферментативные реакции.
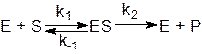 |
Простая ферментативная реакция выглядит следующим образом:
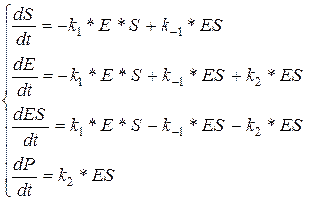 Где E -энзим, S –субстрат, (питательное вещество для организма),
Где E -энзим, S –субстрат, (питательное вещество для организма),
ES –субстратный комплекс, P –продукт реакции.
Скорость процессов зависит от скорости самой медленной (лимитирующей) реакции, т.е. от скорости распада фермент-субстатного комплекса.
Такую задачу можно решить, составив классическую кинетику, а также любую математическую модель, описывающую скорость образования продуктов, полученных при распаде фермент-субстатного комплекса.
Cкорость распада фермент-субстратного комплекса:
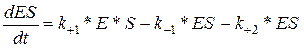 |
При максимальных скоростях в стационарном режиме:
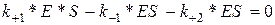 |
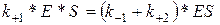 | 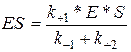 | ||
 Тогда получим концентрацию фермент-субстратного комплекса
Тогда получим концентрацию фермент-субстратного комплекса
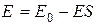 |
Где
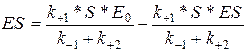
Тогда
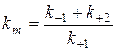 Обозначим:
Обозначим:
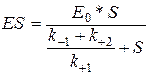 |

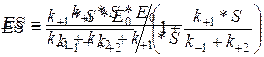 |
– константа Михаэлиса
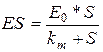 |
Тогда
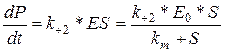 |
Скорость образования продукта:
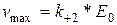 При Е =Е0 скорость будет максимальной:
При Е =Е0 скорость будет максимальной:

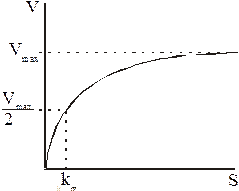
– уравнение Михаэлиса-Ментен
Физический смысл km - это концентрация субстрата, при которой скорость ферментативной реакции принимает величину половины от максимальной.
3.4.1. Ингибирование ферментативных реакций
Дата добавления: 2015-08-01; просмотров: 1486;
