Опыт 1. Влияние концентрации реагирующих веществ на скорость химической реакции
В настоящем опыте исследуется влияние концентрации реагентов на скорость взаимодействия тиосульфата натрия с серной кислотой
Na2S2O3+ H2SO4 = Na2SO4 + SO2 + S + H2O
О скорости реакции можно судить по времени, прошедшем от начала реакции до момента появления в объеме раствора серы (желтоватая муть).
В четыре пробирки налить из бюретки по 6 мл 0,5М раствора серной кислоты. В четыре пронумерованных стаканчика (по 50мл) налить указанное в таблице 1 количество
0,5М раствора тиосульфата натрия и воды. Вылить в стаканчик №1 отмеренные 6 мл серной кислоты, быстро перемешать и измерить время (секунды) до начала появления в объеме раствора мути. Скорость реакции определить как величину, обратно пропорциональную найденному времени. Повторить опыт со стаканчиками №2-№4 и данные занести в таблицу 1.
Таблица 1
| № стакана | Объем раствора, мл | Относительная концентрация
Na2S2O3
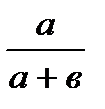
| Время (t), с | Скорость реакции V = 1/t,с-1 | |
| Na2S2O3 а | H2O в | ||||
| 2/3 | |||||
| 1/2 | |||||
| 1/3 |
Результаты наблюдений представить в виде графика: по оси абсцисс отложить относительную концентрацию раствора тиосульфата натрия, по оси ординат – скорость реакции.
Сделать вывод о зависимости скорости реакции от концентрации реагентов.
Дата добавления: 2015-07-24; просмотров: 1920;
